
ЁОЬтФПЁПI.ЯТСаЫЕЗЈжае§ШЗЕФЪЧ ЁЃ
AЃЎБћЯЉЗжзгжага8ИіІвМќЃЌ1ИіІаМќ
BЃЎдкSiO2ОЇЬхжаЃЌ1ИіSiдзгКЭ2ИіOдзгаЮГЩ2ИіЙВМлМќ
CЃЎNF3ЕФЗаЕуБШNH3ЕФЗаЕуЕЭЕУЖрЃЌЪЧвђЮЊNH3ЗжзгМфгаЧтМќЃЌNF3жЛгаЗЖЕТЛЊСІ
DЃЎNCl3КЭBC13ЗжзгжаЃЌжааФдзгЖМВЩгУsp3дгЛЏ
II.ШЫРрдкЪЙгУН№ЪєЕФРњЪЗНјГЬжаЃЌОРњСЫЭЁЂЬњЁЂТСжЎКѓЃЌЕкЫФжжНЋБЛЙуЗКгІгУЕФН№ЪєБЛПЦбЇМвдЄВтЪЧюб(Ti)ЃЌЫќБЛгўЮЊЁАЮДРДЪРМЭЕФН№ЪєЁБЁЃЪдЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉTiдЊЫидкдЊЫижмЦкБэжаЕФЮЛжУЪЧЕк______жмЦкЕк___ ____зхЃЌ
ЦфЛљЬЌдзгЕФЕчзгХХВМЪНЮЊ________ЁЃ
ЃЈ2ЃЉдкTiЕФЛЏКЯЮяжаЃЌПЩвдГЪЯжЃЋ2ЁЂЃЋ3ЁЂЃЋ4Ш§жжЛЏКЯМлЃЌЦфжавдЃЋ4МлЕФTiзюЮЊЮШЖЈЁЃЦЋюбЫсБЕЕФШШЮШЖЈадКУЃЌНщЕчГЃЪ§ИпЃЌдкаЁаЭБфбЙЦїЁЂЛАЭВКЭРЉвєЦїжаЖМгагІгУЃЎЦЋюбЫсБЕОЇЬхжаОЇАћЕФНсЙЙЪОвтЭМШчЭМЫљЪОЃЌЫќЕФЛЏбЇЪНЪЧ ЃЌЦфжаTi4ЃЋЕФбѕХфЮЛЪ§ЮЊ ЃЌBa2ЃЋЕФбѕХфЮЛЪ§ЮЊ ЃЛ

ЃЈ3ЃЉГЃЮТЯТЕФTiCl4ЪЧгаДЬМЄадГєЮЖЕФЮоЩЋЭИУївКЬхЃЌШлЕу-23.2ЁцЃЌЗаЕу136.2ЁцЃЌЫљвдTiCl4гІЪЧ ЛЏКЯЮяЃЌЦфЙЬЬхЪЧ ОЇЬхЁЃTiCl4дкГБЪЊПеЦјжавзЛгЗЂЃЌЫЎНтЖјУААзбЬЃЌетЪЧвђЮЊЫЎНтКѓга________ЩњГЩЁЃ
ЃЈ4ЃЉвбжЊTi3ЃЋПЩаЮГЩХфЮЛЪ§ЮЊ6ЕФХфКЯЮяЃЌЦфПеМфЙЙаЭЮЊе§АЫУцЬхЃЌШчЯТЭМ1ЫљЪОЃЌЮвУЧЭЈГЃПЩвдгУЯТЭМ2ЫљЪОЕФЗНЗЈРДБэЪОЦфПеМфЙЙаЭЃЈЦфжаAБэЪОХфЬхЃЌMБэЪОжааФдзгЃЉЁЃХфЮЛЛЏКЯЮя[Co(NH3)4Cl2]ЕФПеМфЙЙаЭвВЮЊАЫУцЬхаЭЃЌЫќга жжЭЌЗжвьЙЙЬхЃЌЧыдкЯТЭМЗНПђжаНЋЦфЛГіЁЃ

ЁОД№АИЁПЂёЁЂAC
ЂђЁЂЃЈ1ЃЉЫФЃЛIVBЃЛ1s22s22p63s23p63d24s2Лђ[Ar]3d24s2
ЃЈ2ЃЉBaTiO3ЃЛ6ЃЛ12ЃЛ
ЃЈ3ЃЉЙВМлЃЛЗжзгЃЛHC1ЃЛ
ЃЈ4ЃЉ2ЃЛ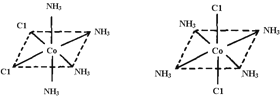
ЁОНтЮіЁП
ЪдЬтЗжЮіЃКЂёЁЂAЃЎБћЯЉЕФНсЙЙМђЪНЮЊCH3-CH=CH2ЃЌC-CЁЂC-HМќОљЮЊІвМќЃЌC=CжавЛИіІвМќЃЌвЛИіІаМќЃЌдђБћЯЉЗжзгга8ИіІвМќКЭ1ИіІаМќЃЌAе§ШЗЃЛBЃЎSiO2ОЇЬхжаЃЌУПИіSiдзгаЮГЩ4ИіЙВМлМќЃЌ1ИіOдзгКЭ2ИіSiдзгаЮГЩ2ИіЙВМлМќЃЌBДэЮѓЃЛCЃЎNF3ЕФЗаЕуБШNH3ЕФЗаЕуЕЭЕУЖрЃЌЪЧвђЮЊNH3ЗжзгМфгаЧтМќЃЌNF3ЗжзгМфжЛгаЗЖЕТЛЊСІЃЌCе§ШЗЃЛDЃЎNCl3жаNаЮГЩ3ИіІвМќЃЌЙТЕчзгЖдЪ§=![]() =1ЃЌЮЊsp3дгЛЏЃЌBCl3жаBаЮГЩ3ИіІвМќЃЌЮоЙТЕчзгЖдЃЌЮЊsp2дгЛЏЃЌDДэЮѓЃЛД№АИбЁACЁЃ
=1ЃЌЮЊsp3дгЛЏЃЌBCl3жаBаЮГЩ3ИіІвМќЃЌЮоЙТЕчзгЖдЃЌЮЊsp2дгЛЏЃЌDДэЮѓЃЛД№АИбЁACЁЃ
ЂђЁЂЃЈ1ЃЉИљОндЊЫижмЦкБэПЩжЊTiдЊЫиЮЛгкдЊЫижмЦкБэЕФЕкЫФжмЦкЕкЂєBзхЃЌTiдЊЫиЪЧ22КХдЊЫиЃЌИљОнКЫЭтЕчзгХХВМЙцТЩПЩжЊЃЌЫќЕФЛљЬЌдзгЕФЕчзгВуХХВМЪНЮЊЃК1s22s22p63s23p63d24s2Лђ[Ar]3d24s2ЃЛ
ЃЈ2ЃЉдкУПИіОЇАћжаОљгавЛИіBaдзгЃЌЫФИіTiдзгБЛЫФИіОЇАћЙВгУЃЌУПИіОЇАћжажЛгавЛИіTiЃЌ12ИіOдзгОљБЛЫФИіОЇАћЙВгУЃЌУПИіОЇАћжаКЌга3ИіOдзгЃЌЙЪЛЏбЇЪНЮЊBaTiO3ЃЌTi4+ЕФбѕХфЮЛЪ§ЮЊ![]() =6ЃЌBa2+ЕФбѕХфЮЛЪ§ЮЊ12ЃК
=6ЃЌBa2+ЕФбѕХфЮЛЪ§ЮЊ12ЃК
ЃЈ3ЃЉГЃЮТЯТЕФTiCl4ЪЧгаДЬМЄадГєЮЖЕФЮоЩЋЭИУївКЬхЃЌШлЕу-23.2ЁцЃЌЗаЕу136.2ЁцЃЌШлЗаЕуНЯЕЭЃЌОЇЬхгЩЗжзгаЮГЩЃЌЪєгкЗжзгОЇЬхЃЌЗжзггЩЙВМлМќаЮГЩЃЌTiCl4дкГБЪЊПеЦјжавзЛгЗЂЃЌЫЎНтЖјУААзбЬЃЌгаHClЩњГЩЃК
ЃЈ4ЃЉCo3+ЮЛгке§АЫУцЬхЕФжааФЃЌNH3КЭCl-ЮЛгке§АЫУцЬхЖЅЕуЃЌЕБСНИіCl-ЯрСкЪБЮЊвЛжжНсЙЙЃЌСНИіCl-ВЛЯрСкЪБЮЊСэвЛжжНсЙЙЃЌЙВгаСНжжНсЙЙЃЌМД ЁЃ
ЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШМСЯЕФЪЙгУКЭЗРЮлШОЪЧЩчЛсЗЂеЙжавЛИіЮоЗЈЛиБмЕФУЌЖмЛАЬтЁЃ
ЃЈ1ЃЉЮвЙњББЗНЖЌМОЩеУКЙЉХЏЫљВњЩњЕФЗЯЦјЪЧЮэіВЕФжївЊРДдДжЎвЛЁЃОбаОПЗЂЯжНЋУКЬПдкO2/CO2ЕФЦјЗеЯТШМЩеЃЌФмЙЛНЕЕЭШМУКЪБNOЕФХХЗХЃЌжївЊЗДгІЮЊЃК2NOЃЈgЃЉ+2COЃЈgЃЉЈTN2ЃЈgЃЉ+2CO2ЃЈgЃЉ ЁїH
ШєЂйN2ЃЈgЃЉ+O2ЃЈgЃЉЈT2NOЃЈgЃЉ ЁїH1=+180.5 kJЁЄmolЃ1
ЂкCOЃЈgЃЉЈTCЃЈsЃЉ+![]() O2ЃЈgЃЉ ЁїH2=+110.5 kJЁЄmolЃ1
O2ЃЈgЃЉ ЁїH2=+110.5 kJЁЄmolЃ1
ЂлCЃЈsЃЉ+O2ЃЈgЃЉЈTCO2ЃЈgЃЉ ЁїH3=Љ393.5 kJЁЄmolЃ1
дђЁїH= kJЁЄmolЃ1ЃЎ
ЃЈ2ЃЉМзДМПЩвдВЙГфКЭВПЗжЬцДњЪЏгЭШМСЯ,ЛКНтФмдДНєеХЁЃвЛЖЈЬѕМўЯТ,дкШнЛ§ЮЊVLЕФУмБеШнЦїжаГфШыa molCOгы2a mol H2КЯГЩМзДМЃЌCOЦНКтзЊЛЏТЪгыЮТЖШЁЂбЙЧПЕФЙиЯЕШчЭМЫљЪОЁЃ

ЂйP1Ѓп P2(ЬюЁАЃОЁБ ЁЂЁА<ЁБ ЛђЁА=ЁБ ),РэгЩЪЧ
ЂкИУМзДМКЯГЩЗДгІдкAЕуЕФЦНКтГЃЪ§K= (гУaКЭVБэЪО)ЁЃ
ЂлЯТСаДыЪЉжаФмЙЛЭЌЪБТњзудіДѓЗДгІЫйТЪКЭЬсИпCOзЊЛЏТЪЕФЪЧ ЁЃ(ЬюаДЯргІзжФИ)
aЁЂЪЙгУИпаЇДпЛЏМС bЁЂНЕЕЭЗДгІЮТЖШ cЁЂдіДѓЬхЯЕбЙЧП
dЁЂВЛЖЯНЋCH3OHДгЗДгІЛьКЯЮяжаЗжРыГіРД eЁЂдіМгЕШЮяжЪЕФСПЕФCOКЭH2
ЃЈ3ЃЉЛњЖЏГЕЕФЮВЦјвВЪЧЮэіВаЮГЩЕФдвђжЎвЛЁЃ

ЂйНќМИФъгаШЫЬсГідкДпЛЏМСЬѕМўЯТ,РћгУЦћгЭжаЛгЗЂГіРДЕФC3H6ДпЛЏЛЙдЮВЦјжаЕФNOЦјЬхЩњГЩШ§жжЮоЮлШОЕФЮяжЪЁЃЧыаДГіИУЙ§ГЬЕФЛЏбЇЗНГЬЪНЃК ЁЃ
ЂкЕчЛЏбЇЦјУєДЋИаЦїЗЈЪЧВтЖЈЦћГЕЮВЦјГЃгУЕФЗНЗЈжЎвЛЁЃЦфжаCOДЋИаЦїЕФЙЄзїдРэШчЩЯЭМЫљЪОЃЌдђЙЄзїЕчМЋЕФЗДгІЪНЮЊ ЁЃ
ЃЈ4ЃЉЙЄвЕЩЯПЩвдгУNaOHШмвКЛђАБЫЎЮќЪеЙ§СПЕФSO2ЃЌЗжБ№ЩњГЩNaHSO3ЁЂNH4HSO3ЃЌЦфЫЎШмвКОљГЪЫсадЁЃЯрЭЌЬѕМўЯТЃЌЭЌХЈЖШЕФСНжжЫсЪНбЮЕФЫЎШмвКжаcЃЈSO32-ЃЉНЯаЁЕФЪЧ ЃЌгУЮФзжКЭЛЏбЇгУгяНтЪЭдвђ ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП COЗжЮівЧвдШМСЯЕчГиЮЊЙЄзїдРэЃЌгУРДВтСПЦћГЕЮВЦјжаЕФCOЕФКЌСПЃЌЦфзАжУШчЭМЫљЪОЃЌИУЕчГижаЕчНтжЪЮЊбѕЛЏюЦЃбѕЛЏФЦЃЌЦфжаO2-ПЩвддкЙЬЬхНщжЪNASICONжаздгЩвЦЖЏЁЃЯТСаЫЕЗЈДэЮѓЕФЪЧЃЈ ЃЉЁЃ

AЃЎИКМЋЕФЕчМЋЗДгІЪНЮЊЃКCO+O2ЁЊЈD2e-ЃНCO2
BЃЎЙЄзїЪБЕчМЋbзїе§МЋЃЌO2-гЩЕчМЋaСїЯђЕчМЋb
CЃЎЙЄзїЪБЕчзггЩЕчМЋaЭЈЙ§ДЋИаЦїСїЯђЕчМЋb
DЃЎДЋИаЦїжаЭЈЙ§ЕФЕчСїдНДѓЃЌЮВЦјжаCOЕФКЌСПдНИп
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгаAЁЂBЁЂCЁЂDЁЂEЮхжждЊЫиЁЃЦфЯрЙиаХЯЂШчЯТЃК
дЊЫи | ЯрЙиаХЯЂ |
A | AдЊЫиЕФвЛжждзгУЛгажазгЃЌжЛгавЛИіжЪзг |
B | BЪЧЕчИКадзюДѓЕФдЊЫи |
C | CЕФЛљЬЌдзг2pЙьЕРгаШ§ИіЮДГЩЖдЕчзг |
D | DЮЊжїзхдЊЫиЃЌЧвгыEЭЌжмЦкЃЌЦфзюЭтВуЩЯгаСНИідЫЖЏзДЬЌВЛЭЌЕФЕчзг |
E | EФмаЮГЩзЉКьЩЋЃЈКьЩЋЃЉЕФE2OКЭEOСНжжбѕЛЏЮя |
ЛиД№ЯТСаЮЪЬтЁЃ
ЃЈ1ЃЉаДГіEдЊЫидзгЛљЬЌЪБMВуЕФЕчзгХХВМЪН ЁЃ
ЃЈ2ЃЉCдЊЫиЕЅжЪЗжзгжаКЌгаІФКЭІаМќЕФМќЪ§жЎБШЮЊ ЁЃ
ЃЈ3ЃЉНтЪЭдкЫЎжаЕФШмНтЖШC7H15OHБШввДМЕЭЕФдвђЪЧЃК ЁЃ
ЃЈ4ЃЉAЁЂCЁЂEШ§жждЊЫиПЩаЮГЩЃКEЃЈCA3ЃЉ42+ХфРызгЃЌЦфжаДцдкЕФЛЏбЇМќРраЭга ЃЈЬюађКХЃЉЁЃ
ЂйХфЮЛМќ ЂкН№ЪєМќ ЂлМЋадЙВМлМќ ЂмЗЧМЋадЙВМлМќ ЂнРызгМќ ЂоЧтМќ
Шє EЃЈCA3ЃЉ42+ОпгаЖдГЦЕФПеМфЙЙаЭЃЎЧвЕБ EЃЈCA3ЃЉ42+жаЕФСНИіCA3ЗжзгБЛСНИіClШЁДњЪБЃЎФмЕУЕНСНжжВЛЭЌНсЙЙЕФВњЮяЃЌдђ EЃЈCA3ЃЉ42+ЕФПеМфЙЙаЭЮЊ ЃЈЬюађКХЃЉЁЃ
aЃЎЦНУце§ЗНаЮ bЃЎе§ЫФУцЬх cЃЎШ§НЧзЖаЭ dЃЎVаЭ
ЃЈ5ЃЉШ§СђЛЏЫФСзЪЧЛЦТЬЩЋеызДНсОЇЃЌЦфНсЙЙШчЭМЫљЪОЁЃ

Ш§СђЛЏЫФСзЗжзгжаPдзгВЩШЁ____дгЛЏЃЌгыPO3ЃЛЅЮЊЕШЕчзгЬхЕФЛЏКЯЮяЗжзгЕФЛЏбЇЪНЮЊ________ЁЃгУNAБэЪОАЂЗќМгЕТТоГЃЪ§ЕФЪ§жЕЃЌ0ЃЎ1molШ§СђЛЏЫФСзЗжзгжаКЌгаЕФЙТЕчзгЖдЪ§ЮЊ_________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТУцЪЧРћгУбЮЧХЕчГиДгФГаЉКЌЕтбЮжаЬсШЁЕтЕФСНИізАжУ, ЯТСаЫЕЗЈжае§ШЗЕФЪЧ
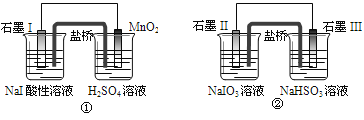
AЃЎСНИізАжУжаЪЏФЋIКЭЪЏФЋIIзїИКМЋ
BЃЎЕтдЊЫидкзАжУЂйжаБЛбѕЛЏЃЌдкзАжУЂкжаБЛЛЙд
CЃЎЂйжаMnO2ЕФЕчМЋЗДгІЪНЮЊЃКMnO2+2H2O+2e-==Mn2++4OH
DЃЎЗДгІЂйЁЂЂкжаЩњГЩЕШСПЕФI2ЪБЕМЯпЩЯЭЈЙ§ЕФЕчзгЪ§жЎБШЮЊ1ЁУ5
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЕЊЕФЛЏКЯЮядкЩњВњЩњЛюжаЙуЗКДцдкЁЃ
ЃЈ1ЃЉЂйТШАЗЃЈNH2ClЃЉЕФЕчзгЪНЮЊ ЁЃПЩЭЈЙ§ЗДгІNH3(g)ЃЋCl2(g)=NH2Cl(g)ЃЋHCl(g)жЦБИТШАЗЃЌвбжЊВПЗжЛЏбЇМќЕФМќФмШчЯТБэЫљЪОЃЈМйЖЈВЛЭЌЮяжЪжаЭЌжжЛЏбЇМќЕФМќФмвЛбљЃЉЃЌдђЩЯЪіЗДгІЕФІЄH= ЁЃ
ЂкNH2ClгыЫЎЗДгІЩњГЩЧПбѕЛЏадЕФЮяжЪЃЌПЩзїГЄаЇЛКЪЭЯћЖОМСЃЌИУЗДгІЕФЛЏбЇЗНГЬЪНЮЊ ЁЃ
ЃЈ2ЃЉгУНЙЬПЛЙдNOЕФЗДгІЮЊЃК2NO(g)+C(s) ![]() N2(g)+CO2(g)ЃЌЯђШнЛ§ОљЮЊ1 LЕФМзЁЂввЁЂБћШ§ИіКуШнКуЮТЃЈЗДгІЮТЖШЗжБ№ЮЊ400ЁцЁЂ400ЁцЁЂTЁцЃЉШнЦїжаЗжБ№МгШызуСПЕФНЙЬПКЭвЛЖЈСПЕФNOЃЌВтЕУИїШнЦїжаn(NO)ЫцЗДгІЪБМфtЕФБфЛЏЧщПіШчЯТБэЫљЪОЃК
N2(g)+CO2(g)ЃЌЯђШнЛ§ОљЮЊ1 LЕФМзЁЂввЁЂБћШ§ИіКуШнКуЮТЃЈЗДгІЮТЖШЗжБ№ЮЊ400ЁцЁЂ400ЁцЁЂTЁцЃЉШнЦїжаЗжБ№МгШызуСПЕФНЙЬПКЭвЛЖЈСПЕФNOЃЌВтЕУИїШнЦїжаn(NO)ЫцЗДгІЪБМфtЕФБфЛЏЧщПіШчЯТБэЫљЪОЃК

ЂйИУЗДгІЮЊ ЃЈЬюЁАЗХШШЁБЛђЁАЮќШШЁБЃЉЗДгІЁЃ
ЂкввШнЦїдк200 minДяЕНЦНКтзДЬЌЃЌдђ0ЁЋ200 minФкгУNOЕФХЈЖШБфЛЏБэЪОЕФЦНОљЗДгІЫйТЪv(NO)= ЁЃ
ЃЈ3ЃЉгУНЙЬПЛЙдNO2ЕФЗДгІЮЊЃК2NO2(g)+2C(s)![]() N2(g)+2CO2(g)ЃЌдкКуЮТЬѕМўЯТЃЌ1 mol NO2КЭзуСПCЗЂЩњИУЗДгІЃЌВтЕУЦНКтЪБNO2КЭCO2ЕФЮяжЪЕФСПХЈЖШгыЦНКтзмбЙЕФЙиЯЕШчЭМЫљЪОЃК
N2(g)+2CO2(g)ЃЌдкКуЮТЬѕМўЯТЃЌ1 mol NO2КЭзуСПCЗЂЩњИУЗДгІЃЌВтЕУЦНКтЪБNO2КЭCO2ЕФЮяжЪЕФСПХЈЖШгыЦНКтзмбЙЕФЙиЯЕШчЭМЫљЪОЃК

ЂйAЁЂBСНЕуЕФХЈЖШЦНКтГЃЪ§ЙиЯЕЃКKc(A) Kc(B)ЃЈЬюЁАЃМЁБЛђЁАЃОЁБЛђЁА=ЁБЃЉЁЃ
ЂкAЁЂBЁЂCШ§ЕужаNO2ЕФзЊЛЏТЪзюИпЕФЪЧ ЃЈЬюЁАAЁБЛђЁАBЁБЛђЁАCЁБЃЉЕуЁЃ
ЂлМЦЫуCЕуЪБИУЗДгІЕФбЙЧПЦНКтГЃЪ§Kp(C)= ЃЈKpЪЧгУЦНКтЗжбЙДњЬцЦНКтХЈЖШМЦЫуЃЌЗжбЙЃНзмбЙЁСЮяжЪЕФСПЗжЪ§ЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгаAЁЂBЁЂCЁЂDЁЂEЮхжжЖЬжмЦкдЊЫи, ЫќУЧЕФдзгађЪ§вРДЮдіДѓЁЃ вбжЊAКЭBдзгОпгаЯрЭЌЕФЕчзгВуЪ§, ЧвAЕФзюЭтВуЕчзгЪ§ЪЧДЮЭтВуЕчзгЪ§ЕФСНБЖ, CЪЧИУжмЦкжадзгАыОЖзюДѓЕФдЊЫиЃЌ CЕФЕЅжЪдкМгШШЯТгыBЕФЕЅжЪГфЗжЗДгІ, ПЩвдЕУЕНгыDЕЅжЪбеЩЋЯрЭЌЕФЕЛЦЩЋЙЬЬЌЛЏКЯЮя,EгыDЯрСкЁЃ ЪдИљОнвдЩЯа№ЪіЛиД№:
ЃЈ1ЃЉдЊЫиУћГЦ: A C __________ E
ЃЈ2ЃЉаДГіAB2гыЙ§СПЧтбѕЛЏФЦШмвКЗДгІЕФРызгЗНГЬЪН ;аДГі C2B2гыAB2ЗДгІЕФЛЏбЇЗНГЬЪН ;
ЃЈ3ЃЉЛГіDЕФдзгНсЙЙЪОвтЭМ ,гУЕчзгЪНБэЪОЛЏКЯЮя C2D ЕФаЮГЩЙ§ГЬ ;
ЃЈ4ЃЉDЁЂEЕФЦјЬЌЧтЛЏЮяЕФЮШЖЈад Дѓгк ЃЈЬюЛЏбЇЪНЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯжгаAЁЂBСНжжЬўЃЌвбжЊAЕФЗжзгЪНЮЊC5HmhtЃЌBЕФзюМђЪНЮЊC5Hn(mЁЂnОљЮЊе§ећЪ§)ЁЃЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЯТСаЙигкЬўAКЭЬўBЕФЫЕЗЈВЛе§ШЗЕФЪЧ (ЬюађКХ)ЁЃ
a.ЬўAКЭЬўBПЩФмЛЅЮЊЭЌЯЕЮя
b.ЬўAКЭЬўBПЩФмЛЅЮЊЭЌЗжвьЙЙЬх
c.ЕБm=12ЪБЃЌЬўAвЛЖЈЮЊЭщЬў
d.ЕБn=11ЪБЃЌЬўBПЩФмЕФЗжзгЪНга2жж
ЃЈ2ЃЉШєЬўAЮЊСДЬўЃЌЧвЗжзгжаЫљгаЬМдзгЖМдкЭЌвЛЬѕжБЯпЩЯЃЌдђAЕФНсЙЙМђЪНЮЊ ЁЃ
ЃЈ3ЃЉШєЬўAЮЊСДЬўЃЌЧвЗжзгжаЫљгаЬМдзгвЛЖЈЙВУцЃЌдквЛЖЈЬѕМўЯТЃЌ1 mol AзюЖрПЩгы1 mol H2МгГЩЃЌдђAЕФУћГЦЪЧ ЁЃ
ЃЈ4ЃЉШєЬўBЮЊБНЕФЭЌЯЕЮяЃЌШЁвЛЖЈСПЕФЬўBЭъШЋШМЩеКѓЃЌЩњГЩЮяЯШЭЈЙ§зуСПЕФХЈСђЫсЃЌХЈСђЫсЕФжЪСПдіМг1.26 gЃЌдйЭЈЙ§зуСПЕФМюЪЏЛвЃЌМюЪЏЛвЕФжЪСПдіМг4.4 gЃЌдђЬўBЕФЗжзгЪНЮЊ ЃЛШєЦфБНЛЗЩЯЕФвЛфхДњЮяжЛгавЛжжЃЌдђЗћКЯДЫЬѕМўЕФЬўBга жжЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЧІаюЕчГиОпгаЕчбЙЮШЖЈЃЌадФмСМКУЃЌАВШЋПЩППЃЌбЛЗЪЙгУЕШгХЕуЁЃЦфЗДгІЗНГЬЪНШчЯТЪНЃКPb (s)+ PbO2(s) +2H2SO4(aq) ![]() 2PbSO4(s) +2H2O(l)ЁЃ
2PbSO4(s) +2H2O(l)ЁЃ
ЃЈ1ЃЉЗХЕчЪБЃЌИКМЋЗЂЩњ_________ЗДгІЃЈЬюЁАбѕЛЏЁБЛђЁАЛЙдЁБЃЉЃЌЦфЕчМЋЗДгІЪНЮЊ______________________________ЃЌ
ЃЈ2ЃЉГфЕчЪБЃЌбєМЋЗЂЩњ___________ЗДгІЃЈЬюЁАбѕЛЏЁБЛђЁАЛЙдЁБЃЉЃЌЦфЕчМЋЗДгІЪНЮЊ_____________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com