
【题目】将Mg、Cu 组成的2.64g固体混合物投入适量稀稍酸中恰好完全反应,收集还原产物气体NO(还原产物只有一种)。然后向反应后的溶液中加入一定浓度的氢氧化钠溶液,使金属恰好沉淀完全,此时生成沉淀的质量为4.68g,则反应过程中收集到NO气体(标况下)体积为( )
A. 8.96LB. 0.896LC. 4.48LD. 0.448L
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
A. 标准状况下22.4L异丁烷的分子数为NA
B. 78g苯(C6H6)和苯乙烯(C8H8)的混合物中含有的碳氢键数一定为6NA
C. 某温度下,1LpH=3的醋酸溶液稀释到10L时,溶液中H+的数目大于0.01NA
D. 3.0g含甲醛(HCHO)的冰醋酸中含有的原子总数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从自然界直接获取的能源称为一次能源,一次能源经加工、转换得到的能源称为二次能源。下列说法不正确的是
A.天然气、太阳能都是一次能源,而氢气是二次能源
B.吸热反应都需要加热到一定温度后才能进行的说法是不正确的
C.用水一次性就能区分出氯化钠、氢氧化钠、硝酸铵、碳酸钙四种固体
D.常温常压下,1molC2H2完全燃烧时放出热量为1299.6kJ,则表示乙炔完全燃烧的热化学方程式为:2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g)△H=-2599.2kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知烃A能使溴水褪色,其产量可以用来衡量一个国家石油化工发展水平。A、B、C、D、E、F、G转化关系如下(以下变化中,有些反应条件及产物未标明)。其中G是天然有机高分子化合物,C、F能发生银镜反应,E分子具有浓郁的果香味,其相对分子质量为88。
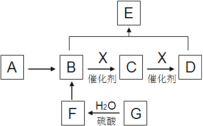
(1)写出A分子的电子式:__________;G的分子式:__________
(2)写出分子式与B相同,但不能与金属钠反应的物质的结构简式__________
(3)写出B+D→E的化学方程式:__________
(4)B→C的反应类型为__________;物质C、F__________(填“是”或“不是”)同一类物质。
(5)F→B过程中还产生了另外一种气态物质M,请简述实验室检验气体M的方法:__________。
(6)工业上制备物质E的方法有多种。其中A与D以物质的量比1:1反应生成E,请判断其反应类型为__________。
(7)E的同分异构体中,能与Na反应,又能与Na2CO3溶液反应的物质是__________(用结构简式书写一种即可)
(8)物质X可由如图装置制备。
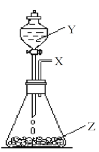
①若Z是一种淡黄色固体,则锥形瓶中发生反应的化学方程式是______________________________
②若Z是一种黑色粉末,则物质Y是__________,Z的作用是__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是( )
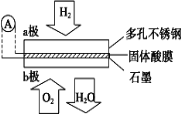
A. b 极上的电极反应式为:O2+2H2O+4e-=4OH-
B. 每转移0.1mol电子,消耗1.12L的H2
C. H+由a极通过固体酸电解质传递到b极
D. 电子通过外电路从b极流向a极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在CO2中,Mg燃烧生成MgO和C。下列说法正确的是( )
A. 元素C的单质只存在金刚石和石墨两种同素异形体
B. Mg、MgO中镁元素微粒的半径:r(Mg2+)>r(Mg)
C. 在该反应条件下,Mg的还原性强于C的还原性
D. 该反应中化学能全部转化为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常温下的六份溶液:①0.01mol/LCH3COOH溶液;②0.01mol/LHCl溶液;③pH=12的氨水;④pH=12的NaOH溶液;⑤0.01mol/LCH3COOH溶液与 pH=12的氨水等体积混合后所得溶液;⑥0.01mol/LHCl溶液与 pH=12的NaOH溶液等体积混合所得溶液。
(1)其中水的电离程度最大的是________(选填序号,下同),水的电离程度相同的是_________;
(2)若将②、③混合后所得溶液 pH=7,则消耗溶液的体积:②______③(选填“>”、“<”或“=”,下同);若将②、③溶液等体积混合后,所得溶液 pH_____________7。
(3)若将①、④溶液按体积比为2:1混合后,所得溶液pH______7(选填“>”、“<”或“=”)此时溶液中除水分子外的各微粒的浓度由大到小的顺序为:__________;将①、④混合,若有c(CH3COO-)>c(H+),则混合液可能呈_________(填序号)。
A.酸性 B.碱性 C.中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大。在如图所示的物质转化关系中,p、q、m、n分别是元素W、X、Y、Z的气体单质,p和s均为有色气体,v的水溶液呈碱性。常温,0.1mol/Lt溶液与0.1mol/L u溶液的pH均为1,下列说法正确的是( )
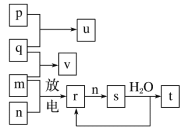
A. 元素的非金属性:Z>Y>X,原子半径:X<Z<Y
B. Y、W的氧化物对应的水化物均为强酸
C. s溶于水的反应中,氧化剂与还原剂的物质的量之比为2∶1
D. v的电子式可表示为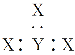
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表代表周期表中的几种短周期元素,下列说法中错误的是

A. A、B、C第一电离能的大小顺序为C>B>A
B. C、D气态氢化物稳定性强弱和沸点高低均为C>D
C. AD3和ED4两分子的中心原子均为sp3杂化
D. ED4分子中各原子均达8电子结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com