
����Ŀ����ҵ�������̿�(ֻ��MnO2��MnO)��H2SO4(����)��FeS2�Ʊ�MnSO4��H2O����������(��֪�����е�FeS2��FeSO4��MnO2��MnO����ȫ��Ӧ)��

��1����֪����ֻ��������Ӧ������������Ӧ��
MnO+H2SO4MnSO4+H2O
FeS2+H2SO4FeSO4+H2S��+S��
��ɵ�������Ӧ��
___MnO2+___FeSO4+___ ____________MnSO4+___ _________+___ _________
��2������A��B�Ļ�ѧʽ�ֱ���____________________��__________________��
��3����ҺX�е�������__________��ʵ������Ũ����ҺYʱʹ�õIJ���������___________________��
��4�����õ��ij���A��������MnSO4��H2O�������ֱ�Ϊ96.0 g��321.1 g�����м����MnOΪ0.1 mol�������������̿���MnO2��MnO�����ʵ���֮��Ϊ____________��
���𰸡�1 2 2 H2SO4 1 1 Fe2(SO4)3 2 H2O S Fe(OH)3 MnSO4��Fe2(SO4)3��H2SO4 ���������ƾ��� 5��1
��������
��1���������⣬��Ӧ����Ҫ�������ᣬ�ṩ���Ի��������ݵ�ʧ�����غ��Ԫ���غ���ƽ����ʽ����2������������Ӧ����ʽ��ת����ϵ�жϳ���A����ҺX�м���MnO������Һ��pH����������Fe(OH)3��������3������������Ӧ����ʽ�ж���ҺX�е���������������Ũ��������������4�����ݹ�ϵʽ��2S~2FeSO4~MnO2������MnO2�����ʵ�����������Ԫ���غ�������̿���MnO�����ʵ�����
��1����Ӧ����Ҫ�������ᣬ�ṩ���Ի�������Ԫ�ػ��ϼ���+4��Ϊ+2��������Ԫ�ػ��ϼ���+2����Ϊ+3�������������ɣ�����Ԫ���غ㣬�����л���ˮ���ɣ����Է�Ӧ����ʽ�� 1 MnO2+2_FeSO4+2H2SO41 MnSO4+ 1 Fe2(SO4)3+2H2O����2������FeS2+H2SO4FeSO4+H2S��+S����֪����AΪ���ʣ���ҺX����MnO������Һ��pH������BΪFe(OH)3����3������������Ӧ����ʽ����֪��ҺX�к�������H2SO4����Ӧ���ɵ�MnSO4��Fe2(SO4)3������ҺX�е�������MnSO4��Fe2(SO4)3��H2SO4����������ʱʹ�õIJ��������в��������ƾ��ơ���4�����ݹ�ϵʽ��2S~2FeSO4~MnO2��n(MnO2)=![]() n(S)
n(S)![]() ��
��![]() =1.5 mol��n(MnSO4��H2O)=
=1.5 mol��n(MnSO4��H2O)=![]() =1.9 mol��������Ԫ���غ��֪n(MnO)=1.9 mol1.5 mol0.1 mol=0.3 mol�������������̿���MnO2��MnO�����ʵ���֮��Ϊ5��1��
=1.9 mol��������Ԫ���غ��֪n(MnO)=1.9 mol1.5 mol0.1 mol=0.3 mol�������������̿���MnO2��MnO�����ʵ���֮��Ϊ5��1��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)7.8g Na2R����0.2mol Na+,��Na2R��Ħ������Ϊ______
(2)��4g NaOH�ܽ���10mLˮ�У���ϡ�ͳ�1L������ȡ��10mL����10mL��Һ�����ʵ���Ũ��Ϊ______.
(3)NAΪ�����ӵ���������֪a gij�����к�������Ϊb����������Ħ������Ϊ______.
(4)��״����,3.4g NH3���״����______LH2S������ͬ��Ŀ����ԭ�ӡ�
(5)ͬ��ͬѹ,��������O2��SO2�����ǵ����ʵ���֮��Ϊ______������ԭ����֮��Ϊ______���ܶ�֮��______.
(6)��״����,��VL HCl��������100mLˮ(�ܶ���1g/mL)�У�������Һ�ܶ�Ϊ��g/mL�������������ʵ���Ũ��Ϊ______.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�ҷ��ֶ�ұ�����е�⾫���ᴿ�ɽ��ߴ����Ʊ��ɱ�����ص���װ����ͼ��ʾ����Cu-Si�Ͻ�����Դ����950����������Һ���ν��е�⾫�����й�˵����ȷ����

A.������Һ̬Cu-Si�Ͻ�����������Һ̬���缫
B.Һ̬���缫��������������Ϊ���ص�����
C.�ڸ�Һ��������Cu������Si��������Si4+������Cu2+����ԭ
D.����Һ���ε�������ʹ�����ܹ����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(Ga)����ͬ���壬������Ϊ����������������������������Ϊ���Ի������ҵ�Ʊ��ص�������ͼ��ʾ��
![]()
�����жϲ��������ǣ� ��
A. Al��Ga�����ڢ�A��B. Ga2O3�������ᷴӦ����GaCl3
C. ���ԣ�Al(OH)3��Ga(OH)3D. Ga(OH)3����NaOH��Ӧ����NaGaO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������̼�ܵ����Ƴɹ������˿Ƽ��Ľ������õ绡���ϳɵ�����̼�ܳ����д���������̼������������̼���������������������ᴿ���˷�Ӧ�еķ�Ӧ�����������C��CO2��H2SO4��K2Cr2O7��Cr2(SO4)3��K2SO4��H2O�������ʡ�
(1)����̼��������ɢ��һ���ܼ��У��γ��ȶ��ķ�ɢϵ���������е�������__________��
�ٶ����ЧӦ���ڼ��뱥��(NH4)2SO4��Һ�����۳����ۿ�ͨ����Ĥ
(2)��������������գ�����ƽ��ѧ����ʽ��____C��____��____H2SO4��____K2SO4��________��____Cr2(SO4)3��____H2O��
(3)H2SO4��������Ӧ�б��ֳ�����������________(��ѡ����)��
A�������� B�������Ժ�����
C������ D����ԭ�Ժ�����
(4)����Ӧ�е���ת����0.8 mol��������������ڱ�״���µ����Ϊ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���飨Bi��λ��Ԫ�����ڱ���VA�壬���̬Ϊ+3ʱ���ȶ��������ƣ�NaBiO3����Һ����ɫ����ȡһ�����������̣�MnSO4����Һ�����������εμ�������Һ����Ӧ�����������ʾ��

��NaBiO3��KMnO4��I2��H2O2����������ǿ������˳��Ϊ�� ��
A. I2��H2O2��KMnO4��NaBiO3B. H2O2��I2��NaBiO3��KMnO4
C. NaBiO3��KMnO4��H2O2��I2D. KMnO4��NaBiO3��I2��H2O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص�Ũ�����Լ���ǩ�ϵIJ������ݣ����ø�Ũ��������480mL1mol��L��1��ϡ���ᡣ�ɹ�ѡ�õ������У��ٽ�ͷ�ιܢ���ƿ���ձ�����������ҩ�ע���Ͳ��������ƽ��

��ش��������⣺
��1������������ʵ���Ũ��Ϊ___ mol��L��1��
��2������ϡ����ʱ����ȱ�ٵ�������____(д��������)��
��3�������㣬����480mL 1mol�� L��1��ϡ������Ҫ����Ͳ��ȡ����Ũ��������Ϊ___mL��
��4���������Ƶ�ϡ������вⶨ��������Ũ�ȴ���1 mol��L��1�����ƹ��������и�������������������ԭ����___�����ţ���
A������ʱ����������ƿ�̶��߽��ж��ݡ�
B����ϡ�ͺ��ϡ��������ת������ƿ�����žͽ����Ժ��ʵ�������
C��ת����Һʱ��������������Һ��������ƿ���档
D������ƿ������ˮϴ�Ӻ�δ���������������ˮ��
E�����ݺ�����ƿ����ҡ�Ⱥ���Һ����ڿ̶��ߣ��㲹�伸��ˮ���̶ȴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����辫ȷ����480mL0.100mol/L��CuSO4��Һ�����²�����ȷ����
A.��ȡ7.68gCuSO4�����500mL��Һ
B.��ȡ12.0g���������500mL��Һ
C.��ȡ8.0gCuSO4������500mLˮ
D.��ȡ12.5g���������500mL��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���ѧ��������ش��������⣺
��1����ͼ�Ǻ�C��H��O����Ԫ�ص�ij�л�����ģ�ͣ�ͼ��������֮������ߴ���������˫���Ȼ�ѧ�����������������ŵ�����Ϊ_______________________

��2��![]() �����ƣ�ϵͳ������________
�����ƣ�ϵͳ������________![]() �ķ���ʽΪ _________
�ķ���ʽΪ _________
��3������ʽΪC5H10��������ϩ��ͬ���칹����_______�֣������������칹��
��4��ij�л�������A�����ϣ��������к�̼Ϊ72.0%������Ϊ6.67%������Ϊ�����������з����ⶨ���л����������Է��������ͷ��ӽṹ��
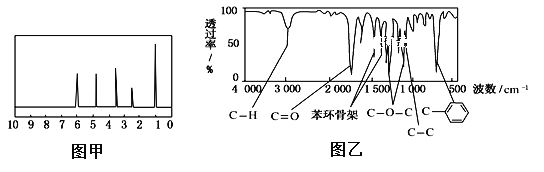
����һ��������������֪A����Է�������Ϊ150��
���������˴Ź����Dz��A�ĺ˴Ź���������5���壬�����֮��Ϊ1:2:2:2:3����ͼ����ʾ��
�����������ú�������Dz��A���ӵĺ��������ͼ����ʾ��
��A�ķ���ʽΪ________��д������������A��һ�ֽṹ��ʽ____________
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com