
【题目】氮的单质及其化合物在生活和生产中有很重要的用途。
(1)氨是合成硝酸、铵盐和氮肥的基本原料。在一定条件下用氮气和氢气合成氨气,然后再用氨氧化法制取硝酸。在整个生产过程中,氮气的利用率为85%。写出氨氧化法制取硝酸的反应式____________现有0.2t液态氮,能生产出浓度为40%的硝酸______________千克。
(2)向27.2 g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5 L,固体物质完全反应,生成NO和Cu(NO3)2。在所得溶液中加入1.0 mol·L-1的NaOH溶液1.0 L,此时溶液呈中性。金属离子已完全沉淀,沉淀质量为39.2 g。
①Cu与Cu2O的物质的量之比?____________
②硝酸的物质的量浓度?___________
(3)将30mLNO和O2混合气体通入过量NaOH溶液中,充分反应后,溶液中只含两种溶质(不考虑水解),且剩余气体体积为2mL。求原混合气体中NO和O2体积比?______________
【答案】4NH3+5O2![]() 4NO+6H2O,2NO+O2=2NO2,3NO2+H2O=2HNO3+NO 1912.5 2∶1 2.4mol/L 3:2或8:7
4NO+6H2O,2NO+O2=2NO2,3NO2+H2O=2HNO3+NO 1912.5 2∶1 2.4mol/L 3:2或8:7
【解析】
(1)氨氧化法制取硝酸流程为:氨气催化氧化生成NO,然后NO与氧气反应生成NO2,最后NO2与水反应生成HNO3;根据关系式N2~2HNO3计算生产浓度40%的硝酸的质量;
(2)在所得溶液中加入1L NaOH溶液,反应后溶液呈中性,金属离子已完全沉淀,溶液中溶质为NaNO3,n(NaNO3)=n(NaOH)=1.0mol/L×1.0L=1mol,沉淀为Cu(OH)2,质量为39.2g,氢氧化铁物质的量为:![]() =0.4mol,根据铜元素守恒有n(Cu)+2n(Cu2O)=n[Cu(OH)2],反应后的溶液中n[[Cu(NO3)2]=n[Cu(OH)2]=0.4mol;
=0.4mol,根据铜元素守恒有n(Cu)+2n(Cu2O)=n[Cu(OH)2],反应后的溶液中n[[Cu(NO3)2]=n[Cu(OH)2]=0.4mol;
①设Cu和Cu2O的物质的量分别为xmol、ymol,根据二者质量及Cu元素物质的量列方程计算二者的物质的量之比;
②利用电子转移守恒计算n(NO),根据N元素守恒可知原硝酸溶液n(HNO3)=n(NO)+n(NaNO3),根据Na元素可知n(NaNO3)=n(NaOH),进而计算硝酸浓度;
(3)氢氧化钠溶液过量,反应后溶液中只含两种溶质,则反应生成NaNO3,发生的反应为:4NO+3O2+4NaOH=4NaNO3+2H2O,剩余的气体可能为氧气,也可能为NO,根据反应方程式进行讨论计算出混合气体中NO与O2的体积。
(1)氨氧化法制取硝酸的反应式:4NH3+5O2![]() 4NO+6H2O,2NO+O2=2NO2,3NO2+H2O=2HNO3+NO;设能生产出浓度为40%的硝酸x千克,则:
4NO+6H2O,2NO+O2=2NO2,3NO2+H2O=2HNO3+NO;设能生产出浓度为40%的硝酸x千克,则:
N2~~~2HNO3
28126
200千克×85% 40%×x千克
则28:126=200千克×85%:40%×x千克,解得x=1912.5;故答案为:4NH3+5O2![]() 4NO+6H2O,2NO+O2=2NO2,3NO2+H2O=2HNO3+NO; 1912.5;
4NO+6H2O,2NO+O2=2NO2,3NO2+H2O=2HNO3+NO; 1912.5;
(2)①在所得溶液中加入NaOH溶液后,此时溶液呈中性,金属离子已完全沉淀,溶液中溶质为NaNO3,n(NaNO3)=n(NaOH)=1.0mol/L×1.0L=1mol,沉淀为Cu(OH)2,质量为39.2g,Cu(OH)2的物质的量为:![]() =0.4mol,根据铜元素守恒有:n(Cu)+2n(Cu2O)=n[Cu(OH)2],所以反应后的溶液中n[[Cu(NO3)2]=n[Cu(OH)2]=0.4mol,设Cu和Cu2O的物质的量分别为xmol、ymol,根据二者质量可得:64x+144y=27.2,根据铜元素守恒有:x+2y=0.4,联立方程解得:x=0.2,y=0.1,所以原固体混合物中Cu和Cu2O的物质的量之比为2:1,故答案为:2:1;
=0.4mol,根据铜元素守恒有:n(Cu)+2n(Cu2O)=n[Cu(OH)2],所以反应后的溶液中n[[Cu(NO3)2]=n[Cu(OH)2]=0.4mol,设Cu和Cu2O的物质的量分别为xmol、ymol,根据二者质量可得:64x+144y=27.2,根据铜元素守恒有:x+2y=0.4,联立方程解得:x=0.2,y=0.1,所以原固体混合物中Cu和Cu2O的物质的量之比为2:1,故答案为:2:1;
②根据电子转移守恒可知:3n(NO)=2n(Cu)+2n(Cu2O),即3n(NO)=2×0.2mol+2×0.1mol,则n(NO)=0.2mol,根据N元素守恒可知n(HNO3)=n(NO)+n(NaNO3)=0.2mol+1.0mol/L×1.0L=1.2mol,所以原硝酸溶液的浓度为![]() =2.4mol/L,故答案为:2.4mol/L;
=2.4mol/L,故答案为:2.4mol/L;
(3)氢氧化钠溶液过量,反应后溶液中只含两种溶质,则反应生成NaNO3,发生的反应为:4NO+3O2+4NaOH=4NaNO3+2H2O,发生反应的NO和O2的总体积为:30mL-2mL=28mL,
若剩余的2mL为NO时,氧气体积为28mL×![]() =12mL,NO体积为:30mL-12mL=18mL,原混合气体中NO和O2体积比18mL:12mL=3:2;若剩余的2mL为氧气时,NO体积为28mL×
=12mL,NO体积为:30mL-12mL=18mL,原混合气体中NO和O2体积比18mL:12mL=3:2;若剩余的2mL为氧气时,NO体积为28mL×![]() =16mL,氧气体积为:30mL-16mL=14mL,原混合气体中NO和O2体积比16mL:14mL=8:7;故答案为:3:2或8:7。
=16mL,氧气体积为:30mL-16mL=14mL,原混合气体中NO和O2体积比16mL:14mL=8:7;故答案为:3:2或8:7。


科目:高中化学 来源: 题型:
【题目】港珠澳大桥设计寿命达120年,对桥体钢构件采用的主要的防腐方法有:①铜梁上安装铝片;②使用高性能富锌(富含锌粉)底漆;③使用高附着性防腐涂料;④预留钢铁腐蚀量。下列分析不正确的是( )
A.①②防腐原理是牺牲阳极的阴极保护法
B.方法①②③只能减缓钢铁腐蚀,未能完全消除
C.钢铁发生吸氧腐蚀时的负极反应式为:![]()
D.防腐涂料可以防水、隔绝空气,降低钢铁在海水中析氢腐蚀速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢溴酸是无色、易挥发的液体,在化工领域用途广泛。实验室模拟一种工业制备氢溴酸的主要流程如下:
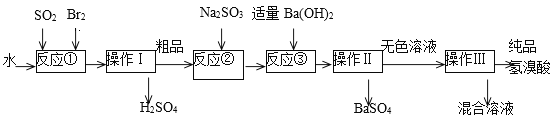
(1)写出反应①的离子方程式___________该反应需要在冰水浴中进行,可能的原因是____________。
(2)操作I的名称__________。
(3)反应②中Na2SO3的目的是_____________________。
(4)操作Ⅱ用到的玻璃仪器有烧杯、_____________________。
(5)工业生产中制得的氢溴酸带有淡淡的黄色。于是甲乙两同学设计了实验加以探究:
①甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,则用于证明该假设所用的试剂为_________,若假设成立可观察到的现象为____________________。
②乙同学假设工业氢溴酸呈淡黄色是因为____,其用于证明该假设成立的方法为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】7.8克过氧化钠固体在常温低压下,与一定量的水蒸气反应,最终得到固体16.8克,此固体物质中一定含有
A.NaOH·H2OB.NaOHC.Na2O2·2H2OD.Na2O2·8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符合的是( )

A.图1表示相同温度下,向pH=10的氢氧化钠溶液和氨水中分别加水稀释时pH变化曲线,其中a表示氨水稀释时pH的变化曲线
B.图2表示已达平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂
C.图3表示工业上用CO生产甲醇的反应CO(g)+2H2(g)![]() CH3OH(g),该反应的ΔH=-91 kJ·mol-1
CH3OH(g),该反应的ΔH=-91 kJ·mol-1
D.图4表示10 mL 0.01 mol·L-1酸性KMnO4溶液与过量的0.1 mol·L-1H2C2O4溶液混合时,n(Mn2+)随时间的变化(Mn2+对该反应有催化作用)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时有关物质的颜色和溶度积(Ksp)如下表:
物质 | AgCl | AgBr | AgI | Ag2S |
颜色 | 白 | 淡黄 | 黄 | 黑 |
Ksp | 1.8×10-10 | 7.7×10-13 | 1.5×10-16 | 1.8×10-50 |
下列叙述中不正确的是( )
A.向AgCl的白色悬浊液中加入0.1 mol/L KI溶液,有黄色沉淀产生
B.25 ℃时,利用表中的溶度积(Ksp),可以计算AgCl、AgBr、AgI、Ag2S饱和水溶液中Ag+的浓度
C.25 ℃,AgCl固体分别在等物质的量浓度NaCl、CaCl2溶液中溶解达到平衡,两溶液中,c(Ag+)和溶度积均相同
D.在5 mL 1.8×10-6 mol/L NaCl溶液中,加入1滴(20滴约为1 mL)1×10-3 mol/L AgNO3溶液,不能产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
A.0.1 mol·L-1(NH4)2Fe(SO4)2溶液中:c(![]() )>c(
)>c(![]() )>c(Fe2+)>c(H+)
)>c(Fe2+)>c(H+)
B.pH=11的氨水和pH=3的盐酸溶液等体积混合,所得溶液中:c(Cl-)>c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
C.在0.1 mol·L-1 Na2CO3溶液中:2c(Na+)=c(![]() )+c(
)+c(![]() )+c(H2CO3)
)+c(H2CO3)
D.0.1 mol·L-1的醋酸钠溶液20 mL与0.1 mol·L-1盐酸10 mL混合后溶液显酸性:c(CH3COO-)> c(Cl-)> c(CH3COOH)> c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积容器中发生反应:2CH4(g)+2NH3(g)+3O2(g)=2HCN(g)+6H2O(g),15分钟内测得反应速率用HCN表示为v(HCN)=0.36 mol/(L·min),该段时间内下列表示正确的是( )
A.15分钟内反应消耗氨气5.4 mol
B.该时间内可用水表示反应速率为v(H2O)=1.08 mol/(L·min)
C.各物质的速率关系有:2v(CH4)=2v(NH3)=3v(O2)
D.15分钟内氧气浓度下降8.1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,依次进行如下实验:
①取一定量冰醋酸,配制成100mL0.1mol/L醋酸溶液;
②取20mL①中所配溶液,加入20mL0.1mol/LNaOH溶液;
③继续滴加amL0.1mol/L稀盐酸,至溶液的pH=7。
下列说法正确的是
A.①中溶液的pH=1
B.②中反应后溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.③中,a=20
D.③中,反应后溶液:c(Na+)=c(CH3COO-)+c(Cl-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com