
【题目】下列变化需要加入还原剂才能实现的是
A. Cl-→C12 B. HCO3- →C032- C. Mn04- →Mn2+ D. Zn→Zn2+
科目:高中化学 来源: 题型:
【题目】O3是一种常见的绿色氧化剂,可由臭氧发生器(原理如图)电解稀硫酸制得。下列说法错误的是

A. 电极a为阴极
B. a极的电极反应为O2+4H++4e-===2H2O
C. 电解一段时间后b极周围的pH下降
D. 标准状况下,当有5.6LO2反应时,收集到O2和O3混合气体4.48L,O3的体积分数为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛被称为继铁、铝之后的第三金属。工业上常用硫酸酸解钛铁矿(主要成分为FeTiO3,还含有部分Fe2O3)的方法制取金红石(TiO2),再还原TiO2制取金属钛。工业制取TiO2的工艺流程图如下:

回答下列问题:
(1)钛酸亚铁(FeTiO3)中Ti的化合价为________________________。
(2)钛液1中钛以TiO2+的形式存在,则FeTiO3与硫酸反应的离子方程式为________。
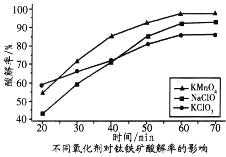
(3)为提高钛铁矿的酸解率,可添加适量氧化剂,依据右图判断,添加的最佳氧化剂为_____________(填化学式)。
(4)钛液1中加入的A物质是____________,流程中的操作a是____________。
(5)制取金红石过程中,需要测定TiO2+的含量。取100mL钛液1,加铝粉,使其发生反应3TiO2++Al+6H+=3Ti3++Al3++3H2O,反应消耗铝1.35g,则钛液1中TiO2+的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列生活中的做法不恰当的是( )
A.贮氯罐意外泄漏,应沿逆风方向疏散群众
B.铝制餐具不宜长期存放酸性、碱性或咸的食物
C.氢氧化铝可作胃酸的中和剂
D.氯气车间液氯泄漏时,应弯腰逃离氯气泄漏区域
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温(500K)、体积为2.0L 的密闭容器中通入1.0 mol N2和1 mol H2发生合成氨反应,20 min 后达到平衡,测得反应放出的热量为 18.4 kJ,混合气体的总物质的量为 1.6 mol。
(1)从开始反应至达到平衡时,用NH3表示该反应的化学反应速率V(NH3)=__________。
(2)该反应的热化学方程式为_____________________________________________。
(3)若拆开1 mol H—H键和1 mol N![]() N 键需要的能量分别是436 kJ和946 kJ,则拆开1 mol N—H键需要的能量是__________kJ。
N 键需要的能量分别是436 kJ和946 kJ,则拆开1 mol N—H键需要的能量是__________kJ。
(4)判断该反应达到平衡状态的依据是____________(填序号)。
①单位时间内消耗1mol N2 的同时消耗了3mol H2 ;
②单位时间内断裂1mol N≡N 的同时断裂了6mol N–H;
③V正(N2)=V逆(NH3);
④NH3的物质的量分数不再随时间而变化
⑤容器内气体的压强不再随时间而变化的状态 ;
⑥容器内气体的密度不再随时间而变化的状态;
⑦c(N2):c(H2):c(NH3)=1:3:2 ;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由两个或两个以上的苯环以共有环边的方式相互稠合的多环芳香烃称为稠环芳香烃。下列椭圆烯也属于稠环芳香烃。
① 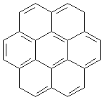 ②
② 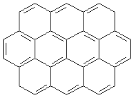
据此回答下列问题:
(1)已知椭圆烯①的分子式为C24 H12,则椭圆烯②的分子式为_________________。
(2)上述椭圆烯的一氯取代物各有几种同分异构体?①有_______种,②有_______种。
(3)假如上述椭圆烯可以和氢气在一定条件下发生加成反应生成饱和脂环烃,则加氢后的生成物分子中所有的碳原子是否仍在同一平面内?____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法的是
A.合金具有优良性能,可用于制造新型金属材料
B.氧化铁俗称铁红,可用作红色油漆和外墙涂料
C.二氧化硫具有漂白性,常用来漂白食品
D.A12O3可用作耐高温材料,A1(OH)3可用于中和过多的胃酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A与B反应生成C,假定反应由A、B开始,它们的初始浓度均为1.0mol·L-1。反应进行2min后A的浓度为0.8 mol·L-1,B的浓度为0.6 mol·L-1,C的浓度为0.6 mol·L-1。
⑴2min内的平均速率为V(A)=_________,V(B)=________,V(C)=________;
⑵V(A):V(B):V(C)=___________________;
⑶该反应的化学方程式为:_______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com