
【题目】(1)熔融盐燃料电池具有高的发电效率,因而受到重视。可用熔融的碳酸盐作为电解质,向负极充入燃料气CH4,用空气与CO2的混合气作为正极的助燃气,以石墨为电极材料,制得燃料电池。工作过程中,CO32-移向__极(填“正”或“负”),负极的电极反应式为__,正极的电极反应式为___。
(2)某实验小组同学对电化学原理进行了一系列探究活动。
①如图为某实验小组依据的氧化还原反应:__(用离子方程式表示)设计的原电池装置。
②其他条件不变,若将CuCl2溶液换为HCl溶液,石墨的电极反应式为___。

(3)如图为相互串联的甲、乙两电解池,其中甲池为电解精炼铜的装置。试回答下列问题:

①A极材料是___,电极反应为___,B极材料是__,主要电极反应为__,电解质溶液为___。
②乙池中若滴入少量酚酞溶液,电解一段时间后Fe极附近溶液呈___色。
③常温下,若甲池中阴极增重12.8g,则乙池中阳极放出的气体在标准状况下的体积为___,若此时乙池剩余液体为400mL,则电解后溶液pH为___。
【答案】负 CH4+4CO32--8e-=5CO2+2H2O 2O2+8e-+4CO2=4CO32- Fe+Cu2+=Fe2++Cu 2H++2e-=H2↑ 纯铜 Cu2++2e-=Cu 粗铜 Cu-2e-=Cu2+ CuSO4溶液 红 4.48L 14
【解析】
(1)原电池放电时,阳离子移向正极、阴离子移向负极;以熔融盐为电解质的甲烷燃料电池放电时,甲烷在负极失电子生成二氧化碳和水;氧气在正极得电子生成碳酸根离子。
(2)①根据电池总反应回答;
②铁与盐酸反应放出氢气;
(3)①电解法精炼铜,粗铜作阳极、精铜作阴极,硫酸铜作电解质溶液;
②乙池中Fe作阴极,阴极氢离子得电子生成氢气;
③常温下,甲池中阴极增重12.8g,即生成铜的质量是12.8g,根据电子守恒计算。
(1)原电池放电时,阴离子移向负极,所以CO32-移向负极;以熔融盐为电解质的甲烷燃料电池放电时,甲烷在负极失电子生成二氧化碳和水,负极反应式是CH4+4CO32--8e-=5CO2+2H2O;氧气在正极得电子生成碳酸根离子,正极反应式是2O2+8e-+4CO2=4CO32-。
(2)①根据图示,铁是负极,电池总反应是Fe+Cu2+=Fe2++Cu,所以依据氧化还原反应Fe+Cu2+=Fe2++Cu设计的原电池装置;
②铁与盐酸反应放出氢气,所以正极放出氢气,石墨的电极反应式为2H++2e-=H2↑;
(3)①电解法精炼铜,A极是阴极,电极材料是纯铜,电极反应为Cu2++2e-=Cu,B是阳极,阳极材料是粗铜,主要电极反应为Cu-2e-=Cu2+,电解质溶液为CuSO4溶液。
②乙池中Fe作阴极,阴极氢离子得电子生成氢气,电极反应式是2H2O+2e-= H2↑+2OH-,溶液显碱性,Fe极附近溶液呈红色;
③常温下,甲池中阴极增重12.8g,即生成铜的质量是12.8g,电路中转移电子的物质的量是![]() 0.4mol,乙池中阳极放出的气体是氯气,根据电子守恒,生成氯气的物质的量是0.2mol,在标准状况下的体积是0.2mol×22.4L/mol=4.48L;根据2H2O+2e-= H2↑+2OH-,生成氢氧根离子的物质的量是0.4mol,氢氧根离子的浓度是
0.4mol,乙池中阳极放出的气体是氯气,根据电子守恒,生成氯气的物质的量是0.2mol,在标准状况下的体积是0.2mol×22.4L/mol=4.48L;根据2H2O+2e-= H2↑+2OH-,生成氢氧根离子的物质的量是0.4mol,氢氧根离子的浓度是![]() 1mol/L,所以pH=14。
1mol/L,所以pH=14。


科目:高中化学 来源: 题型:
【题目】Mg﹣H2O2电池可用于无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如图。下列说法正确的是( )
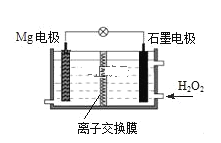
A.Mg电极是该电池的正极
B.溶液中Cl﹣向正极移动
C.该电池的总反应为:Mg+H2O2═Mg(OH)2
D.H2O2在石墨电极上发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶状液氢(主要成分是H2和CH4)有望运用于未来的运载火箭和空间运输系统。实验测得101kPa时,1molH2完全燃烧生成液态水,放出285.8kJ的热量;1molCH4完全燃烧生成液态水和CO2,放出890.3kJ的热量。下列热化学方程式书写正确的是( )
A.2H2(g)+O2(g)=2H2O(l) ΔH=+285.8kJmol-1
B.2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJmol-1
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3kJmol-1
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美托洛尔可用于治疗高血压及心绞痛,某合成路线如下:
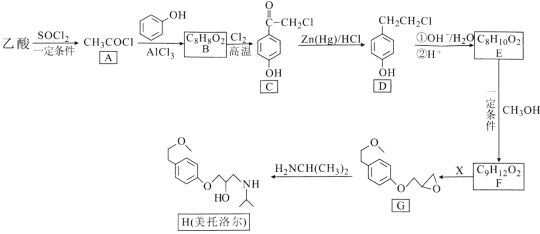
回答下列问题:
(1)美托洛尔分子中含氧官能团的名称是_____。
(2)A→B的反应类型是____,G的分子式为____。
(3)反应E→F的化学方程式为_______。
(4)试剂X的分子式为C3H5OCl,则X的结构简式为____。
(5)B的同分异构体中,含有苯环且能发生水解反应的共有____种,其中苯环上只有一个取代基且能发生银镜反应的结构简式为_____。
(6)4-苄基苯酚(![]() )是一种药物中间体,请设计以苯甲酸和苯酚为原料制备4-苄基苯酚的合成路线:__________(无机试剂任用)。
)是一种药物中间体,请设计以苯甲酸和苯酚为原料制备4-苄基苯酚的合成路线:__________(无机试剂任用)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫、氮的氧化物是形成酸雨的主要原因,一种比较常用的方法是用NH3处理氮的氧化物(NxOy)。完成下列问题。
(1)已知:①2NO(g)=N2(g)+O2(g) △H=-177kJ/mol
②4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=-1253.4kJ/mol
则用NH3处理NO生成氮气和气态水的热化学方程式为__。
(2)已知:N2(g)+3H2(g)![]() 2NH3(g) △H<0。不同温度下,向三个一样的容器中投入相同的反应物进行反应,测得不同压强下平衡混合物中NH3的物质的量分数如图所示。
2NH3(g) △H<0。不同温度下,向三个一样的容器中投入相同的反应物进行反应,测得不同压强下平衡混合物中NH3的物质的量分数如图所示。

①M点的v正__Q点的v正(填“>”“<”或“=”),原因是__。
②维持10MPa、T3℃的条件不变,要提高H2的转化率,可以采取的措施是__(任写一条)。
③图中三条曲线对应的温度T1、T2、T3由高到低的顺序为___。
④恒温恒容条件下,能说明反应N2(g)+3H2(g)![]() 2NH3(g)达到平衡状态的是__(填选项字母)
2NH3(g)达到平衡状态的是__(填选项字母)
A.![]() 保持不变
保持不变
B.3molH-H键断裂的同时,有2molN-H键断裂
C.2v(N2)=v(NH3)
D.反应器中的压强不再发生变化
⑤T3温度下,将1molN2和3molH2充入2L的恒容密闭容器中反应,一段时间后达到N点的平衡状态,则反应的平衡常数为K=__(结果保留2位小数),M点与Q点对应的平衡常数大小关系为M__Q(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我省近年来以铁矿石为原料的产业发展迅猛,下列有关说法正确的是
A.以焦炭和铁矿石为原料炼铁的原理是用焦炭直接还原化合态的铁
B.据报道,庐江磁性材料产生“磁”力无穷,磁性氧化铁的化学式是![]()
C.为证明某铁矿石中存在铁离子,可将铁矿石溶于硝酸后,再加KSCN溶液
D.利用铁矿石制得的能除去污水中的![]() ,可知相同条件下,
,可知相同条件下,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将物质的量相等的硫酸铝和硫酸铵溶于水形成VmL混合溶液,向混合溶液中逐滴加入某氢氧化钠溶液(其物质的量浓度为混合溶液中两溶质的物质的量浓度之和),直至过量.下列表示氢氧化钠溶液加入的体积(x)与溶液中沉淀物的量(y)的关系示意图中正确的是( )
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、下图是用0.1000mol/L的盐酸滴定某未知浓度的NaOH溶液的示意图和某次滴定前后盛放盐酸的滴定管中液面的位置。

实验编号 | 待测NaOH溶液的体积(mL) | 滴定前盐酸的读数(mL) | 滴定后盐酸的读数(mL) |
1 | 20.00 | 1.20 | 23.22 |
2 | 20.00 | 1.21 | 29.21 |
3 | 20.00 | 1.50 | 23.48 |
请回答下列问题:
(1)仪器A的名称是_________________。
(2)盐酸的体积读数:滴定前读数为___________,滴定后读数为_____________。
(3)某实验小组同学的三次实验的实验数据如上表所示。根据表中数据计算出待测NaOH溶液的平均溶度是____________mol/L(保留四位有效数字)。
(4)对下列几种假定情况进行讨论:
①取待测溶液的滴定管,放液前滴定管尖端有气泡,放液后气泡消失,对测定结果的影响是____________(填“无影响”“偏高”或“偏低”,下同)
②滴定前锥形瓶未用待测液润洗,对测定结果的影响是_______________;
Ⅱ、氧化还原滴定实验与酸碱中和滴定类似,原理是用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之。现用0.001mol/L酸性KMnO4溶液滴定位置浓度的Na2SO3溶液,反应的离子方程式是2MnO4- + 5SO32- + 6H+=2Mn2+ + 5SO42- + 3H2O。请回答下列问题:
(1)该滴定实验所需仪器有________________。
A、酸式滴定管(50mL) B、碱式滴定管(50mL) C、量筒(10mL) D、锥形瓶 E、铁架台F、滴定管夹 G、烧杯 H、胶头滴管 I、漏斗
(2)实验时,应用_____________(填“酸式”或“碱式”,下同)滴定管盛放高锰酸钾溶液,应用__________滴定管盛放亚硫酸钠溶液。
(3)该实验_____________(填“需要”或“不需要”)加入指示剂,原因是_____________。滴定达到终点的标志是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.按系统命名法,有机物![]() 可命名为3,7-二甲基-4-乙基辛烷
可命名为3,7-二甲基-4-乙基辛烷
B.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等
C.苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色
D.结构片段为![]() 的高聚物,其单体是甲醛和苯酚
的高聚物,其单体是甲醛和苯酚
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com