
【题目】从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。以下是氯元素形成物质的二维图的部分信息。
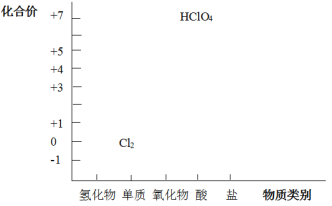
(1)根据图中信息,写出任意一种氯的氧化物的化学式_____。
(2)HCl既具有氧化性,又具有还原性。
①请任意写出一个体现HCl氧化性的化学方程式_____________。
②浓HCl可作为还原剂在加热条件下与MnO2发生反应制备Cl2,写出该反应的化学方程式_________。
【答案】Cl2O或Cl2O3或Cl2O5或Cl2O7 Zn+2HCl =ZnCl2+ H2 ↑ MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
【解析】
⑴根据图中信息,氯的价态有+1,+3,+5,+7,任意一种氯的氧化物的化学式Cl2O或Cl2O3或Cl2O5或Cl2O7。
⑵①化合价降低,表现氧化性,因此体现HCl氧化性的化学方程式是Zn+2HCl =ZnCl2+ H2 ↑等。
②浓HCl可作为还原剂在加热条件下与MnO2发生反应制备Cl2,该反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
⑴根据图中信息,氯的价态有+1,+3,+5,+7,任意一种氯的氧化物的化学式Cl2O或Cl2O3或Cl2O5或Cl2O7,故答案为:Cl2O或Cl2O3或Cl2O5或Cl2O7。
⑵①化合价降低,表现氧化性,因此体现HCl氧化性的化学方程式是Zn+2HCl =ZnCl2+ H2 ↑等,故答案为:Zn+2HCl =ZnCl2+ H2 ↑。
②浓HCl可作为还原剂在加热条件下与MnO2发生反应制备Cl2,该反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】某学校化学学习小组为探究二氧化氮的性质,按如图所示装置进行实验。
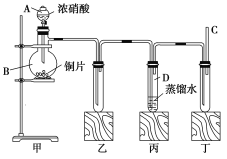
回答下列问题:
(1)装置甲中盛放浓硝酸的仪器A的名称是_____,该装置中发生反应的化学方程式为___。
(2)实验过程中,装置乙、丙中出现的现象分别是__________、____________;装置丙中的试管内发生反应的离子方程式为________________(不是离子反应的不写)。
(3)取下装置丙中的试管D,在其中滴加FeSO4溶液,溶液变为________色,为了证明铁元素在该反应中的产物,可以再向溶液中滴加KSCN溶液,溶液变为________色。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行下列实验:将①中的浓硫酸滴入②中,预测的现象与结论相符的是( )

A. 若②为浓盐酸;产生大量气体产生;说明硫酸的酸性比盐酸强
B. 若②为铜片;有气泡产生,底部生成灰白色固体;说明浓硫酸有强氧化性
C. 若②为蓝色硫酸铜晶体;蓝色晶体变为白色;说明浓硫酸有吸水性,发生物理变化
D. 若②为蔗糖;白色固体变为黑色海绵状,有气体放出;说明浓硫酸有脱水性、氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某澄清溶液可能含有Na+、NH4+、Fe2+、K+、I-、CO32-、SO42-中的若干种离子,分别取2份该溶液于试管进行如下实验:
①向一份溶液中滴加溴水,溶液显浅黄色。
②向另一份溶液中滴加少量![]() 溶液,加热,将湿润的红色石蕊试纸置于试管口。溶液中产生白色沉淀并立即变灰绿色,试管口的石蕊试纸不变色。
溶液,加热,将湿润的红色石蕊试纸置于试管口。溶液中产生白色沉淀并立即变灰绿色,试管口的石蕊试纸不变色。
下列说法正确的是
A.原溶液中一定有Fe2+、I-
B.原溶液中无法确定的有SO42-、Na+、K+、I-
C.原溶液中一定没有CO32-、NH4+、SO42-
D.用铂丝蘸取原溶液在酒精灯火焰上灼烧,可直接观察火焰颜色确定溶液是否存在Na+、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,在一定的条件下,它们之间具有如下转化关系:![]() 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是
A.若甲为焦炭,则丁可能是O2B.若甲为Fe,则丁可能是氯气
C.若甲为Fe,则丁可能是硝酸D.若甲为NaOH 溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列问题:
(1)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,试回答:该元素核外价电子排布图___,电子排布式_____。
(2)指出配合物K3[Co(CN)6]中的中心离子、配位体及其配位数:____、____、____。
(3)下列分子中若有手性原子,请用“*”标出其手性碳原子。____
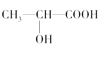
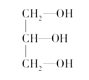
(4)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填序号)____。
(5)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4____H2SO3;HClO3____HClO4;H3PO4___H3PO3。
(6)根据价层电子对互斥理论判断下列问题:
NH3中心原子的杂化方式为___杂化,VSEPR构型为__,分子的立体构型为____。
(7)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种微生物燃料电池的结构示意图如下所示,关于该电池的叙述正确的是( )
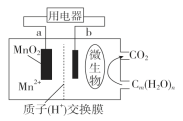
A. 电池工作时,电子由a流向b
B. 微生物所在电极区放电时发生还原反应
C. 放电过程中,H+从正极区移向负极区
D. 正极反应式为:MnO2+4H++2e-===Mn2++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸(无水醋酸)中的电离常数:从下表格中判断下列说法不正确的是( )
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
A.在无水醋酸中1mol/L的高氯酸的电离度约为0.4%
B.在无水醋酸中硝酸是这四种酸中最弱的酸
C.在无水醋酸中,硫酸可以和高氯酸钠反应制备出高氯酸
D.水对于这四种酸的强弱没有区分能力,但醋酸可以区分这四种酸的强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应![]() 在容积为10L的密闭容器中进行。起始时
在容积为10L的密闭容器中进行。起始时![]() 和
和![]() 均为0.20mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。下列说法不正确的是( )
均为0.20mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。下列说法不正确的是( )

A. 实验c条件下,从反应开始至达到平衡时![]()
B. 实验a条件下,用浓度表示的平衡常数为100
C. 该反应的![]()
D. 比较实验a、c可判断升高温度反应速率加快
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com