
【题目】氨对人类的生产生活具有重要影响。
(1)氨的制备与利用。
① 工业合成氨的化学方程式是_______________________________。
② 氨催化氧化生成一氧化氮反应的化学方程式是_____________________________。
(2)氨的定量检测。
水体中氨气和铵根离子(统称氨氮)总量的检测备受关注。利用氨气传感器检测水体中氨氮含量的示意图如下:

① 利用平衡原理分析含氨氮水样中加入NaOH溶液的作用:_____________________。
② 若利用氨气传感器将1 L水样中的氨氮完全转化为N2时,转移电子的物质的量为6×10-4 mol ,则水样中氨氮(以氨气计)含量为_______mg·L-1。
(3)氨的转化与去除。
微生物燃料电池(MFC)是一种现代化氨氮去除技术。下图为MFC碳氮联合同时去除的氮转化系统原理示意图。
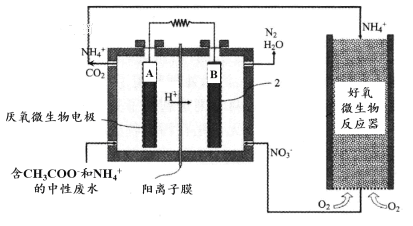
① 已知A、B两极生成CO2和N2,写出A极的电极反应式:______________________。
② 用化学用语简述NH4+去除的原理:_________________________________________。
【答案】N2+ 3H2![]() 2NH3 4NH3 + 5O2
2NH3 4NH3 + 5O2![]() 4NO + 6H2O c(OH-)增大,使NH4++ OH-
4NO + 6H2O c(OH-)增大,使NH4++ OH-![]() NH3·H2O
NH3·H2O![]() NH3+ H2O平衡正向移动,利于生成氨气,被空气吹出 3.4 CH3COO-- 8e-+ 2H2O =2CO2+ 7H+ NH4+在好氧微生物反应器中转化为NO3-:NH4++ 2O2= NO3- + 2H++ H2O;
NH3+ H2O平衡正向移动,利于生成氨气,被空气吹出 3.4 CH3COO-- 8e-+ 2H2O =2CO2+ 7H+ NH4+在好氧微生物反应器中转化为NO3-:NH4++ 2O2= NO3- + 2H++ H2O;
NO3-在MFC电池正极转化为N2:2NO3- +12H++ 10e- =N2 + 6H2O
【解析】
(1)①工业合成氨是利用氮气和氢气催化剂作用下高温高压反应生成氨气,反应的化学方程式为:N2+3H2![]() 2NH3;
2NH3;
②氨气的催化氧化生成一氧化氮和水,反应的化学方程式为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(2)①利用平衡原理分析含氨氮水样中加入NaOH溶液的作用是c(OH-)增大,使NH4++OH-NH3H2ONH3+H2O平衡正向移动,利于生成氨气,被空气吹出;
②将1L水样中的氨氮完全转化为N2时,转移电子的物质的量为6×10-4mol,依据氮元素守恒2NH3~N2~6e-,
2NH3~N2~6e-,
2 6
n 6×10-4mol/L
n=2×10-4mol/L;水样中氨氮(以氨气计)含量=2×10-4mol/L×17g/mol=3.4×10-3g/L=3.4mg/L;
(3)①图示分析可知微生物燃料电池中氢离子移向B电极,说明A为原电池的负极,B为原电池的正极,NO3-离子在正极得到电子生成氮气发生还原反应,CH3COO-在原电池负极失电子生成二氧化碳气体,发生氧化反应,环境为酸性介质,则A极的电极反应式为:CH3COO--8e-+2H2O═2CO2+7H+,B电极反应式为:2NO3-+12H++10e-═N2+6H2O;
②NH4+在好氧微生物反应器中转化为NO3-,NH4++2O2═NO3-+2H++H2O,硝酸根离子在原电池正极发生还原反应生成氮气,2NO3-+12H++10e-═N2+6H2O。


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】在一体积为2L的密闭容器中充入2mol X,一定条件下可发生反应:2X(g)![]() 3Y(g),该反应的反应速率(v)与时间(t)的关系如图所示,已知
3Y(g),该反应的反应速率(v)与时间(t)的关系如图所示,已知![]() min时容器内有1.5mol Y。下列叙述正确的是( )
min时容器内有1.5mol Y。下列叙述正确的是( )

A. 若![]() min时升高温度,则反应速率不变
min时升高温度,则反应速率不变
B. ![]() ~
~![]() min内,
min内,![]() ,反应不再发生
,反应不再发生
C. 0~![]() min内,
min内,![]()
D. ![]() min时,只有正反应发生
min时,只有正反应发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下联氨![]() 的水溶液中有:
的水溶液中有:
![]()
![]()
![]()
![]() 提示:二元弱碱的电离也是分步电离
提示:二元弱碱的电离也是分步电离![]()
该溶液中的微粒的物质的量分数![]() 随
随![]() 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是![]()
![]()
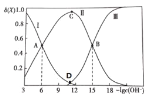
A.据A点可求:![]()
B.D点溶液的 ![]()
C.若C点为![]() 溶液,则存在:
溶液,则存在:![]()
D.在![]() 水溶液中,
水溶液中,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,原理如图所示。下列说法正确的是
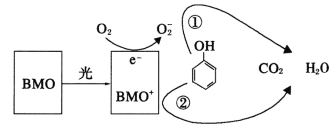
A.该过程的总反应:C6H6O+7O2![]() 6CO2+3H2O
6CO2+3H2O
B.该过程中BMO表现出较强氧化性
C.光催化降解过程中,光能转化为化学能、热能等
D.①和②中被降解的苯酚的物质的量之比为1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列叙述中不正确的是( )
A.16g氧气中含有的氧原子数目为NA
B.1L0.1mol·L-1Na2CO3溶液中含有的阴离子数目大于0.1NA
C.标准状况下,22.4LCl2中含有的电子数为34NA
D.标准状况下,22.4L乙醇中含有的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在密闭容器中发生可逆反应的平衡常数K=![]() 。当反应达到平衡时,n(A)∶n(B)∶n(C)=2∶2∶1。若保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则
。当反应达到平衡时,n(A)∶n(B)∶n(C)=2∶2∶1。若保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则
A.K值增大B.达到新平衡后,C的体积分数增大
C.平衡不移动D.达到新平衡后,vA比原平衡减慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体离子导体依靠离子迁移传导电流。如图是一种固体电池,Ag+可以在RbAg4I5晶体中迁移,空气中的O2透过聚四氟乙烯膜与AlI3反应生成I2,Ag和I2作用形成原电池。下列说法错误的是( )
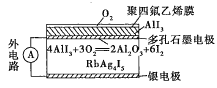
A.I2与Ag反应属于放热反应
B.Ag+从多孔石墨电极向银电极移动
C.多孔石墨电极为正极,银电极为负极
D.银电极的电极反应式为Ag-e-=Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法错误的是
A. 3g 3He含有的中子数为1NA
B. 1 L 0.1 mol·L1磷酸钠溶液含有的![]() 数目为0.1NA
数目为0.1NA
C. 1 mol K2Cr2O7被还原为Cr3+转移的电子数为6NA
D. 48 g正丁烷和10 g异丁烷的混合物中共价键数目为13NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各实验装置的叙述中,正确的是![]()
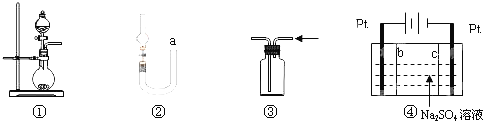
A.图![]() 可用于制取少量
可用于制取少量![]() 或用
或用![]() 和浓盐酸制取
和浓盐酸制取![]()
B.可用从a处加水的方法检验图![]() 装置的气密性
装置的气密性
C.实验室可用图![]() 的方法收集
的方法收集![]() 或
或![]()
D.利用图![]() 装置制硫酸和氢氧化钠,其中c为阴离子交换膜、b为阳离子交换膜
装置制硫酸和氢氧化钠,其中c为阴离子交换膜、b为阳离子交换膜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com