
| A、①② | B、①③ | C、②③ | D、③④ |
科目:高中化学 来源: 题型:
| A、加热后的蒸发皿,要用坩埚钳夹取 | ||
| B、试管和烧杯都可以直接在火焰上加热 | ||
C、给试管里的液体加热,液体的体积一般不超过试管容积的
| ||
| D、用剩的药品不要乱丢,要放回原试剂瓶里 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、Fe2+、ClO-、SO42- |
| B、Na+、Cu2+、S2-、ClO- |
| C、Na+、Ba2+、OH-、NO3- |
| D、Na+、Al3+、SiO32-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Al3+、HCO3-、SO42- |
| B、Ca2+、NH4+、CO32-、Cl- |
| C、Na+、K+、NO3-、ClO- |
| D、Na+、Fe2+、I-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
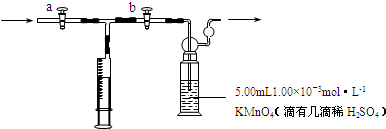
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com