
【题目】有一种细菌在酸性水溶液中,有氧气的情况下,可以将黄铜矿(主要成分是CuFe![]() ,含少量杂质SiO2)氧化为硫酸盐。运用该原理生产铜和绿矾(FeSO4·7H2O)的流程如下:
,含少量杂质SiO2)氧化为硫酸盐。运用该原理生产铜和绿矾(FeSO4·7H2O)的流程如下:
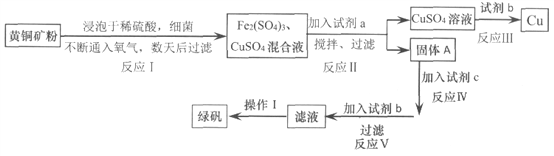
已知:
Fe2+ | Cu2+ | Fe3+ | |
开始转化成氢氧化物沉淀时的pH | 7.6 | 4.7 | 2.7 |
完全转化成氢氧化物沉淀时的pH | 9.6 | 6.7 | 3.7 |
回答下列问题:
(1)试剂a是_________,调节溶液的pH值,为使Fe3+完全沉淀,合适pH的范围是_______。
(2)试剂b为________,请写出反应III的离子方程式________________。
(3)固体A成份是________。
(4)欲从滤液中获得绿矾晶体,操作I应为________________、洗涤干燥。
(5)反应I中参加反应的n(CuFeS2):n(O2)=________________。
【答案】 CuO或Cu(OH)2 3.7~4.7 铁粉 Fe+Cu2+=Cu+Fe2+ Fe(OH)3 加热浓缩,降温结晶,过滤 4:17 或1:17/4或4.25
【解析】(1)为了调节溶液PH值,用CuO或Cu(OH)2在不引入新杂质的情况下消耗酸溶时的酸,使溶液中的铁转化为氢氧化铁而与硫酸铜溶液分离,为使Fe3+完全沉淀,合适pH的范围是3.7~4.7;(2)试剂b从硫酸铜溶液中置换出铜,则试剂b应该为铁粉,反应产生的硫酸亚铁可并入滤液用于制备绿矾,反应III的离子方程式为:Fe+Cu2+=Cu+Fe2+;(3)从工艺流程图可知,Fe3+在溶液中存在水解平衡,即Fe3++ 3H2O![]() Fe(OH)3+3H+,在PH达3.7时,Fe3+沉淀完全,当加入氧化铜后,氧化铜能与H+反应,促进水解平衡右移,使Fe3+转化为Fe(OH)3被除去,而氧化铜不被损耗,且不会引入新杂质,固体A为氢氧化铁;(4)欲从滤液中获得绿矾晶体,操作I应为加热浓缩,降温结晶,过滤、洗涤干燥;(5)反应Ⅰ中的反应物是CuFeS2、O2、H2SO4三种物质,生成物是硫酸铁、硫酸铜和水,根据奇偶法配平,所以方程式是:4CuFeS2+17O2+2H2SO4═2Fe2(SO4)3+4CuSO4+2H2O;根据反应可知,参加反应的n(CuFeS2):n(O2)=4:17=1:
Fe(OH)3+3H+,在PH达3.7时,Fe3+沉淀完全,当加入氧化铜后,氧化铜能与H+反应,促进水解平衡右移,使Fe3+转化为Fe(OH)3被除去,而氧化铜不被损耗,且不会引入新杂质,固体A为氢氧化铁;(4)欲从滤液中获得绿矾晶体,操作I应为加热浓缩,降温结晶,过滤、洗涤干燥;(5)反应Ⅰ中的反应物是CuFeS2、O2、H2SO4三种物质,生成物是硫酸铁、硫酸铜和水,根据奇偶法配平,所以方程式是:4CuFeS2+17O2+2H2SO4═2Fe2(SO4)3+4CuSO4+2H2O;根据反应可知,参加反应的n(CuFeS2):n(O2)=4:17=1: ![]() =4.25。
=4.25。


科目:高中化学 来源: 题型:
【题目】分类是化学学习中经常用到的方法,下列对一些物质或化学反应的分类以及依据正确的是( )
A. H2SO4是酸,因为H2SO4中含有氢元素
B. 豆浆是胶体,因为豆浆中的分散质粒子直径在1nm~100nm之间
C. Na和H2O的反应不是离子反应,因为反应中没有离子参加
D. 燃烧必须有氧气参与,因而没有氧气参与的反应一定没有燃烧现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同温度下,向2 L密闭容器中加入1 mol NO和1 mol活性炭,发生反应:2NO(g)+C(s)![]() N2(g)+CO2(g)△H=-213.5 kJ/mol,达到平衡时的数据如下:
N2(g)+CO2(g)△H=-213.5 kJ/mol,达到平衡时的数据如下:
温度/℃ | n(活性炭)/mol | n(CO2)/mol |
T1 | 0.70 | |
T2 | 0.25 |
下列说法不正确的是
A. 上述信息可推知:T1<T2
B. T1℃时,该反应的平衡常数K=9/16
C. T2℃时,若反应达平衡后再缩小容器的体积,c(N2):c(NO)不变
D. T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子液体在有机合成、无机合成等方面有着重要应用。咪唑是合成“离子液体”的一种原料,其结构如图所示。下列有关咪唑说法不正确的是
![]()
A. 化学式C3H4N2
B. 分子中含有一种非极性键和两种极性键
C. 可以发生取代、加成、氧化反应
D. 一氯取代物的同分异构体共有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨反应过程中的能量变化如图所示,下列说法错误的是( )

A. 反应体系中加入催化剂,不会改变反应的热效应
B. 反应物的总能量高于生成物的总能量
C. 该反应的热化学方程式为3H2+N2![]() 2NH3 ΔH=Q(Q>0)
2NH3 ΔH=Q(Q>0)
D. 该反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。

下列分析不正确的是( )
A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH-
C.c点,两溶液中含有相同量的OH-
D.a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学利用原电池装置探究物质的性质。
资料显示:原电池装置中,负极反应物的还原性越强,或正极反应物的氧化性越强,原电池的电压越大。 |
(1)同学们利用下表中装置进行实验并记录。
装置 | 编号 | 电极A | 溶液B | 操作及现象 |
| Ⅰ | Fe | pH=2的 H2SO4 | 连接装置后,石墨表面产生无色气泡;电压表指针偏转 |
Ⅱ | Cu | pH=2的H2SO4 | 连接装置后,石墨表面无明显现象;电压表指针偏转,记录读数为a |
①同学们认为实验Ⅰ中铁主要发生了析氢腐蚀,其正极反应式是_________。
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其判断依据是_________;乙同学认为实验Ⅱ中应发生吸氧腐蚀,其正极的电极反应式是_________。
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性的因素。
编号 | 溶液B | 操作及现象 |
Ⅲ | 经煮沸的pH=2的 H2SO4 | 溶液表面用煤油覆盖,连接装置后,电压表指针微微偏转,记录读数为b |
Ⅳ | pH=2的H2SO4 | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为c;取出电极,向溶液中加入数滴浓Na2SO4溶液混合后,插入电极,保持O2通入,电压表读数仍为c |
Ⅴ | pH=12的NaOH | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为d |
①丙同学比较实验Ⅱ、Ⅲ、Ⅳ的电压表读数为:c>a>b,请解释原因是_________。
②丁同学对Ⅳ、Ⅴ进行比较,其目的是探究对O2氧化性的_________影响。
③实验Ⅳ中加入Na2SO4溶液的目的是_________。
④为达到丁同学的目的,经讨论,同学们认为应改用右图装置对Ⅳ、Ⅴ重复进行实验,其设计意图是_________;重复实验时,记录电压表读数依次为c′、d′,且c′>d′,由此得出的结论是_________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系互为同分异构体的是( )
A.35C1和37ClB.CH3CH2CH2 CH3和CH(CH3)3
C.CH3CH3和CH3CH2CH3D.H2O和H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯是工业上常用的化工原料,可以用于合成安息香酸苄酯和高分子化合物G (部分反应条件略去),流程如下所示,请回答下列问题:
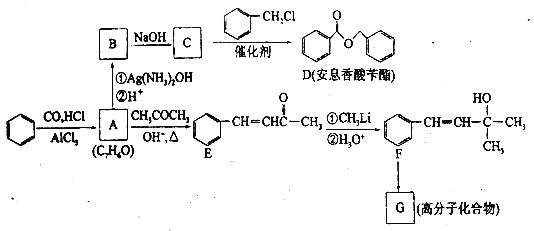
(1)A的化学名称是________,B中的官能团名称是________。
(2)E分子中最多可能有_____个碳原子共平面;G的结构简式为_________;
(3)C生成D的反应类型为___________。
(4)A生成E的化学方程式为_________________。
(5)H是D的同分异构体,分子中含有酯基,有两个苯环且不直接相连,符合上述条件的结构有_______种,其中核磁共振氢谱有6组峰,且面积比为3:2:2:2:2:1的同分异构体的结构简式为_______(写出一种即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com