
����Ŀ�����Ļ������������������й㷺���ڡ�
��1�������ǽ�1mol�����������AB��Ϊ������̬ԭ��A��B�������������֪���л�ѧ���ļ������±���
![]()
д��1mol��̬��(H2N-NH2)ȼ�����ɵ�����ˮ�������Ȼ�ѧ����ʽ________________��
��2���ý�̿��ԭNO�ķ�ӦΪ��2NO(g)+C(s)![]() N2(g)+CO2(g)�����ݻ���Ϊ1L�ļס��ҡ����������ݺ���(��Ӧ�¶ȷֱ�Ϊ400�桢400�桢T��)�����зֱ���������Ľ�̿��һ������NO����ø�������n(NO)�淴Ӧʱ��t�ı仯������±���ʾ��
N2(g)+CO2(g)�����ݻ���Ϊ1L�ļס��ҡ����������ݺ���(��Ӧ�¶ȷֱ�Ϊ400�桢400�桢T��)�����зֱ���������Ľ�̿��һ������NO����ø�������n(NO)�淴Ӧʱ��t�ı仯������±���ʾ��
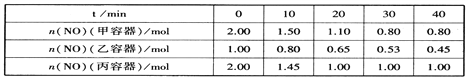
�ٸ÷�ӦΪ________(��������������������)��Ӧ��
����������60minʱ�ﵽƽ��״̬����0��60min����NO��Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(NO)=____________��
��3���ý�̿��ԭNO2�ķ�ӦΪ��2NO2(g)+2C(s) ![]() N2(g)+2CO2(g)���ں��������£�1molNO2������C�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
N2(g)+2CO2(g)���ں��������£�1molNO2������C�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
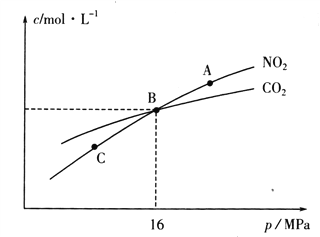
��A��C�����Ũ��ƽ�ⳣ����ϵ��Kc(A)________Kc(C)(����<������>������=��)��
��A��B��C������NO2��ת������ߵ���________(����A������B������C��)�㡣
�ۼ���B��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��Kp(B)=________(Kp����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
���𰸡�![]() ���� 0.01mol/(L��min) �� C 3.2MPa
���� 0.01mol/(L��min) �� C 3.2MPa
��������
������1�������ʱ�=��Ӧ���ܼ��ܣ��������ܼ��ܼ���1mol��̬��(H2N-NH2)ȼ�����ɵ�����ˮ�������ʱ�����2�����Ƚϼס�����ͼ�����ݣ����ķ�Ӧ���ʴ��ڼף���֪�����¶ȴ���400�� ��ƽ��ʱ����NOŨ�ȴ��ڼף����������¶�ƽ�������ƶ���������![]() ���㷴Ӧ���ʣ���3����A��C�����¶���ͬ������ƽ�ⳣ����ȣ�������ѹǿƽ�������ƶ���������ƽ�ⳣ������ʽ����B��ʱ�÷�Ӧ��ѹǿƽ�ⳣ����
���㷴Ӧ���ʣ���3����A��C�����¶���ͬ������ƽ�ⳣ����ȣ�������ѹǿƽ�������ƶ���������ƽ�ⳣ������ʽ����B��ʱ�÷�Ӧ��ѹǿƽ�ⳣ����
��������1�������ʱ�=��Ӧ���ܼ��ܣ��������ܼ����� 1mol��̬��(H2N-NH2)ȼ�����ɵ�����ˮ�������ʱ�=193KJ/mol��391 KJ/mol��4��497 KJ/mol��946 KJ/mol��463 KJ/mol��4=��544 KJ/mol������1mol��̬��(H2N-NH2)ȼ�����ɵ�����ˮ�������Ȼ�ѧ����ʽ��![]() ��
��
��2�����Ƚϼס�����ͼ�����ݣ����ķ�Ӧ���ʴ��ڼף���֪�����¶ȴ���400�� ��ƽ��ʱ����NOŨ�ȴ��ڼף����������¶�ƽ�������ƶ�����������Ӧ������
��
��ƽ�ⳣ��=![]() �������¶���ͬ������ƽ�ⳣ����ͬ������װ��NO��Ũ�ȱ仯��Ϊxmol/L��
�������¶���ͬ������ƽ�ⳣ����ͬ������װ��NO��Ũ�ȱ仯��Ϊxmol/L��
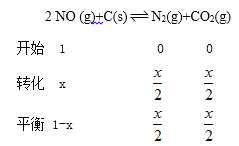
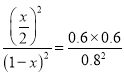 ��x=0.6������
��x=0.6������![]() ��v(NO)=
��v(NO)=![]() 0.01mol/(L��min)��
0.01mol/(L��min)��
��3����A��C�����¶���ͬ������ƽ�ⳣ���������Kc(A)=Kc(C)��������ѹǿƽ�������ƶ���NO2��ת������ߵ���C�������ݷ���ʽ��N2(g)��ƽ��Ũ����CO2Ũ�ȵ�![]() ������B��ʱ��NO2��N2��CO2���ʵ��������ֱ���
������B��ʱ��NO2��N2��CO2���ʵ��������ֱ���![]() ��
��![]() ��
��![]() �� B��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��=
�� B��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��=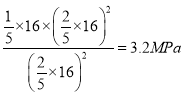 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʾ�����Ҵ�����ͨ����ɫ��ĩ(CrO3)����ɫ��ĩ�����ɫ��ĩ(Cr2O3)��������ȩ������ȩ�ܻ�ԭ���Ը��������Һ��ijС���������װ���Ʊ�������ȩ������˵��������ǣ� ��
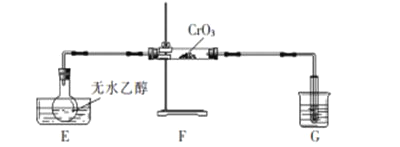
A.ˮ��E��װ��ˮ���ձ�G��װ��ˮ
B.������ȩ�ķ�������Ӧ�����Һ�еμ����Ը��������Һ
C.E������һ֧�¶ȼƣ�����������Ҵ���������
D.����������������롢�����ֲ�Ʒ�е���ȩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������У�ʼ��������������ǣ� ��
A.NO2ͨ��FeSO4��Һ��
B.SO2ͨ�����ữ��Ba(NO3)2��Һ��
C.NH3ͨ��AlCl3��Һ��
D.CO2ͨ��CaCl2��Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ҩ��H(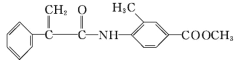 )��һ�ֿ���������������ҩ���ϳ�·����ͼ��ʾ��
)��һ�ֿ���������������ҩ���ϳ�·����ͼ��ʾ��
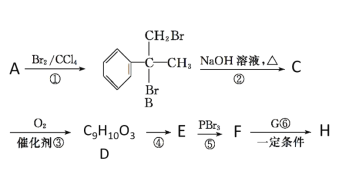
��֪����E�ķ���ʽΪC9H8O2����ʹ������Ȼ�̼��Һ��ɫ��
��RCOOH![]()
![]() (R����)��
(R����)��
��![]()
![]()
![]() ��
��
��ش��������⣺
��1��A�Ľṹ��ʽΪ________��D�Ĺ����ŵ�����Ϊ____________��
��2�����ķ�Ӧ������________��
��3��д��B��C�Ļ�ѧ����ʽ�� ______________________________________��
��4��E�ж���ͬ���칹��,ͬʱ��������������E��ͬ���칹��Ľṹ��ʽ_______��
��.�ܷ���������Ӧ
��.�ܷ���ˮ�ⷴӦ
��.�����к��Ļ�ֻ�б������ұ�����ֻ��һ��ȡ������
��5�����պϳ�H������·�ߣ����һ������ȩ��NH2CH(CH3)2Ϊ��ʼԭ���Ʊ�ҽҩ�м���CH3CONHCH(CH3)2�ĺϳ�·�ߡ�
________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�Ӧ2A+B![]() 3C+4D����ʾ��Ӧ����������
3C+4D����ʾ��Ӧ����������
A.VA=0.75mol/(L��s)B.VB=0.5mol/(L��s)C.VC=1.0mol/(L��s)D.VD=1.5mol/(L��s)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���һ��2L���ܱ������м���3mol A��2.5mol ��B���������·�Ӧ3A(��)��B(��)xC(��)��2D(��)��5���Ӻ�Ӧ�ﵽƽ��ʱ����������ڵ�ѹǿ��С��ͬʱCΪ0.25mol/L�����н��۴������
A.ƽ��ʱ��A��Ũ��Ϊ0.75mol/L
B.ƽ��ʱ�� B��ת����Ϊ20%
C.D��ƽ����Ӧ����Ϊ0.1mol/(L��min)
D.��Ӧ��ʼ��ƽ��Ĺ����л�������ƽ����Է��������ڼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ȣ�ClO2���㷺Ӧ����ֽ��Ư�ס�ɱ��������ˮ��������������ҵ�����ü״���ԭNaClO3�ķ����Ʊ�ClO2�������������£�
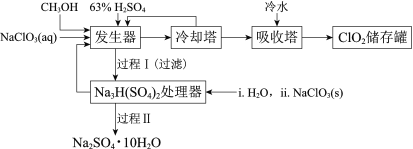
��֪��a�����������Ʊ�ClO2�ķ�Ӧ��12NaClO3+8H2SO4+3CH3OH= 12ClO2��+3HCOOH+4Na3H(SO4)2��+9H2O
b��������ʵ��۷е㣺
���� | CH3OH | HCOOH | ClO2 |
�۵�/�� | ��97 | 9 | ��59 |
�е�/�� | 65 | 101 | 11 |
(1)ClO2������ֽ��Ư�ס�ɱ���������������______�ԡ�
(2)��ȴ�����ڷ���ClO2������CH3OH��Ӧ���Ƶ�����¶�Ϊ______������ĸ����
A��0~10�� B��20~30�� C��60~70��
(3)�����̢���̢���Ի��â����Na2SO4��10H2O����ʹ����ԭ��ѭ�����á�
��֪��Na2SO4��10H2O��Na2SO4���ܽ����������ͼ��
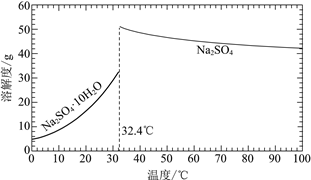
��Na3H(SO4)2�������л��â��ʱ�����NaClO3���壬��â���ܽ�ƽ��ĽǶȽ�����ԭ��______��
�ڽ��Na2SO4��10H2O��Na2SO4���ܽ�����ߣ����̢�IJ����ǣ���32.4�����������______��
��Na3H(SO4)2����������Һ�п���ѭ�����õ�ԭ����NaClO3��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����������ܱ������з�����Ӧ4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g)����2min��ﵽƽ�⡣NH3��Ũ�ȼ�����0.6mol��L��1������˵����ȷ���ǣ� ��
4NO(g)+6H2O(g)����2min��ﵽƽ�⡣NH3��Ũ�ȼ�����0.6mol��L��1������˵����ȷ���ǣ� ��
A.ƽ��ʱ��5V��(O2)=4V��(NO)
B.2minĩ�ķ�Ӧ���ʣ���NO��ʾ��0.3 mol��L-1��min-1
C.�ɻ��������ܶȲ��ٸı���ж��ﵽƽ��
D.�ɻ�������ѹǿ���ٸı���ж��ﵽƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס������ձ��и�ʢ��100mL1.5mol��L-1�����������������Һ�������ձ��зֱ����2.7g�����ۣ����㷴Ӧ���������ɵ������������ǣ� ��
A.1��1B.1��2C.2��1D.3��2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com