
【题目】碳固体氧化物电池是一种高效、环境友好的燃料电池。电池工作时,物质的转化原理如下图所示。下列说法正确的是
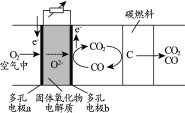
A.多孔电极a上,氧气发生氧化反应
B.多孔电极b的反应:CO-2e-+O2-=CO2
C.整个装置的总反应:CO2+C=2CO
D.该电池能将碳燃料产生的能量100%转化为电能
 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值。下列叙述正确的是( )
为阿伏加德罗常数的值。下列叙述正确的是( )
A.![]() 乙烷分子中含有的共价键数目为
乙烷分子中含有的共价键数目为![]()
B.![]() 完全溶于水转移的电子数为
完全溶于水转移的电子数为![]()
C.标准状况下,![]() 含有的原子数为
含有的原子数为![]()
D.![]() 乙烯和丙烯的混合物中含有的质子数为
乙烯和丙烯的混合物中含有的质子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是( )
A. 人们最早先根据味道来获得朴素的酸、碱概念:一切有酸味的物质都是酸,一切有涩味的物质都是碱。
B. 波义耳基于指示剂变色来分辨酸碱:酸一定能使石蕊变红,碱一定能使石蕊变蓝。
C. 地球上最大规模的化学反应是植物的光合作用,人类利用氮肥的最有效的反应是合成氨反应。
D. 酸碱质子理论:凡是能给出![]() 的物质就是酸,凡是能结合
的物质就是酸,凡是能结合![]() 的物质就是碱,适用水溶液,也适用非水溶液或无水条件。
的物质就是碱,适用水溶液,也适用非水溶液或无水条件。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备并收集干燥、纯净氯气的装置如图所示:

(1)写出实验室制备Cl2的化学方程式:___。
(2)写出指定试剂的名称,C__,D__。
(3)C的作用是__,D的作用是__,F的作用是___。
(4)检验氯气是否收集满的操作:___。
(5)实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还可以用其他很多方法制取氯气,其中用高锰酸钾和浓盐酸反应制备氯气的化学方程式可表示为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,其中该反应中HCl的作用是___,若反应产生0.5mol Cl2,则消耗的氧化剂的物质的量为___mol,反应转移的电子数是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 干冰升华和液氯气化时,都只需克服分子间作用力
B. 硫酸氢钠晶体溶于水,需要克服离子键和共价键
C. ![]() 和
和![]() 中,每个原子的最外层都具有8电子稳定结构
中,每个原子的最外层都具有8电子稳定结构
D. 石墨转化为金刚石时,既有共价键的断裂,又有共价键的形成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:
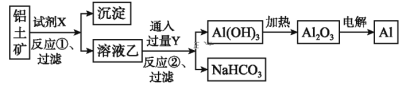
下列叙述正确的是( )
A. 试剂X可以是氢氧化钠溶液,也可以是盐酸
B. 反应①过滤后所得沉淀为氢氧化铁
C. 图中所示转化反应都不是氧化还原反应
D. 反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有以下物质相互转化。其中A为金属试回答:

(1)写出B的化学式________________,D的化学式________________。
(2)写出由D转变成H的化学方程式________________。
(3)写出向G溶液加入A的有关离子反应方程式________________。
(4)写出E转变为F的实验现象为:_________________________化学方程式:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学小组通过下列步骤测定某工厂废液中铜离子的浓度(已知废水中Fe3+对测定有干扰作用)。
i. 经检验废液中含有Fe3+离子,取V1 mL上述废液,加入NH4HF2,再加H2SO4酸化至pH<4,再次检测,未检验出Fe3+离子;
ii. 在上述溶液中,加入过量KI溶液,放置3 min,有沉淀CuI生成,立即用0.1000 mol/LNa2S2O3标准溶液滴定至浅黄色,加3 mL淀粉指示剂,继续滴定,至溶液变为浅蓝色;
iii. 再向上述溶液中加入10% KSCN溶液10 mL,继续滴定至终点,共消耗Na2S2O3溶液V2 mL。
已知:①CuI、CuSCN均为白色难溶物,CuI能吸附少量I2,CuSCN不吸附I2。
②I2在水溶液中溶解度较小,I-+I2![]() I3-、I-、I2、I3-的平衡体系溶液呈黄色
I3-、I-、I2、I3-的平衡体系溶液呈黄色
③I2+2S2O32-=2I-+S4O62-,S2O32-和S4O62-无色;
(1)①步骤i中检验含Fe3+离子操作和现象_______。
②已知 Fe3++6F-![]() [FeF6]3-,如果省略步骤i,则导致实验结果________(填“偏大”或 “偏小” ) 。
[FeF6]3-,如果省略步骤i,则导致实验结果________(填“偏大”或 “偏小” ) 。
(2)①步骤ii中生成沉淀的离子方程式_____________。
②步骤ii中加入的KI的量是理论值的2至3倍,其目的一是使Cu2+充分反应;二是__________。
(3)①步骤iii中加入KSCN溶液使ii中的沉淀转化为CuSCN沉淀,其目的是___________。
②步骤iii中判定滴定终点的现象是_____________。
(4)经小组测定,废液中c(Cu2+)=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z 和 W 代表原子序数依次增大的四种短周期主族元素,它们满足以下条件:①在元素周期表中,Z 与 Y、W 均相邻;②X、Y、W 分别位于不同周期;③Y、Z、W 三种元素的原子最外层电子数之和为 17。下列说法正确的是
A.四种元素非金属性从弱到强的顺序为:X<W<Z<Y
B.四种元素的原子半径由小到大的顺序为:r(X)<r(Y)<r(Z)<r(W)
C.X 与其余三种元素之间形成的核外电子总数为 10 的微粒只有 4 种
D.X、Y、Z 既能形成离子化合物,又能形成共价化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com