
【题目】X、Y、Z 和 W 代表原子序数依次增大的四种短周期主族元素,它们满足以下条件:①在元素周期表中,Z 与 Y、W 均相邻;②X、Y、W 分别位于不同周期;③Y、Z、W 三种元素的原子最外层电子数之和为 17。下列说法正确的是
A.四种元素非金属性从弱到强的顺序为:X<W<Z<Y
B.四种元素的原子半径由小到大的顺序为:r(X)<r(Y)<r(Z)<r(W)
C.X 与其余三种元素之间形成的核外电子总数为 10 的微粒只有 4 种
D.X、Y、Z 既能形成离子化合物,又能形成共价化合物
【答案】D
【解析】
X、Y、Z和W代表原子序数依次增大的四种短周期主族元素,在元素周期表中,Z与Y、W均相邻,Y、Z、W三种元素的原子最外层电子数之和为17,若Y、Z、W三者处于同一周期或同一主族,最外层电子数之和不可能为17,处于不同周期的Y、Z、W两两相邻,可能出现的位置关系有: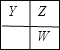 、
、![]() ,设Y的最外层电子数为x,若为第一种情况,则有x+x+1+x+1=17,解得x=5,Y、Z、W对应的三种元素分别为N,O,S;若为第二种情况,则有x+x+x+1=17,x=
,设Y的最外层电子数为x,若为第一种情况,则有x+x+1+x+1=17,解得x=5,Y、Z、W对应的三种元素分别为N,O,S;若为第二种情况,则有x+x+x+1=17,x=![]() ,不合理,且X、Y、W分别位于不同周期,则X为H元素。
,不合理,且X、Y、W分别位于不同周期,则X为H元素。
A.同周期从左到右,非金属性增强,元素非金属性Y<Z,故A错误;
B.Y和Z位于相同周期,原子半径从左到右原子半径逐渐减小,应为r(Y)>r(Z),故B错误;
C.H与其余三种元素之间形成的核外电子总数为10的微粒有NH3、NH4+、OH-、H2O、H3O+等,故C错误;
D.H、N、O三元素可以形成硝酸,属于共价化合物,可以形成硝酸铵,属于离子化合物,故D正确;
故选D。


科目:高中化学 来源: 题型:
【题目】碳固体氧化物电池是一种高效、环境友好的燃料电池。电池工作时,物质的转化原理如下图所示。下列说法正确的是
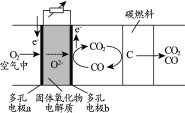
A.多孔电极a上,氧气发生氧化反应
B.多孔电极b的反应:CO-2e-+O2-=CO2
C.整个装置的总反应:CO2+C=2CO
D.该电池能将碳燃料产生的能量100%转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等体积两种一元酸“酸1”和“酸2”分别用等浓度的 KOH 溶液滴定,滴定曲线如图所示。下列说法错误的是
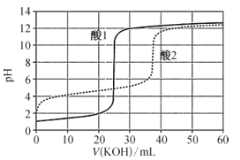
A.“酸1”比“酸2”的酸性强
B.“酸2”的浓度为0.01mo1L-1
C.“酸2”的Ka 的数量级约为10-5
D.滴定“酸1”和“酸2”均可用酚酞作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学组装了如图所示的电化学装置。电极Ⅰ为Al,其他电极均为Cu,则下列说法正确的是
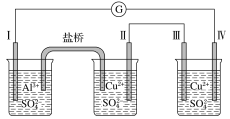
A. 电流方向:电极Ⅳ→![]() →电极Ⅰ
→电极Ⅰ
B. 电极Ⅰ发生还原反应
C. 电极Ⅱ逐渐溶解
D. 电极Ⅲ的电极反应:Cu2++2e-=Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是由常见元素组成的一些单质及其化合物之间的转化关系图。各方框表示有关的一种反应物或生成物(部分物质已经略去)。其中A、B、D在常温下均为无色无味的气体,C是能使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体。

(1)写出C→E的化学方程式: 。
(2)实验室常用加热两种固体混合物的方法制备物质C,其化学方程式为: ,干燥C常用 (填写试剂名称)。
(3)E物质遇到D物质时,会观察到 现象,若用排水法收集F,则最终集气瓶中收集到的气体为 (填写物质的化学式)。
(4)写出A→D的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四甲基氢氧化铵[(CH3)4NOH]常用作电子工业清洗剂,以四甲基氯化铵[(CH3)4NCl]为原料,采用电渗析法合成[(CH3)4NOH],其工作原理如图所示(a、b 为石墨电极,c、d、e 为离子交换膜),下列说法不正确的是
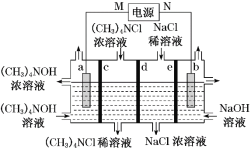
A.N 为电源正极
B.b 极 电 极 反 应 式 : 4OHˉ-4eˉ=O2↑+2H2O
C.c 为阳离子交换膜,d、e 均为阴离子交换膜
D.a、b 两极均有气体生成,同温同压下体积比为 2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家制造出一种使用固态电解质的燃料电池,其效率更高,可用于航天航空。如图1所示装置中,以稀土金属材料作为惰性电极,在电极上分别通入CH4和空气,其中固态电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-(O2+4e-=2O2-)。
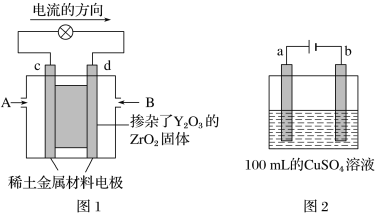
(1)c电极的名称为________(填“正极”或“负极”),d电极上的电极反应式为: ____。
(2)如图2所示用惰性电极电解100 mL 0.5 mol·L-1CuSO4溶液,a电极上的电极反应式为: __________,若a电极产生56 mL(标准状况)气体,则所得溶液的c(H+)=________(不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入________(填字母)。
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.白色无机盐 X(含三种元素,相对分子质量小于 400)能与水发生反应。为了探究 X 的组成,设计并完成了以下实验:
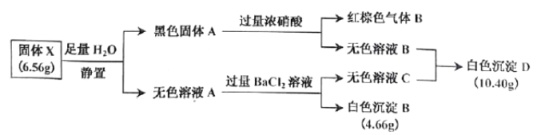
已知:白色沉淀 D 中的一种成分及质量与沉淀 B 相同。
(1)白色沉淀 D 的成分为_________(填写化学式)。
(2)黑色固体 A 与浓硝酸反应的离子方程式是_________。
(3)X 与 H2O 反应的化学方程式是_________。
Ⅱ.已知:①将 0.1 mol·Lˉ1KI 溶液加入到 0.1 mol·Lˉ1 FeCl3 溶液中时,可以看到溶液颜色加深,滴加淀粉后溶液变为蓝色;②当离子浓度相同时,氧化性:Ag+>Fe3+;③ 若浓度减小时,离子的氧化性也会随之减弱。
(1)甲同学猜测,0.1 mol·Lˉ1 KI 溶液(事先加入几滴淀粉溶液)加入到 0.1 mol·Lˉ1AgNO3 溶液中时,溶液应变蓝色。请写出该猜测对应的离子方程式_________。实 验结果未见到蓝色。
(2)乙同学认为甲同学的实验方案有问题,理由是_________。请你用原电池的方法证明Ag+也能氧化 Iˉ,要求画出实验装置图,并标明电极材料及电解质溶液 ________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读下面的信息,推断元素及有关物质,按要求回答问题:
信息①:X、Y、Z、W是常见的短周期元素,其原子序数依次增大,且原子核外最外层电子数均不少于2。(1)根据信息①,X一定不是_________(填序号)。
A.氢 B. 碳 C. 氧 D. 硫
信息②:上述四种元素的单质均能在足量的氧气中燃烧,生成的四种氧化物中,有两种能溶于稀硫酸,三种能溶于浓氢氧化钠溶液,氧化物的相对分子质量都大于26。
(2)这四种元素中是否可能有一种是铝元素?______。
信息③:向上述四种元素单质组成的混合物中加入足量盐酸溶液,固体部分溶解,过滤,向滤液中加入过量的烧碱溶液,最终溶液中析出白色沉淀。
(3)白色沉淀物的化学式为___________。
信息④:向上述四种元素单质组成的混合物中加入足量烧碱溶液,固体部分溶解,过滤,向滤液中加入过量的盐酸溶液,最终溶液中析出白色沉淀。
(4)析出白色沉淀的离子方程式为__________________________。
信息⑤:X与W同主族
(5)X与浓硫酸加热时反应的化学方程式为___;Y在X的氧化物中能剧烈燃烧,其反应现象为__。
(6)已知H![]() 的燃烧热为285.8 kJ/mol。现有X的氢化物XH4和H2的混合气体各0.1mol,与O
的燃烧热为285.8 kJ/mol。现有X的氢化物XH4和H2的混合气体各0.1mol,与O![]() 完全燃烧生成H2O(1)时,放出的热量为117.6kJ。则XH4完全燃烧的热化学反应方程式为:________。
完全燃烧生成H2O(1)时,放出的热量为117.6kJ。则XH4完全燃烧的热化学反应方程式为:________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com