
| 滴定次数 | 待测液体积 (mL) | 标准KMnO4溶液体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 3.00 | 23.00 |
| 第三次 | 25.00 | 4.00 | 24.10 |
| 难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
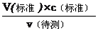
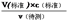 分析,可知c(待测)偏大,故C正确;D.碱式滴定管尖嘴部分有气泡,滴定后消失,造成V(标准)偏大,根据c(待测)=
分析,可知c(待测)偏大,故C正确;D.碱式滴定管尖嘴部分有气泡,滴定后消失,造成V(标准)偏大,根据c(待测)=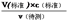 分析,可知c(标准)偏大,故D正确。(2)①因为KMnO4具有强氧化性,会腐蚀橡胶管,故应用酸式滴定管盛装;因KMnO4溶液自身的颜色作为指示剂判断滴定终点时,再滴加KMnO4溶液时,溶液将由无色变为紫色;②设草酸的浓度为c,
分析,可知c(标准)偏大,故D正确。(2)①因为KMnO4具有强氧化性,会腐蚀橡胶管,故应用酸式滴定管盛装;因KMnO4溶液自身的颜色作为指示剂判断滴定终点时,再滴加KMnO4溶液时,溶液将由无色变为紫色;②设草酸的浓度为c,

科目:高中化学 来源:不详 题型:单选题
| A.开发水能、风能、太阳能、地热能、核能等新能源,减少使用煤、石油等化石燃料 |
| B.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源 |
| C.大力开采煤、石油和天然气,以满足经济发展的需要 |
| D.大力发展新能源汽车,如混合动力汽车、电动汽车等,以减少碳、氮氧化物的排放 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(OH一)>c(H+)时,a=b | B.c(K+)>c(CH3COO—)时,a>b |
| C.c(OH一)=c(H+)时,a>b | D.c(K+)<c(CH3COO—)时,a<b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
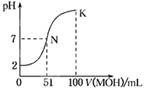
| A.HA为弱酸,MOH为强碱 |
| B.pH=7时,HA与MOH恰好完全反应 |
| C.在N点,c(A-)=c(M+) + c(MOH) |
| D.在K点,c(M+)>c(A-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.95℃时纯水的pH<7,说明加热可导致水呈酸性 |
| B.将pH=3的CH3COOH溶液加水稀释10倍后pH=4 |
| C.0.2 mol/L的盐酸1L加水到2L后,溶液的pH=1 |
| D.NaHCO3溶液水解反应的方程式: HCO3-+ H2O = H3O++ CO32- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①>②>③>④ | B.②>①>④>③ | C.③>④>②>① | D.④>③>②>① |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①中水的电离程度最小,②③④中水的电离程度一样大 |
| B.将②③混合,若pH=7,则消耗溶液的体积:②<③ |
| C.将①、④混合,若有c(CH3COO¯)>c(H+),则混合液一定呈碱性 |
| D.将①、④等体积混合,所得溶液中一定有:c(OH¯)=c(H+) + c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.稀释pH=10的氨水,溶液中所有离子的浓度均降低 |
| B.pH均为5的盐酸和氯化铵溶液中,水的电离程度相同 |
| C.等浓度的碳酸钠与碳酸氢钠溶液相比,碳酸钠溶液的pH大 |
| D.分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com