
【题目】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)对于反应:2SO2(g)+O2(g) ![]() 2SO3(g);如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)=________________________;υ(SO3)=_______________________。
2SO3(g);如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)=________________________;υ(SO3)=_______________________。
(2)已知:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) ![]() 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) ![]() SO3(g)+NO(g)的ΔH=______ kJ·mol-1。
SO3(g)+NO(g)的ΔH=______ kJ·mol-1。
(3)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是______。
a、体系压强保持不变 b、混合气体颜色保持不变
c、SO3和NO的体积比保持不变 d、每消耗1 mol SO3的同时生成1 mol NO
【答案】 0.025 mol·L-1·min-1 0.05 mol·L-1·min-1 -41.8 b、d
【解析】(1)对于反应:2SO2(g)+O2(g) ![]() 2SO3(g);反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)=
2SO3(g);反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)=![]() υ(SO2)=0.05 mol·L-1·min-1×
υ(SO2)=0.05 mol·L-1·min-1×![]() =0.025 mol·L-1·min-1;υ(SO3)= υ(SO2)=0.05 mol·L-1·min-1,故答案为:0.025 mol·L-1·min-1;0.05 mol·L-1·min-1;
=0.025 mol·L-1·min-1;υ(SO3)= υ(SO2)=0.05 mol·L-1·min-1,故答案为:0.025 mol·L-1·min-1;0.05 mol·L-1·min-1;
(2)已知:①2SO2(g)+O2(g)2SO3(g)△H=-196.6kJmol-1,②2NO(g)+O2(g)2NO2(g)△H=-113.0kJmol-1,利用盖斯定律将①×![]() -②×
-②×![]() 得NO2(g)+SO2(g)SO3(g)+NO(g)△H=
得NO2(g)+SO2(g)SO3(g)+NO(g)△H=![]() ×(-196.6kJmol-1)-
×(-196.6kJmol-1)- ![]() ×(-113.0kJmol-1)=-41.8kJmol-1,故答案为:-41.8;
×(-113.0kJmol-1)=-41.8kJmol-1,故答案为:-41.8;
(3)a.无论是否达到平衡,体系压强都保持不变,不能用于判断是否达到平衡状态,故a错误;b.混合气体颜色保持不变,说明浓度不变,达到平衡状态,故b正确;c.SO3和NO的计量数之比为1:1,无论是否达到平衡,二者的体积比保持不变,不能判断是否达到平衡状态,故c错误;d.物质的量之比等于化学计量数之比,每消耗1mol SO3的同时生成1molNO,表示正逆反应速率相等,反应达到平衡状态,故d正确;故答案为:bd。


科目:高中化学 来源: 题型:
【题目】已知分解1mol KClO3放出热量38.8kJ,在MnO2下加热,KClO3的分解机理为:
①2KClO3+4MnO2![]() 2KCl+2Mn2O7 慢
2KCl+2Mn2O7 慢
②2Mn2O7![]() 4MnO2+3O2 快
4MnO2+3O2 快
下列有关说法不正确的是( )
A.1 mol KClO3所具有的总能量高于1 mol KCl所具有的总能量
B.KClO3分解速率快慢主要取决于反应①
C.1 g KClO3 ,1 g MnO2,0.1 g Mn2O7混合加热,充分反应后MnO2质量为1 g
D.将固体二氧化锰碾碎,可加快KClO3的分解速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验中需用2.0molL-1的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3固体的质量分别为 ( )
A. 1 000mL;212.0g B. 500mL;100.7g
C. 1000mL;201.4g D. 100mL;21.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸钾是一种强氧化剂,在不同条件下KClO3将KI氧化为I2或KIO3。某实验小组在实验室中对KClO3和KI的反应进行了探究。回答下列问题:
实验一 制取氯酸钾
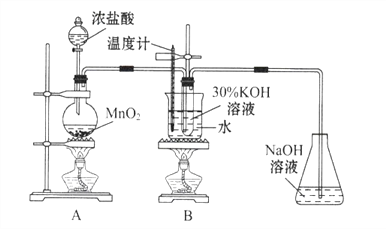
(1)A中反应的化学方程式为_______。实验开始时,首先进行的实验步骤是________。
(2)制取实验结束后,取出B中试管冷却结晶,过滤,洗涤.该实验操作过程需要的玻璃仪器有_______.
(3)A和B装置之间缺少除去氯气中氯化氢的装置,是否会对实验结果产生不利影响,其理由是_________(填“是”或“否”,若选择“是”请说明理由,若选择“否”则不需说明理由)
实验二 氯酸钾与碘化钾反应的研究
(4)该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
试管编号 | 1 | 2 | 3 | 4 |
0.20molL﹣1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0molL﹣1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
实验现象 |
①系列a实验的实验目的是__.
②设计1号试管实验的作用是__.
③若2号试管实验现象是溶液变为黄色,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如右图所示。关于这两种晶体的说法正确的是

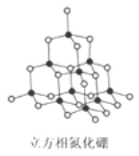
A.两种晶体均为原子晶体
B.立方相氮化硼含有σ键和π键,所以硬度大
C.六方相氮化硼层结构与石墨相似却不导电的原因是层状结构中没有自由移动的电子
D.NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一.1mol NH4BF4含有1 mol配位键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨硼烷是一种有效、安全的固体储氢材料,氨硼烷的结构和乙烷相似,如下图。

(1)氨硼烷的晶体类型为____________.
(2)氨硼烷分子中氮原子、硼原子的杂化轨道类型分别为 和 .
(3)氨硼烷晶体中存在的作用力有 (填序号)
A离子键 B极性键 C非极性键 D配位键 E金属键 F氢键 G范德华力
(4)硼酸的结构式可表示为 ,请写出硼酸溶于水后溶液显酸性的离子方程式 ________ 。
,请写出硼酸溶于水后溶液显酸性的离子方程式 ________ 。
(5)以NaBH4为硼源、某配合物为氨源可用于制备氨硼烷.为测定该配合物的结构,取2.32g配合物进行如下实验:用重量法分析金属元素,测得镍元素的质量为0.59g;在碱性条件下加热蒸出NH3,用滴定法测出其物质的量为0.06mol;滴加过量硝酸银溶液,有白色沉淀生成,加热,沉淀没有增加;用摩尔法分析含量,测得氯元素质量为0.71g.
①该配合物中镍离子的基态电子排布式为 .
②该配合物的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(双选)油脂是人体重要的能源物质,下列关于油脂的叙述正确的是( )
A. 油脂的主要成分是高级脂肪酸 B. 油脂属于天然有机高分子化合物
C. 煎炸食物的花生油比牛油的熔点低 D. 油脂可以在碱性条件下水解,用于制取肥皂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com