
【题目】“要想做好实验,就要敏于观察。”——波义耳。体弱多病的波义耳为给自己治病自修医 学,到处寻方问药。自己配制药物,所以研究医学必须研制药物和做实验。下列有关实验的 选项正确的是( )
A.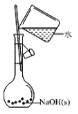 配制 0.10 mol/L NaOH 溶液B.
配制 0.10 mol/L NaOH 溶液B. 除去 CO 中的 CO2
除去 CO 中的 CO2
C.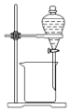 用来分离乙醇和水D.
用来分离乙醇和水D.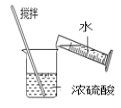 稀释浓硫酸
稀释浓硫酸
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】一般较强酸可制取较弱酸,这是复分解反应的规律之一。已知在常温下测得浓度均为0.1mol/L的下列 3 种溶液的 pH:
溶质 | NaHCO3 | Na2CO3 | NaClO |
pH | 8.34 | 11.6 | 10.3 |
下列有关说法正确的是( )
A. 以上溶液的 pH 是用广泛 pH 试纸测定的
B. 反应CO2+H2O+2NaClO=Na2CO3+2HClO可以发生
C. 室温下,电离常数: K2( H2CO3)>K( HClO)
D. 在新制氯水中加入少量 NaHCO3固体可以提高溶液中 HClO 的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
已知:①CuCl可以由CuCl2用适当的还原剂如SO2,SnCl2等还原制得:2Cu2++2Cl-+SO2+2H2O![]() 2CuCl↓+4H++SO42-,2CuCl2+SnCl2=2CuCl↓+SnCl4,②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子:
2CuCl↓+4H++SO42-,2CuCl2+SnCl2=2CuCl↓+SnCl4,②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子:  。
。
请回答下列问题:
(1)基态Cu原子的核外电子排布式为_____;H、N、O三种元素的电负性由大到小的顺序是____。
(2)SO2分子的空间构型为________;与SnCl4互为等电子体的一种离子的化学式为________。
(3)乙二胺分子中氮原子轨道的杂化类型为________。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是__________。
(4)②中所形成的配离子中含有的化学键类型有______(填字母)。
A.配位键 B.极性键 C.离子键 D.非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为![]() ,下列关于该物质的说法中不正确的是
,下列关于该物质的说法中不正确的是
A. 该物质不能发生消去反应,但能在一定条件下发生加聚反应
B. 该物质不能和AgNO3溶液反应产生AgBr沉淀
C. 该物质在NaOH的醇溶液中加热可转化为醇类
D. 该物质可使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是A、B、C、D四种有机物的有关信息:
A | ①能使溴的四氯化碳溶液褪色; ②能与水在一定条件下反应生成C; ③比例模型为: |
B | ①由C、H两种元素组成; ②球棍模型为: |
C | ①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③与二甲醚互为同分异构体。 |
D | ①相对分子质量比C物质少2; ②能由物质C氧化而成。 |
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称为___________(系统命名法);写出该生成物与足量的NaOH水溶液共热的化学方程式___________。
(2)A与氢气发生加成反应后生成分子F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2。当n=________时,这类有机物开始出现同分异构体。
(3)B具有的性质是________(填序号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤高锰酸钾酸性溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在浓硫酸作用下,B与浓硝酸反应的化学方程式为: _______
(4)写出由C氧化生成D的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在由Na2S、Na2SO3、Na2SO4组成的固体混合物中,已知S的质量分数为25.6%,则氧的质量分数为
A. 36.8%B. 37.6%C. 51.2%D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L硫酸溶液450mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是_________(填序号),本实验所用玻璃仪器E的规格和名称为_____________。

(2)下列操作中,容量瓶所不具备的功能有__________(填序号)
a.配制一定体积准确浓度的标准溶液 b.长期贮存溶液
c.用来加热溶解固体溶质 d.量取220毫升体积的液
(3)如果实验室有l0mL、25mL、50mL量筒,根据计算得知:量取质量分数为98%、密度为1.84g.cm-3的浓硫酸应选用__________mL规格的量筒最好。
(4)在配制NaOH溶液实验中,其他操作均正确,若定容时仰视刻度线,则所配制溶液浓度_______0.1mol/L(填“大于”“等于”或“小于”,下同)。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度__________0.1mol/L。
(5)如果定容时不小心超过刻度线,应如何操作__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型的合成氨的方法如图所示,下列说法正确的是
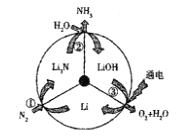
A. 反应①属于“氮的固定”B. 反应②属于氧化还原反应
C. 反应③可通过电解![]() 水溶液实现D. 上述三步循环的总结果为:
水溶液实现D. 上述三步循环的总结果为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】机动车排放的污染物主要有碳氢化合物、一氧化碳和氮氧化物等。汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。
(1)已知:![]()
![]()
![]()
![]()
![]()
![]()
则反应![]()
![]() __________。
__________。
(2)科学家研究出了一种高效催化剂,可以将![]() 和
和![]() 发生反应生成
发生反应生成![]() (g)和
(g)和![]() (g)。在T℃下,向某恒容密闭容器中通入a mol/L
(g)。在T℃下,向某恒容密闭容器中通入a mol/L![]() 、b mol/L
、b mol/L![]() ,使其发生上述反应,测得
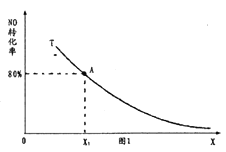
,使其发生上述反应,测得![]() 的平衡转化率与投料比X(表示a、b两者的比值)的关系如图1中曲线所示。若
的平衡转化率与投料比X(表示a、b两者的比值)的关系如图1中曲线所示。若![]() 、
、![]() ,反应开始到达到平衡所用时间是2min,则反应发生2min内
,反应开始到达到平衡所用时间是2min,则反应发生2min内![]() 的平均反应速率v(
的平均反应速率v(![]() )=________,平衡态A点的平衡常数K=________。
)=________,平衡态A点的平衡常数K=________。
(3)柴油燃油车是通过尿素-选择性催化还原(Urea-SCR)法处理氮氧化物。Urea-SCR的工作原理为:尿素[![]() ]水溶液通过喷嘴喷入排气管中,当温度高于160℃时尿素水解产生
]水溶液通过喷嘴喷入排气管中,当温度高于160℃时尿素水解产生![]() ,生成的
,生成的![]() 与尾气混合后,加入适合的催化剂,使氮氧化物得以处理。图2为在不同投料比[
与尾气混合后,加入适合的催化剂,使氮氧化物得以处理。图2为在不同投料比[![]() ]时
]时![]() 转化效率随温度变化的曲线。
转化效率随温度变化的曲线。
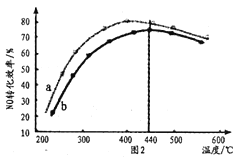
①尿素与![]() 物质的量比a_____b(填“>”、“=”或“<”)。
物质的量比a_____b(填“>”、“=”或“<”)。
②由图可知,下列说法错误的是____
A.400℃以下,随着温度升高,尿素水解释放氨气的速率加快,![]() 转化效率升高
转化效率升高
B.400℃以下,温度升高,反应活化能降低,导致化学反应速率加快
C.440℃以上,温度过高,可能使催化剂活性降低,导致![]() 转化效率下降
转化效率下降
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com