
【题目】A、B、C、D、E、F六种常见的单质或化合物在一定条件下有如下图所示的相互转化关系,所有反应物和生成物均已给出。
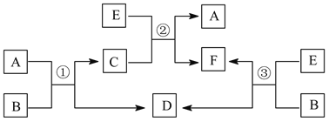
(1)若B在常温下为液态;C是一种有磁性的化合物;E是一种无色、无味的有毒气体。则反应③的化学方程式______________。
(2)若B由两种元素组成,其简单离子的电子层结构相同;绿色植物的光合作用和呼吸作用可实现自然界中D、E的循环。则B的电子式为_________________,11.6 g A和E组成的混合气体与足量的B固体反应,固体增重3.6 g,则A、E混合气中E 的体积分数为_________________________。
(3)若A和E都是第四周期常见的金属单质,其余都是常见的盐,反应①②③都在溶液中进行,则B、C、F氧化性由强到弱顺序为(用离子符号表示)____________。
【答案】CO+H2O![]() CO2+H2
CO2+H2 ![]() 20% Fe3+>Cu2+>Zn2+
20% Fe3+>Cu2+>Zn2+
【解析】
(1)若在常温下为液态,则B是水,C是一种有磁性的化合物,则A为Fe,C为Fe3O4,D为H2,E是一种无色、无味的有毒气体,由转化关系可知,E为CO,F为CO2;
(2)若B由两种元素组成,其简单离子的电子层结构相同,绿色植物的光合作用和呼吸作用能实现自然界中D和E的循环,则D和E分别是CO2 和O2的一种,可以推断B是Na2O2,由反应①可知E和A反应生成D,由反应③可知E和B反应生成D,则D是O2;结合反应②、反应③可知E是CO2,F为Na2CO3,A为H2O,C为NaOH;
(3)若A和E都是第四周期常见的金属单质,其余都是常见的盐,反应①②③都在溶液中进行,则根据物质转化关系可知:A为Cu单质,B含Fe3+,C含Cu2+,D含Fe2+,E为Zn,F含Zn2+。据此解答。
(1)根据上述分析可知:A为Fe,B为H2O,C为Fe3O4,D为O2,E为CO,F为CO2。反应③是CO与H2O在高温下反应产生CO2和H2,反应方程式为:CO+H2O![]() CO2+H2;
CO2+H2;
(2)根据上述分析可知:A为H2O,B为Na2O2,C为NaOH,D为H2,E为CO2,F为Na2CO3。
B是Na2O2,该物质是离子化合物,电子式为:![]() ;
;
11.6 g H2O、CO2的混合气体与足量Na2O2发生反应:2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2=2Na2CO3+O2,固体增重3.6 g,假设混合气体中H2O、CO2的物质的量分别是x、y,则18x+44y=11.6,根据方程式中物质反应转化关系可知2x+28y=3.6,解得x=0.4 mol,y=0.1 mol,由于在相同条件下气体的体积比等于气体的物质的量的比,所以H2O、CO2的混合气体中CO2的体积分数为:![]() ×100%=20%;
×100%=20%;
(3)根据上述分析可知:A为Cu单质,B为含Fe3+的盐,C为含Cu2+的盐,D为含Fe2+的盐,E为Zn,F为含Zn2+的盐。反应①为Cu+2Fe3+=2Fe2++Cu2+,可知物质的氧化性:Fe3+>Cu2+;反应②为Zn+Cu2+=Zn2++Cu2+,可知物质的氧化性:Cu2+>Zn2+;反应③为Zn+2Fe3+=2Fe2++Zn2+,可知物质的氧化性:Fe3+>Zn2+。则Fe3+、Cu2+、Zn2+的氧化性由强到弱的顺序为:Fe3+>Cu2+>Zn2+。


科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应2X(g)+3Y(g)![]() 4Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.2mol·L-1、0.3 mol·L-1、0.16 mol·L-1,则下列判断不合理的是
4Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.2mol·L-1、0.3 mol·L-1、0.16 mol·L-1,则下列判断不合理的是
A.c1∶c2=2∶3
B.X、Y的转化率不相等
C.平衡时,Y和Z的生成速率之比为3∶4
D.c1的取值范围为0<c1<0.28 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
A. 原子半径:A>B>D>CB. 原子序数:d>c>b>a
C. 离子半径:C>D>B>AD. 单质的还原性:A>B>D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水溶液中的离子反应在许多领域都有广泛的应用,请回答下列问题。
(1)在配制氯化铁溶液时,常常会出现浑浊,可以加入少量的__________防止上述问题。
(2)明矾具有净水的作用,原因是:___________________________(用离子方程式表示)。
(3)将25 ℃时pH=12的NaOH溶液a L与pH=1的HCl溶液b L混合。若所得混合液为中性,则a∶b=______________。
(4)加热蒸干AlCl3溶液并灼烧所得固体,最终得到的产物是______________
(5)常温下,已知Ksp[M(OH)3] =1.0×1038,要使溶液中的M3+降至105mol/L,则应调节溶液pH=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( )
A. -44.2kJ·mol-1 B. +44.2kJ·mlo-1
C. -330kJ·mol-1 D. +330kJ·mlo-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数,下列说法正确的是
A.标准状况下,22.4LSO3中含有氧原子数目为3NA
B.在25℃、101kPa下,1 mol 硫和2 mol硫燃烧热相等
C.18 g D2O中含有的质子数目为10NA
D.含0.5 mol H2SO4的稀溶液与含0.5mol Ba(OH)2 的晶体完全中和所放出的热量为中和热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A. 的同分异构体中,有醇、酚、酯类物质
的同分异构体中,有醇、酚、酯类物质
B.1 mol![]() 最多能与4 mol NaOH反应
最多能与4 mol NaOH反应
C.纯净物C4H8的核磁共振氢谱峰最多为4
D.化学式为C8H8的有机物,一定能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 0.10 mol·L-1NaOH溶液分别滴定20.00 mL 0.10 mol·L-1HCl溶液和20.00 mL 0.10 mol·L-1CH3COOH溶液,得到2条滴定曲线,如下图所示,则下列说法正确的是
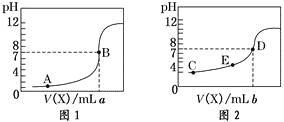
A.图2是滴定盐酸的曲线
B.a与b的关系是:a<b
C.E点对应离子浓度由大到小的顺序为: c(CH3COO-) >c(Na+) >c(H+) >c(OH-)
D.这两次滴定都可以用甲基橙作为指示剂且颜色变化为红变橙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】留兰香(薄荷中的一种)可用来治疗感冒咳嗽、胃痛腹胀、神经性头痛等,其有效成分为葛缕酮(结构简式如图)。下列有关葛缕酮的说法正确的是
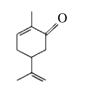
A.葛缕酮的分子式为C10H16O
B.葛缕酮使溴水和酸性KMnO4溶液褪色的原理相同
C.葛缕酮中所有碳原子可能处于同一个平面
D.羟基直接连苯环且苯环上有2个取代基的葛缕酮的同分异构体有12种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com