
【题目】下列说法正确的是
A.  与
与![]() 含有相同的官能团,互为同系物
含有相同的官能团,互为同系物
B. 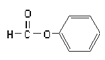 属于醛类,官能团为-CHO
属于醛类,官能团为-CHO
C. ![]() 的名称为:2-乙基-1-丁烯
的名称为:2-乙基-1-丁烯
D. ![]() 的名称为:2-甲基-1,3-二丁烯
的名称为:2-甲基-1,3-二丁烯
【答案】C
【解析】
A. 前者—OH与苯环的侧链相连,属于醇类,后者—OH直接与苯环相连,属于酚类,尽管分子构成相差了1个CH2,但是二者不是同一类物质,所以它们不互为同系物,A错误;
B. 该物质属于酯类(甲酸酯,含有醛基),官能团为酯基, B错误;
C. 该物质的官能团为碳碳双键,含有官能团的最长的碳链有4个C,因此主链含有4个C,为丁烯;编号时官能团的编号要小,因此碳碳双键的编号为1,乙基的编号为2,命名为2-乙基-1-丁烯,C正确;
D. 该物质中含有2个碳碳双键,且含有碳碳双键最长的碳链有4个碳原子,因此该物质为丁二烯。编号时,不管是从左端还是右端,碳碳双键的编号均为1、3,因此编号的选择,让甲基的编号的编号小,甲基的编号为2,则该物质的名称应为:2-甲基-1,3-丁二烯,故D错误。


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
【题目】三氧化二铬可用作搪瓷、陶瓷、人造革、建筑材料的着色剂。由高碳铬铁合金(含Cr、Fe及C)制备三氧化二铬的工艺流程如下:

已知:Cr(OH)3是两性氢氧化物,草酸亚铁为微溶物。
回答下列问题:
(1)步骤Ⅰ浸取时,为提高浸取速率,除将高碳铬铁合金制成粉末外,还可采取的措施是__________________________(写一点);浸取铬时反应的离子方程式为_______________。
(2)步骤Ⅱ滤渣返回再次浸取的目的是_____________________________________________。
(3)步骤Ⅲ除铁时,溶液的pH对铁的去除率影响如图1所示:

图1 图2
pH小于2.3时,铁去除率低,其原因是_______________________________________。
(4)步骤Ⅳ能说明沉淀已洗涤干净的操作是________________________________________。
(5)步骤Ⅴ沉铬时,生成Cr(OH)3的化学方程式为_____________________________;沉铬时,溶液pH与铬的回收率关系如图2所示,当pH>8.5时,pH越大,铬的回收率越低,其可能原因是____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度如表所示,下列说法不正确的是
物质 | X | Y | Z | W |
初始浓度/mol·L-1 | 0.5 | 0.5 | 0 | 0 |
平衡浓度/mol·L-1 | 0.1 | 0.1 | 0.4 | 0.4 |
A. 反应达到平衡时,X的体积分数为10%
B. 该温度下反应的平衡常数K=16
C. 保持温度不变增大压强,反应速率加快,平衡向正反应方向移动
D. 若X、Y的初始浓度均为0.8 mol·L-1,则达到平衡时,W的浓度为0.64 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,醋酸溶液中存在电离平衡:CH3COOH ![]() CH3COO- + H+
CH3COO- + H+
(1)某温度时,0.1 mol·L-1的醋酸溶液中的c(H+) 与0.01 mol·L-1 的醋酸溶液中的c(H+)的比值 ____(填“大于”“小于”或“等于”)10,理由是_________。
(2)常温下0.1 mol/L的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是:_____________。
A.c(H+) B.![]() C.c(H+)·c(OH) D.c(OH)/c(H+)
C.c(H+)·c(OH) D.c(OH)/c(H+)
(3)现有pH均为3的醋酸、硫酸两瓶溶液:
①设两种溶液的物质的量浓度依次为c1、c2,则其关系式为_________(用“<”“>”或“=”表示,下同)。
②取相同体积的两种酸分别加入等体积的蒸馏水后,再分别加入少量等量的锌粉,反应开始时放出氢气的速率依次为v1、v2,则其关系式为_______,反应结束放出的氢气的体积依次为V1、V2,则其关系式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释工业生产或应用的化学用语中,不正确的是
A. FeCl3溶液刻蚀铜电路板:2Fe3++Cu==2Fe2++Cu2+
B. Na2O2用作供氧剂:Na2O2+H2O==2NaOH +O2↑
C. 氯气制漂白液:Cl2+2NaOH==NaCl+NaClO +H2O
D. Na2CO3溶液处理水垢:CaSO4(s)+CO32![]() CaCO3(s)+SO42
CaCO3(s)+SO42
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型)。下列关于普伐他汀的性质描述不正确的是( )
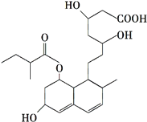
A. 3个—OH皆可因催化氧化生成醛基
B. 能使酸性KMnO4溶液褪色
C. 能发生加成、取代、消去反应
D. 1 mol该物质最多可与2mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.8g NaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是( )
A.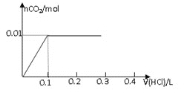
B.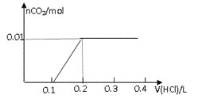
C.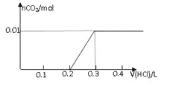
D.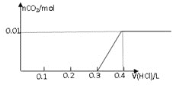
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫、氯、氮是三种常见的非金属元素。
完成下列填空:
(1)我们祖先的四大发明之一黑火药的爆炸反应为:S+2KNO3+3C A+N2↑+3CO2↑(已配平)。氮原子核外电子排布式为______________,生成物固体 A属于_____晶体。
(2)工业合成氨可以实现大规模固氮,氨可用于生产氯化铵、硫酸铵等化学肥料,等物质的量浓度的两溶液相同温度下pH大小为:氯化铵___________硫酸铵(选填>、=或<)。
(3)工业上在催化剂条件下,用NH3作为还原剂将烟气中的NO2还原成无害的氮气和水,反应方程式可表示为:8NH3(g)+6NO2(g)![]() 7N2(g)+12H2O(g),用单线桥标出该反应电子转移的方向和数目______,若该反应氧化产物比还原产物多0.1mol,被吸收的NO2在标准状况下的体积为_________。
7N2(g)+12H2O(g),用单线桥标出该反应电子转移的方向和数目______,若该反应氧化产物比还原产物多0.1mol,被吸收的NO2在标准状况下的体积为_________。
(4)氯水成分的多样性决定了其性质的复杂性,氯气可用作自来水生产过程中的消毒剂,写出其中主要的化学反应方程式______________________________,在硝酸银溶液中滴加氯水,可以看到有白色沉淀产生,起作用的微粒是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高岭土主要由高岭石![]() 长期风化而成,其中还含有一定量的白云石
长期风化而成,其中还含有一定量的白云石![]() ,高岭土是制作陶瓷的原料。完成下列填空:
,高岭土是制作陶瓷的原料。完成下列填空:
(1)矿石中除![]() 外的三种非金属元素的原子半径从小到大的顺序是______。硅原子的核外电子排布式是___,镁原子核外有_________种能量不同的电子。
外的三种非金属元素的原子半径从小到大的顺序是______。硅原子的核外电子排布式是___,镁原子核外有_________种能量不同的电子。
(2)判断![]() 的金属性强于
的金属性强于![]() 的事实是____________。
的事实是____________。
a. ![]() 的碱性强于
的碱性强于![]()
b. ![]() 微溶于水,
微溶于水,![]() 难溶于水
难溶于水
c. 与热水反应,钙比镁剧烈
d. 单质钙保存在煤油里,单质镁不需要
(3)![]() 和
和![]() 同是ⅣA族元素的氧化物,
同是ⅣA族元素的氧化物,![]() 的熔点明显比
的熔点明显比![]() 高的原因是________。
高的原因是________。
(4)氮化硅(![]() )是一种新型陶瓷材料,制备反应如下:
)是一种新型陶瓷材料,制备反应如下:![]() ,该反应的平衡常数表达式___________;反应达到平衡后,若增大
,该反应的平衡常数表达式___________;反应达到平衡后,若增大![]() 浓度,则
浓度,则![]() 值____________(填“增大”“减小”或“不变”)。
值____________(填“增大”“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com