
【题目】常见无机物A、B、C、D存在如图转化关系:
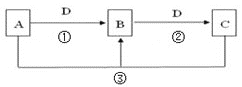
(1)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一![]() 遇空气会变色,则反应
遇空气会变色,则反应![]() 的化学方程式为_________________________________________________。
的化学方程式为_________________________________________________。
(2)若A为常见挥发性强酸,D是生产生活中用量最大用途最广的金属单质,则B的化学式是_____________________。
(3)若A、C、D都是常见气体,C是形成酸雨的主要气体,则A的电子式是____________。
(4)若A、B、C的水溶液均显碱性,焰色反应均为黄色,D为![]() ,举出C的一种用途_______________________。
,举出C的一种用途_______________________。
【答案】![]()
![]()
![]() 治疗胃酸过多、发酵粉、泡沫灭火器等
治疗胃酸过多、发酵粉、泡沫灭火器等
【解析】
(1)若A是一种碱性气体,常用作制冷剂,为氨气,B是汽车尾气之一,遇空气会变色,则B是NO,D是氧气,C是二氧化氮,反应![]() 的化学方程式为:
的化学方程式为:![]() ,
,
故答案为:![]() ;
;
(2)若A为常见挥发性强酸,D是生产生活中用量最大用途最广的金属单质,则D是Fe,B能和D反应生成C,则A是硝酸、B是硝酸铁、C是硝酸亚铁,则B的化学式为![]() ,
,
故答案为:![]() ;
;
(3)若A、C、D都是常见气体,C是形成酸雨的主要气体,则C是二氧化硫,A是硫化氢、D是氧气、B是S,A的电子式是![]() ,
,
故答案为:![]() ;
;
(4)若A、B、C的水溶液均显碱性,焰色反应均为黄色,说明都含有Na元素,D为![]() ,A为NaOH、B是碳酸钠、C为碳酸氢钠,B为强碱弱酸盐,碳酸根离子水解导致溶液呈碱性,碳酸氢钠溶液呈弱碱性,碳酸氢钠能水解,所以其用途有治疗胃酸过多、发酵粉、泡沫灭火器等,
,A为NaOH、B是碳酸钠、C为碳酸氢钠,B为强碱弱酸盐,碳酸根离子水解导致溶液呈碱性,碳酸氢钠溶液呈弱碱性,碳酸氢钠能水解,所以其用途有治疗胃酸过多、发酵粉、泡沫灭火器等,
故答案为:治疗胃酸过多、发酵粉、泡沫灭火器等。


科目:高中化学 来源: 题型:
【题目】(1)可逆反应2SO2(g)+O2(g)![]() 2SO3(g);ΔH<0,在其他条件不变时,
2SO3(g);ΔH<0,在其他条件不变时,
①升温反应速率________,增大压强反应速率________;
②达到化学平衡时,v正(SO2)________(填“大于”“小于”或“等于”)v逆(SO3);若平衡后增加O2的浓度,平衡向________方向移动,SO2的转化率________;若升高温度,则平衡向________方向移动。
(2)将等物质的量的A、B、C、D四种物质混合,发生如下反应:aA+bB![]() cC(s)+dD,当反应进行一定时间后,测得A减少了nmol,B减少了
cC(s)+dD,当反应进行一定时间后,测得A减少了nmol,B减少了![]() nmol,C增加了
nmol,C增加了![]() nmol,D增加了nmol,此时达到化学平衡,该化学方程式中各物质的系数为:a=______、b=______、c=______、d=______。
nmol,D增加了nmol,此时达到化学平衡,该化学方程式中各物质的系数为:a=______、b=______、c=______、d=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.40gNaOH中含有的共用电子对数为2NA
B.常温常压下,1.8g甲基(—CD3)中含有的中子数为0.9NA
C.31g白磷(![]() )含有共价键的总数为6NA
)含有共价键的总数为6NA
D.标况下,22.4LH2O中所含氢氧键的数目约为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些有机物质的分子式采取适当变形会简化计算。下列计算中错误的是
A.Wg 葡萄糖充分燃烧后,燃烧产物和足量的Na2O2充分反应,固体质量增加 Wg
B.等质量的甲烷、乙烯、乙炔充分燃烧,消耗的氧气的物质的量依次增多
C.乙酸和两种链状单烯烃混合物中氧的质量分数为 a,则碳的质量分数是![]()
D.等物质的量的乙醇与丙烯酸(CH2=CH-COOH)充分燃烧,消耗的氧气的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.100molL-1NaOH溶液分别滴定20.00mL浓度均0.100molL-1CH3COOH溶液和HCN溶液,所得滴定曲线如图。下列说法不正确的是( )
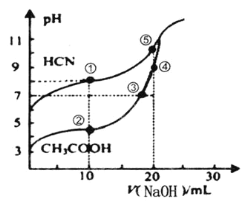
A.点①和点②所示溶液中:c(CH3COO-)>c(CN-)
B.点③时:c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
C.点③和点④所示溶液中水的电离程度:③<④
D.点④溶液中阴离子总数小于点⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物 A 的分子式为 C9H18O2,可发生如下转化,其中 B 与 C 相对分子质量相同, 则 A 可能的结构有
![]()
A.4 种B.6 种C.8 种D.16 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制乙烯通常采用95%的乙醇与浓硫酸![]() 体积比为1:3混合加热到170℃方法制得,其制备原理可表示如下:CH3CH2OH+H2SO4(浓)
体积比为1:3混合加热到170℃方法制得,其制备原理可表示如下:CH3CH2OH+H2SO4(浓)![]() CH3CH2OSO2OH+H2O①
CH3CH2OSO2OH+H2O①
CH3CH2OSO2OH(浓)![]() CH2= CH2 + H2SO4②
CH2= CH2 + H2SO4②
(1)浓硫酸在乙烯生成中作用为 ______ ,反应①属于 ______ 反应,反应②属于 ______ 反应.
(2)此法在实际操作中由于浓H2SO4的用量大、比热容高,加热至170℃所需时间长,有人将乙醇和浓H2SO4的混合液加热到80℃时,一次性投入一些小碎块的生石灰,大大缩短了反应所需时间,提高了乙烯的产率,试用速率和平衡理论解释之 ______
(3)反应过程中乙醇常被炭化,使溶液有黑色物质出现,随着反应进行炭化现象越来越严重,同时还可使制得的乙烯气体中含有CO2、SO2等气体,为了减少反应过程中炭化现象又不影响乙烯的生成,下列措施合理的是 ______ .
A.调整乙醇和浓硫酸的体积比为1:4
B.调整乙醇和浓硫酸的体积比为1:2
C.用大理石代替碎瓷片
D.降低反应体系温度至140℃
E.用其他脱水剂(如P2O5)代替浓硫酸
(4)如图为有人设计确认混合气体中含有乙烯和二氧化硫的实验装置图.(下列试剂可供选择:品红溶液、氢氧化钠溶液、溴水、酸性高锰酸钾)
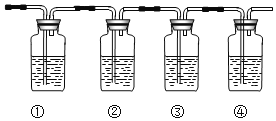
A.①②③④中可盛放的试剂分别为①______ ; ②______ ;③ ______ ; ④ ______ ;
B.能说明二氧化硫气体存在的现象是 ______ ;
C.能确认含有乙烯的现象是 ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl是一种化工原料,可以制备一系列物质,如图所示。下列说法不正确的是( )
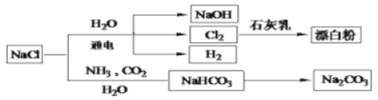
A.以电解饱和食盐水为基础制取氯气等产品的工业称为氯碱工业
B.用石灰乳与Cl2制取的漂白粉的有效成分是Ca(ClO)2
C.Cl2不与铁反应,因此液氯可储存在钢瓶中
D.侯氏制碱法实现了从NaCl到Na2CO3的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示方法正确的是( )
A. 若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B. 由C(石墨)=C(金刚石)ΔH=+1.9 kJ·mol-1可知,金刚石比石墨稳定
C. 在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)![]() 2H2O(l) ΔH=+285.8 kJ·mol-1
2H2O(l) ΔH=+285.8 kJ·mol-1
D. 在稀溶液中:H++OH-![]() H2O ΔH=-57.3 kJ·mol-1,若将含1mol CH3COOH与含1mol NaOH的溶液混合,放出的热量小于57.3 kJ
H2O ΔH=-57.3 kJ·mol-1,若将含1mol CH3COOH与含1mol NaOH的溶液混合,放出的热量小于57.3 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com