
����Ŀ��36.5 g HCl�ܽ���1 Lˮ��(ˮ���ܶȽ���Ϊ1 g��mL��1)��������Һ���ܶ�Ϊ�� g��mL��1����������Ϊw�����ʵ���Ũ��Ϊc mol��L��1��NA��ʾ�����ӵ���������������������ȷ����(����)
A. ������Һ�����ʵ���Ũ��Ϊ1 mol��L��1
B. ������Һ�к���NA��HCl����
C. 36.5 g HCl����ռ�е����Ϊ22.4 L
D. ������Һ������������w��![]()
���𰸡�D
��������
A��36.5gHCl�ܽ���1Lˮ��(ˮ���ܶȽ���Ϊ1g/ml)��������Һ���������1L������Ϊ�Ȼ��⣬���ʵ���Ũ��c=![]() =
=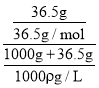 =
= ![]() mol/L����A����
mol/L����A����
B���Ȼ�����ǿ����ʣ�����ˮ��ȫ���룬��Һ�����Ȼ�����ӣ���B����
C��36.5gHCl�������ʵ���Ϊ1mol����״����ռ�е����Ϊ22.4L��ѡ�����¶�ѹǿ��֪������ȷ��������������C����
D��������Һ��������������=![]() =
=![]() ����D��ȷ��
����D��ȷ��
��ѡD��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1������ͨ��Fe(OH)3���壬�ɿ���������ͨ·�����������________��
��2��19gij���۽������Ȼ���ACl2�к���0.4mol Cl�����ӣ���ACl2��Ħ������________
��3���ڱ�״���£����4.2g����A�������3360mL����A������ʲô����________
��4���ڱ�״����15 g CO��CO2�Ļ�����壬���Ϊ11.2 L����CO2��CO�����֮����________��
��5���ڱ�״���£���224 L HCl��������635 mLˮ�У�����������ܶ�Ϊ1.18 g��cm��3�������������ʵ���Ũ�ȷֱ���________
��6�������������ʣ���NaCl���� ������ ��CaCO3���� ������KCl ������ ��ͭ ��CO2 ��ŨH2SO4 ��KOH���壻�������������ڵ���ʵ���________
��7��Ca(HCO3)2��Һ����������������Һ��ϵ����ӷ���ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҷ�������Ľṹ����ͼ����1mol��Ҷ�������ֱ���Ũ��ˮ��NaOH��Һ��ȫ��Ӧ�������ĵ�Br2��NaOH�����ʵ����ֱ�Ϊ( )
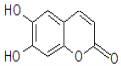
A. 2molBr2��2molNaOHB. 2molBr2��3molNaOH
C. 3molBr2��4molNaOHD. 4molBr2��4molNaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��װ����ij��ʵ����������(�г�װ��ʡ��)����ƿ��ʢ�е�����ļ����Cl2���ù�����һ��ʱ���
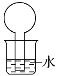
A. ֻ������CH3Clһ���л���
B. ��ƿ��Һ�治��������
C. ��ƿ�ڵ�Һ����ܻ�ֲ�
D. ��ˮ�м���ʯ����Һ���ޱ仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
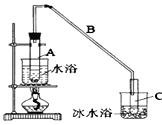
����Ŀ��ij��ѧС���������������������װ��(��ͼ)���Ի������Ʊ�����ϩ��
��֪��
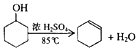
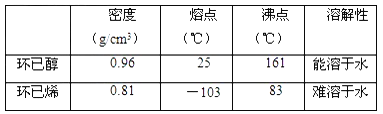
(1)�Ʊ���Ʒ��
��12.5 mL�����������Թ�A�У��ټ���l mLŨ���ᣬҡ�Ⱥ�������Ƭ��������������Ӧ��ȫ�����Թ�C�ڵõ�����ϩ��Ʒ��
�ٵ���B���˵�������е�������_____________________________________��
���Թ�C���ڱ�ˮԡ�е�Ŀ����_____________________________________��
(2)�Ʊ���Ʒ��
�ٻ���ϩ��Ʒ�к��л������������������ʵȡ����뱥��ʳ��ˮ�������á��ֲ㣬����ϩ��_____��(���ϻ���)����Һ����________(������)ϴ�ӡ�
a��KMnO4��Һ b��ϡH2SO4 c��Na2CO3��Һ
�ڽ���Һ�õ��Ļ���ϩ�ٽ��������ռ���Ʒʱ�����Ƶ��¶�Ӧ��_______���ҡ�
(3)�������ֻ���ϩ��Ʒ�ʹ�Ʒ�ķ�������������___________��
a�������Ը��������Һ b���ý����� c���ⶨ�е�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л����Һ�У�������Ũ�ȵĴ�С˳����ȷ����
A. 10 mL 0.1 mol/L��ˮ��10 mL 0.1 mol/L�����ϣ�c(Cl)��c(![]() )��c(OH)��c(H+)
)��c(OH)��c(H+)
B. 10 mL 0.1 mol/L NH4Cl��Һ��5 mL 0.2 mol/L NaOH��Һ��ϣ�c(Na+)=c(Cl)��c(OH)��c(H+)
C. 10 mL 0.1 mol/L CH3COOH��Һ��5 mL 0.2 mol/L NaOH��Һ��ϣ�c(Na+)=c(CH3COO)��c(OH)��c(H+)
D. 10 mL 0.5 mol/L CH3COONa��Һ��6 mL 1 mol/L�����ϣ�c(Cl)��c(Na+)��c(OH)��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A. �ñ���ʳ��ˮ���ˮ����ʯ���ã�������Ч���Ʋ�����Ȳ������
B. ʳƷ��װ���Ͼ���ϩ�����ӳɷ�Ӧ�����ϻ�
C. ![]() ������Ϊ4��������2������
������Ϊ4��������2������
D. �ؽᾧ���ᴿ������ʱ��Ϊ��ȥ���ʺͷ�ֹ������������Ӧ�ó��ȹ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ũ����㷺Ӧ����ϡ�н�����ʪ��ұ��ƯȾ��ҵ�������ӹ�����ҩƷ���л�ҩ��������������С�
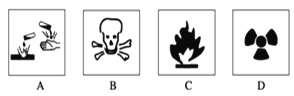
��.(1)��ʢ��Ũ������Լ�ƿ�ı�ǩ��Ӧӡ��ͼ��ʾ��־�е�____________��
(2)��12.0mol/LŨ��������230mL 0.3mol/L��ϡ���ᣬ��Ҫ����Ͳ��ȡŨ��������Ϊ______��
(3)��Һ���ƹ�������Ҫ�IJ������������ձ�������������Ͳ������____________________��
(4)��Һϡ�����������²�����
a����ȡŨ�����һ�������ˮ�����ձ���ϡ�ͣ�
b����������Ũ����������
c�����µߵ�ҡ�ȣ�
d��������ˮ���̶���1-2cm�ط������ý�ͷ�ιܼ�����ˮ����Һ����̶������У�
e����ϡ��Һת��������ƿ��ϴ���ձ��Ͳ�����������ϴ��Һת��������ƿ����
������ȷ�IJ���˳��Ϊ__________________________
(5)ʵ������е����²����ᵼ������������ҺŨ�ȣ�����ƫ��������ƫС��������������
a����ȡŨ����ʱ���ӣ�__________ ��
b����ȡŨ�������ϴ����Ͳ����ϴ��Һת��������ƿ��__________ ��
c��ʵ��ǰ������ƿ����������������ˮ��__________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��EΪԭ������������������ֶ�����Ԫ�أ�����CΪ�������ڼ����Ӱ뾶��С��Ԫ�أ�0.1mol��L1A��B��D������������Ӧ��ˮ������Һ��ˮϡ��ʱ��Һ��pH�仯�����ͼ��������˵���в���ȷ����

A. C�Ƶ�������ʢװA��D����ۺ������Ũ��Һ
B. AE3��D2E2����������ԭ���������ﵽ8���ӽṹ
C. B��D��E�ĵ��ʻ��������ж�����������Ư��������
D. ��ҵ�Ϸֱ������ڵ�B��E��C��E�γɵĻ������Ʊ�B��C����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com