
【题目】Ⅰ. 由中科院等离子体物理研究所自主研制的全超导托卡马克实验装置(俗称“人造太阳”)正在接受技术升级。人造太阳是利用氘、氚核聚变反应释放巨大能量原理而实现的。下列说法正确的是________。
A.氕、氘、氚三种元素在周期表中的位置不同
B.20 g D2O含有的中子数为6.02×1024个
C.在隔绝空气和高温下LiCl与金属钠反应可获得金属锂
Ⅱ. 部分元素在周期表中的位置如下:
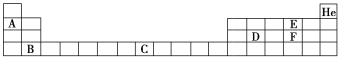
请回答下列问题:
(1)元素C在周期表中的位置为________。
(2)判断E和F对应的简单氢化物沸点高低,并解释原因____________。
(3)用电子式表示F的氢化物的形成过程:___________。
Ⅲ.溴及其化合物广泛用于医药、塑料阻燃剂等,苦卤提溴的工业流程如下:
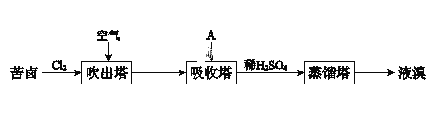
(1)结合元素周期律解释Cl的非金属性强于Br的原因:_______________。
(2)吸收塔中,A吸收了Br2后的溶液中含有Br和BrO3,则A是________(填序号)。
A.NaCl溶液 B.Na2CO3溶液 C.SO2气体
(3)从吸收塔出来的溶液中加入稀H2SO4得到Br2的离子方程式是______。
【答案】BC 第四周期Ⅷ族 H2O沸点高,水分子可形成分子间氢键作用力强,故沸点高 ![]() Cl和Br均为第ⅦA族元素,原子最外层电子数均为7,电子层数Cl<Br,原子半径Cl<Br,得电子能力Cl>Br,非金属性Cl>Br B 5Br+ BrO3 + 6H+ =3Br2 + 3H2O
Cl和Br均为第ⅦA族元素,原子最外层电子数均为7,电子层数Cl<Br,原子半径Cl<Br,得电子能力Cl>Br,非金属性Cl>Br B 5Br+ BrO3 + 6H+ =3Br2 + 3H2O
【解析】
A.氕、氘、氚三种元素为H的同位素,质子数相同;
B.D2O的摩尔质量为20g/mol,则20g D2O即1mol;
C.还原性:Na>Li,在隔绝空气和高温下LiCl与金属钠反应可获得金属锂;
Ⅱ.根据元素周期表的信息,A为Li,B为Ca,C为Fe,D为Si,E为O,F为S。
Ⅲ.苦卤中的溴离子与氯气反应生成溴,在吹出塔经热空气吹出溴蒸气,在吸收塔吸收,生成Br和BrO3,再与稀硫酸反应生成单质溴。
A.氕、氘、氚三种元素为H的同位素,质子数相同,则在周期表中的位置相同,A错误;
B.D2O的摩尔质量为20g/mol,则20g D2O即1mol,1mol D2O含有的中子的物质的量为10mol,所以1mol含有的中子数为6.02×1024个,B正确;
C.还原性:Na>Li,在隔绝空气和高温下LiCl与金属钠反应可获得金属锂,C正确;
答案为BC;
II.(1)元素C为Fe,位于第四周期Ⅷ族;
(2)E和F分别为O、S,氢化物为H2O、H2S,水分子间可形成氢键,导致分子间的作用力增大,熔沸点升高,则H2O沸点高;
(3)F的氢化物为H2S,电子式表示其形成过程为![]() ;
;
III.(1)Cl、Br属于同一主族,最外层均有7个电子,Cl原子核外有3个电子层,Br有4个电子层,则原子半径Cl<Br,原子核对核外电子的作用力Cl>Br,得电子能力Cl>Br,则非金属性:Cl>Br;
(2)Br2在碱性溶液中生成Br和BrO3,结合题中给定试剂,答案为B;
(3)Br和BrO3,在酸性条件下生成溴和水,反应的离子方程式为5Br+BrO3+6H+ =3Br2+ 3H2O。


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
【题目】如图所示甲是某学生验证铜和浓硝酸反应的装置,乙、丙是另外两位同学对甲装置改进后的装置:
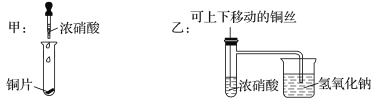
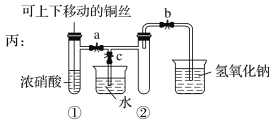
(1)甲、乙、丙三个装置中共同发生的反应的化学方程式是__________________________________。
(2)和甲装置相比,乙装置的优点是①______________________;②________________。
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置。实验时先关闭活塞________,再打开活塞________,才能使NO2气体充满②试管;当气体充满②试管后,将铜丝提起与溶液脱离。欲使烧杯中的水进入②试管,应该_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素a、b、c、d、e的原子序数依次增大。a的简单阴离子与锂离子具有相同的电子层结构,b原子最外层电子数等于内层电子数的2倍。d的单质与稀盐酸剧烈反应放出a2。在1L0.2mol·L-1a2e的水溶液中缓慢通入ec2气体,该溶液的pH与ec2气体体积(标准状况)的关系如图所示。下列说法不正确的是
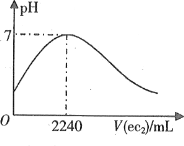
A.a和b可构成所有原子共平面的分子
B.在b、c、e的气态氢化物中,c的最稳定
C.d的氯化物一定能破坏水的电离平衡
D.e的最高价含氧酸与其氢化物可能发生氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为21。则下列说法不正确的是
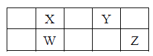
A. 原子半径大小:Y<XB. W的简单气态氢化物比X的稳定
C. Z的最高价氧化物对应的水化物是一种强酸D. W的氧化物可溶于烧碱溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有抗菌作用的白头翁素衍生物H的合成路线如下图所示:
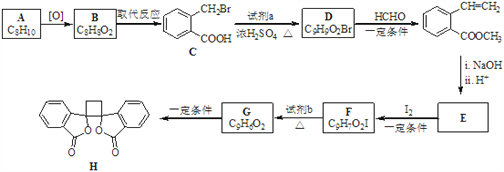
已知:i.RCH2Br ![]() R﹣HC═CH﹣R′
R﹣HC═CH﹣R′
ii.R﹣HC═CH﹣R′![]()
![]()
iii.R﹣HC═CH﹣R′![]()
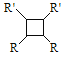
(以上R、R'、R'代表氢、烷基或芳基等)
(1)A属于芳香烃,其名称是_______________________。
(2)D的结构简式是_______________________________。
(3)由F生成G的反应类型是________________________________________。
(4)由E与I2在一定条件下反应生成F的化学方程式是_____________________;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是_______________________________。
(5)下列说法正确的是___________(选填字母序号)。
A. G存在顺反异构体
B. 由G生成H的反应是加成反应
C. 1 mol G最多可以与1 mol H2发生加成反应
D. 1 mol F或1 mol H与足量NaOH溶液反应,均消耗2 molNaOH
(6)以乙烯为起始原料,结合已知信息选用必要的无机试剂合成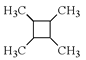 写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。___________________
写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一包白色粉末X,由BaCl2、K2SO4、CaCO3、NaOH、CuCl2、KCl中的一种或几种组成,为了探究其成分,进行了如下实验:
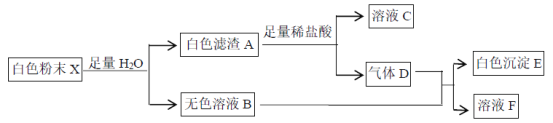
下列判断正确的是
A. 白色滤渣A可能为CaCO3、BaSO4的混合物
B. K2SO4、CuCl2一定不存在
C. KCl、K2SO4可能存在
D. CaCO3、BaCl2一定存在,NaOH可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】发射“神舟七号”载人飞船的是我国自行研制的“长征一号D”运载火箭。该火箭的主要燃料是偏二甲肼(用R表示)和四氧化二氮,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:![]() ,下列叙述错误的是( )
,下列叙述错误的是( )
A. 此反应是氧化还原反应
B. 反应瞬间产生大量高温气体,推动火箭飞行
C. 在此反应中![]() 作还原剂
作还原剂
D. R的分子式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将总物质的量为amol的钠和铝的混合物投入到水中,若两者的物质的量之比n(Na):n(Al)=2:3,则生成的氢气在标准状况下的体积为( )
A.11.24a LB.36.6a LC.17.92a LD.44.82a L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A是一种重要的化工原料,采用以下路线合成X。
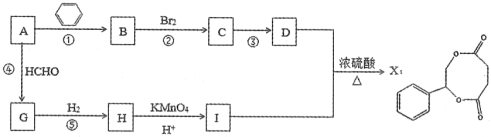
已知:RC≡CH+HCHO![]() RC≡CCH2OH
RC≡CCH2OH
请回答下列问题:
(1)若反应①、②、④的原子利用率均为100%,则A的名称为:_____。
(2)物质G的结构简式为:_____。
(3)写出反应③的化学反应方程式:______。
(4)物质E是物质D发生催化氧化后生成的有机产物,请写出E与银氨溶液反应的化学方程式:______。
(5)物质H和物质I可以在一定条件下合成链状聚合物,请写出化学方程式: ____。
(6)符合下列条件的D的同分异构体共有________种。
i.与FeCl3溶液能发生显色反应 ii.苯环上的一氯代物只有一种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com