
【题目】在同温同压下,下列各组热化学方程式中Q2 > Q1的是( )
A. 2H2(g)+O2(g)=2H2O(l) ΔH== -Q1 2H2(g)+O2(g)=2H2O(g) ΔH== - Q2
B. S(g)+O2(g)=SO2(g) ΔH== - Q1 S(s)+O2(g)=SO2(g) ΔH== - Q2
C. C(s)+![]() O2(g)=CO(g) ΔH== - Q1 C(s)+O2(g)=CO2(g) ΔH== - Q2
O2(g)=CO(g) ΔH== - Q1 C(s)+O2(g)=CO2(g) ΔH== - Q2
D. H2(g)+Cl2(g)=2HCl(g) ΔH== - Q1 ![]() H2(g)+
H2(g)+![]() Cl2(g)= HCl(g) ΔH== - Q2
Cl2(g)= HCl(g) ΔH== - Q2
 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
【题目】电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱。25℃时,有关物质的电离平衡常数如下表所示。根据该表,回答下列问题:
化学式 | HF | CH3COOH | H2SO3 | H2CO3 | H2S |
电离平衡 常数(Ka) | 4.0×10-4 | 1.8×10-5 | K1=1.54×10-2 K2=1.02×10-7 | K1=4.4×10-7 K2=4.7×10-11 | K1=9.1×10-8 K2=1.1×10-12 |
(1)同浓度的F-、CO32-、CH3COO-、HS-结合H+的能力最强的为__________
(2)溶液中不可能大量共存的离子组是__________
a.HS-、SO32- b.HF、CH3COO- c.HS-、HCO3- d. HSO3-、HCO3-
(3)Na2CO3溶液通入过量H2S的离子方程式是:_____。
(4)OH-浓度相同的等体积的两份溶液HCl(A)和 CH3COOH(E),分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是_______(填写序号)。
①反应所需要的时间E>A ②开始反应时的速率A>E
③参加反应的锌的物质的量A=E ④反应过程的平均速率E>A
⑤A溶液里有锌剩余 ⑥E溶液里有锌剩余
(5)向 0.l molL-1 CH3COOH溶液中滴加 NaOH 溶液至c(CH3COOH) : c(CH3COO-) =2 : 36,此时溶液pH = __________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应:mA(g) + nB(g)![]() pC(g) H= Q kJ·mol-1,在密闭容器中进行,右图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是
pC(g) H= Q kJ·mol-1,在密闭容器中进行,右图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是
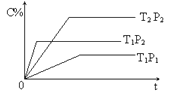
A. T1<T2 P1>P2 m+n<P Q<0B. T1>T2 P1<P2 m+n>P Q>0
C. T1<T2 P1<P2 m+n<P Q>0D. T1>T2 P1<P2 m+n>P Q<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组设计了下列装置,验证二氧化碳跟过氧化钠反应时需要与水接触。

(装置分析)
(1)装置①中反应的离子方程式是____________________________。
(2)装置②中的试剂是________(填序号)。
a.饱和NaHCO3溶液 b.饱和Na2CO3溶液 c.浓H2SO4
(3)装置③中的试剂是__________。
(进行实验)
步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(4)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是_____________。
(5)过氧化钠跟二氧化碳反应的化学方程式是______________________。
(实验反思)
(6)有同学提出质疑:“上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应。”其理由是______。
(7)需要补充的实验操作是:取⑤中反应后的少量固体,______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝自然形成的氧化膜易脱落。以硫酸为电解液,分别以石墨和铝材作阴、阳极材料,经过电解处理形成氧化铝膜,抗蚀能力强。其制备的简要流程如图所示。下列用来解释流程中反应的方程式不正确的是
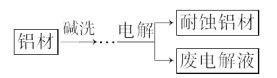
A. 碱洗目的是除去铝材表面的自然氧化膜:2OH-+Al2O3===2AlO2-+H2O
B. 碱洗时铝材表面会出现气泡:2Al+2OH-+2H2O===2AlO2-+3H2↑
C. 获得耐蚀铝材的电极反应:4Al-12e-+3O2===2Al2O3
D. 用稀氨水洗去耐蚀铝材表面的酸:NH3·H2O+H+===NH4++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲、乙、丙、丁四个烧杯中分别盛有100mL蒸馏水,然后分别放入等物质的量的Na、Na2O、Na2O2、NaOH,待固体完全溶解,则四个烧杯中溶液的质量分数的大小顺序为( )
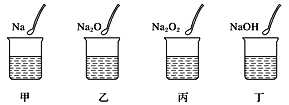
A.甲<乙<丙<丁B.丁<甲<乙=丙C.甲=丁<乙=丙D.丁<甲<乙<丙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由Zn、Cu、Al、Fe四种金属中的两种组成的混合物41.5g,与足量的盐酸反应产生的氢气在标况下为22.4升,则混合物中一定含有的金属是 ( )
A.ZnB.FeC.AlD.Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机反应方程式书写及其反应类型都正确的是( )
A. ![]()
![]()
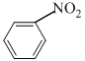 取代反应
取代反应
B. 2CH3CHO+O2![]() 2CH3COOH 氧化反应
2CH3COOH 氧化反应
C. CH2=CH2+Br2 → CH3CHBr2 加成反应
D. HCOOH+CH3CH2OH ![]() HCOOCH3CH2+H2O 酯化反应
HCOOCH3CH2+H2O 酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是制备和研究乙炔性质的实验装置图,有关说法不正确的是

A. 用蒸馏水替代a中饱和食盐水产生的乙炔更为纯净
B. c(过量)的作用是除去影响后续实验的杂质
C. d、e中溶液褪色的原理不同
D. f处产生明亮、伴有浓烟的火焰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com