
【题目】下列有机反应方程式书写及其反应类型都正确的是( )
A. ![]()
![]()
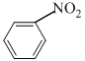 取代反应
取代反应
B. 2CH3CHO+O2![]() 2CH3COOH 氧化反应
2CH3COOH 氧化反应
C. CH2=CH2+Br2 → CH3CHBr2 加成反应
D. HCOOH+CH3CH2OH ![]() HCOOCH3CH2+H2O 酯化反应
HCOOCH3CH2+H2O 酯化反应
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】化学在生产和日常生活中有着重要的应用,下表中用途与其性质或原理对应关系不正确的是 ( )
选项 | 现象或事实 | 解释 |
A | Na2O2常用于潜水艇或呼吸面具的供氧剂 | Na2O2与H2O、CO2反应产生O2 |
B | 常用铝箔做包装材料 | 金属铝有好的延展性 |
C | FeCl3溶液可用于刻制印刷铜电路板 | FeCl3可与Cu发生反应 |
D | 烧菜用过的铁锅,经放置常出现红棕色斑迹 | 烧菜时铁锅被染色 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,下列各组热化学方程式中Q2 > Q1的是( )
A. 2H2(g)+O2(g)=2H2O(l) ΔH== -Q1 2H2(g)+O2(g)=2H2O(g) ΔH== - Q2
B. S(g)+O2(g)=SO2(g) ΔH== - Q1 S(s)+O2(g)=SO2(g) ΔH== - Q2
C. C(s)+![]() O2(g)=CO(g) ΔH== - Q1 C(s)+O2(g)=CO2(g) ΔH== - Q2
O2(g)=CO(g) ΔH== - Q1 C(s)+O2(g)=CO2(g) ΔH== - Q2
D. H2(g)+Cl2(g)=2HCl(g) ΔH== - Q1 ![]() H2(g)+
H2(g)+![]() Cl2(g)= HCl(g) ΔH== - Q2
Cl2(g)= HCl(g) ΔH== - Q2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:
CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.1
COS(g)+H2(g) K=0.1
反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是
A. 升高温度,H2S浓度增加,表明该反应是吸热反应
B. 通入CO后,正反应速率逐渐增大
C. 反应前H2S物质的量为7mol
D. CO的平衡转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学依据资料深入探究Fe3+在水溶液中的行为。
资料:i.Fe3+ 在水溶液中以水合铁离子的形式存在,如[Fe(H2O)6]3+;
[Fe(H2O)6]3+发生如下水解反应:
[Fe(H2O)6]3+(几乎无色)+nH2O![]() [Fe(H2O)6-n(OH)n]3-n(黄色)+nH3O+(n=0~6);
[Fe(H2O)6-n(OH)n]3-n(黄色)+nH3O+(n=0~6);
ii.[FeCl4(H2O)2]-为黄色。
【实验I】

【实验II】
分别用试管①、③中的试剂作为待测液,用色度计测定其透光率。透光率越小,溶液颜色越深;透光率越大,溶液颜色越浅。


图1 图2
Fe(NO3)3溶液透光率随温度变化曲线 FeCl3溶液透光率随温度变化曲线
(1)实验I中,试管②溶液变为无色的原因是 。
(2)实验I中,试管③溶液呈棕黄色与[FeCl4(H2O)2]-有关,支持此结论的实验现象是 。
(3)由实验II图1、2可知:加热时,溶液颜色 (填“变浅”、“变深”或“不变”)。
(4)由实验II,可以得出如下结论:
[结论一]FeCl3溶液中存在可逆反应:[FeCl4(H2O)2]-+4H2O![]() [Fe(H2O)6]3++4Cl-
[Fe(H2O)6]3++4Cl-
得出此结论的理由是 。
[结论二] 结论一中反应的ΔH (填“>0”或“<0”)。
(5)实验小组同学重新设计了一个实验证明(4)中结论一。实验方案:取试管①中溶液, (请描述必要的实验操作和现象)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的△H前者大于后者的是
①C(s)+O(g)=CO(g)ΔH1 ; C(s)+![]() O2(g)=CO(g) ΔH2
O2(g)=CO(g) ΔH2
②S(s)+O2 (g)=SO2 (g) ΔH3 ; S(g)+O2 (g)=SO2 (g) ΔH4
③H2(g)+ ![]() O2(g)=H2O(l) ΔH5;2H2(g)+O2(g)=2H2O(l) ΔH6
O2(g)=H2O(l) ΔH5;2H2(g)+O2(g)=2H2O(l) ΔH6
④CaCO3(s)=CaO(s)+CO2(g) ΔH7;CaO(s)+H2O(l)=Ca(OH)2(s) ΔH8
A. ①B. ④C. ②③④D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。下列说法正确的是


A.过程①中钛氧键断裂会释放能量
B.CO2分解反应的热化学方程式为2CO2(g)=2CO(g)+O2(g)ΔH=+30kJ/mol
C.使用TiO2作催化剂可以降低反应的焓变,从而提高化学反应速率
D.该反应中,光能和热能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验。
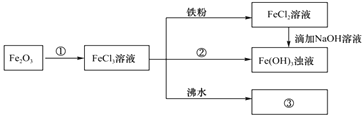
(1)请写出Fe2O3与①反应的离子方程式___。
(2)物质②可能为___。
(3)请写出FeCl3与铁粉反应的离子方程式___。
(4)向FeCl2溶液中滴加NaOH溶液,该过程的现象为___,过程中发生的氧化还原反应为(用化学方程式表达)___。
(5)将FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得分散系③___,提纯此分散系的方法叫___,它与FeCl3溶液、Fe(OH)3浊液的本质区别是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀废水中常含有阴离子A,排放前可加CuSO4溶液处理,使之转化为沉淀B,按如下流程进行实验。
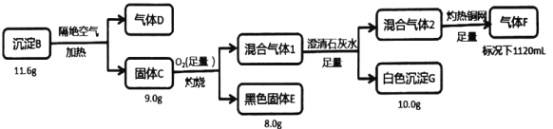
已知:B含三种元素;气体D标况下密度2.32g/L;混合气体l无色无味;气体F标况下密度为1.25g/L。请回答:
(1)组成B的三种元素是___,气体D的分子式是___。
(2)写出固体C在足量氧气中灼烧的方程式___。
(3)固体C在沸腾的稀盐酸中会生成一种弱酸和一种白色沉淀,该白色沉淀是共价化合物(测其分子量为199),则反应的化学方程式是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com