
【题目】金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。
(1)Ti基态原子的电子排布式为____________。
(2)Ti能与B、C、N、O等非金属元素形成稳定的化合物,B、C、N的电负性由大到小的顺序为_____;C、N、O的第一电离能由大到小的顺序为_____________。
(3)N的氢化物常作制冷剂,原因是______________。
(4)月球岩石—玄武岩的主要成分为钛酸亚铁(FeTiO3)。FeTiO3与80%的硫酸反应可生成TiOSO4。
SO42-的空间构型为_______形。其中硫原子采用_________杂化,写出SO42-的一种等电子体的化学式:______。
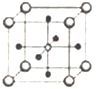
(5)Ti、Ca、O相互作用能形成如图晶体结构(Ti4+位于立方体的顶点、Ca2+位于立方体体心),该晶体的化学式为________。Ti4+和周围_____个O2-相紧邻。该晶胞的边长为apm,则其密度为______g/cm3。
【答案】 1s22s22p63s23p63d24s2 N>C>B N>O>C NH3分子键能形成氢键,沸点较高,以液化,故能够做制冷剂 正四面体 sp3 ClO4- CaTiO3 12 136/(6.02·a3)×107g/cm3
【解析】(1)Ti的原子核外有22个电子,根据电子的排布规律可知基态Ti原子的核外电子排布为1s22s22p63s23p63d24s2或[Ar]3d24s2;(2)根据元素电负性的比较,同周期中的元素,随核电荷数的增加,电负性增强,所以电负性N>C>B;第一电离能随核电荷数的增加而增大,但N的最外层的轨道是半充满状态,比较稳定,所以第一电离能N>O>C;(3)NH3分子间能形成氢键,沸点较高,易液化,故能够做制冷剂;(4)SO42-中的S原子的价层电子对数是![]() ,无孤对电子,所以硫酸根离子的空间构型是正四面体型;其中S采取的是sp3杂化;原子数和价电子数分别都相等的是等电子体,则SO42-的一种等电子体的化学式为ClO4-等。(5)Ti4+位于立方体的顶点,个数是8×1/8=1,Ca2+位于立方体体心,共计1个,氧原子位于面心处,个数6×1/2=3,因此该晶体的化学式为CaTiO3。每层的Ti4+都与4个O2-紧邻,所以该晶体中Ti4+和周围的12个O2-紧邻;该晶胞的边长为apm,则其晶胞的体积是(a×10-10cm)3,所以密度为
,无孤对电子,所以硫酸根离子的空间构型是正四面体型;其中S采取的是sp3杂化;原子数和价电子数分别都相等的是等电子体,则SO42-的一种等电子体的化学式为ClO4-等。(5)Ti4+位于立方体的顶点,个数是8×1/8=1,Ca2+位于立方体体心,共计1个,氧原子位于面心处,个数6×1/2=3,因此该晶体的化学式为CaTiO3。每层的Ti4+都与4个O2-紧邻,所以该晶体中Ti4+和周围的12个O2-紧邻;该晶胞的边长为apm,则其晶胞的体积是(a×10-10cm)3,所以密度为![]() g/cm3。
g/cm3。


科目:高中化学 来源: 题型:
【题目】下列实验能达到预期目的的是
A. 用溴水检验汽油中是否含有不饱和脂肪烃
B. 除去苯中混有的苯酚,加入浓溴水,过滤
C. 除去乙醇中混有的水,加入金属钠,蒸馏
D. 乙烷气体中混有乙烯, 通入酸性高锰酸钾溶液,洗气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学镀银法是非金属表面镀银的常用方法。下图是研究化学镀银中银元素利用率的实验装置(夹持仪器略):
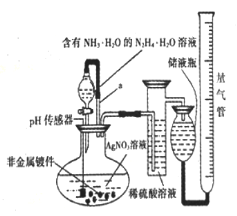
化学镀银中的反应如下:
I:4AgNO3+N2H4·H2O=4Ag↓+N2↑+4HNO3+H2O
Ⅱ:NH3·H2O + HNO3=NH4NO3+H2O
Ⅲ:Ag++2 NH3·H2O= [Ag(NH3)2]++2H2O
(1)写出N2H4的电子式______________。已知稀硝酸的氧化性强于Ag+,N2H4·H2O中加适量氨水的一个重要目的是控制溶液的pH在8~9之间。筒述溶液不能呈酸性的理由___________。
(2)带有导管a的分液漏斗叫恒压漏斗,下列关于恒压漏斗在该实验中的作用说法正确的是____(填选项字母)。
A.防止稀硫酸倒吸进入圆底烧瓶
B.使漏斗中液体顺利流下
C.减小加入液体体积对测量气体体积的误差
D.方便检验装置的气密性
(3)银膜是否均匀致密的关键在于“沉银”速率控制,一般速率越慢,银膜越均匀越致密。简述加入氨水的另外一个目的________。
(4)未被还原的Ag+占总银元素质量比(ψ1)叫非还原损耗,被还原但是没有在镀件上附着沉淀的银占总银元素质量比(ψ2)叫还原损耗。实验中用200 mL 0.100 mol/L AgNO3溶液,加过量的N2H4·H2O,测得相关数据如下:
I:非金属镀件镀前质量为20. 000克,镀后质量(已清洗干燥)为21. 728克;
Ⅱ:量气管收集到的气体折算标准状况体积为106. 400 mL。
则ψ1= __________;ψ2=____________。
(5)化学镀银中常用次磷酸钠(NaH2PO2)做还原剂,已知该反应的氧化产物为磷酸,写出该反应的离子反应方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化铈(CeO2)是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。

已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
(1)稀酸A的分子式是_____________________。
(2)滤液1中加入H2O2溶液的目的是__________________。
(3)设计实验证明滤液1中含有Fe2+_____________________。
(4)已知Fe2+溶液可以和难溶于水的FeO(OH)反应生成Fe3O4,书写该反应的离子方程式____________。
(5)由滤液2生成Ce(OH)4的离子方程式__________________。
(6)硫酸铁铵晶体[Fe2(SO4)3·2(NH4)2SO4·3H2O]广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是___________________。
(7)取上述流程中得到的Ce(OH)4产品0.531 g,加硫酸溶解后,用浓度为0.l000mol·L-1FeSO 4标准溶液滴定至终点时(铈被还原为Ce3+ ),消耗25.00 mL标准溶液。该产品中Ce(OH)4的质置分数为_______(结果保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】游离态的氮经一系列转化可以得到硝酸,如下图所示。

(1)NH3和O2在催化剂作用下反应,其化学方程式是______________。
(2)NO2→HNO3反应中氧化剂和还原剂的物质的量之比为________________。
(3)2NO(g)+O2(g) ![]() 2NO2(g)是制造硝酸的重要反应之一。在800℃时,向容积为1L的密闭容器中充入0.010molNO和0.005molO2,反应过程中NO的浓度随时间变化如下图所示。
2NO2(g)是制造硝酸的重要反应之一。在800℃时,向容积为1L的密闭容器中充入0.010molNO和0.005molO2,反应过程中NO的浓度随时间变化如下图所示。

①2min内,v(O2)=________mol/(L·min)
②800℃时,该反应的化学平衡常数为__________。
③判断该反应达到平衡的依据是(写出2条即可)____________。
④已知:ⅰ.
ⅱ.N2(g)+2O2(g)=2NO2(g) ΔH=+68kJ·mol-1,写出NO生成NO2热化学方程式_____________,温度对于NO生成NO2平衡转化率的影响是:___________________。
(4)电解法处理含氮氧化物废气,可以回收硝酸。实验室模拟电解法吸收NO,装置如图所示(均为石墨电极)。请写出电极过程中NO转化为硝酸的电极反应式:______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的四种短周期元素,A、B、C、D、F是由其中的两种或三种元素组成的化合物,E是由Z元素形成的单质,0.1molL-1 D溶液的pH为13(25℃)。它们满足如图转化关系,则下列说法正确的是

A. 由X、Y、Z、W四种元素组成的盐溶液pH小于7
B. 化合物F中含有共价键和离子键
C. 0.1molB与足量C完全反应共转移电子数为0.2NA
D. Z元素的最高正价为+6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N、S对应的化合物,是重要的化学物质。试回答下列问题:
(1)已知:氢气的燃烧热为286.0kJ/mol,氨气的燃烧热为382.5 kJ/mol ,则合成氨反应的热化学方程式
为_____________________。
(2)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理。已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,则另一反应的离子方程式为________________。
(3)用活性炭还原法处理氮氧化物。 有关反应为C(s)+2NO(g) ![]() N2(g)+CO2(g)。
N2(g)+CO2(g)。
某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T)条件下反应,反应进行到不同时间测得各物质的浓度如表:
时间(min) 浓度(molL-1) | NO | N2 | CO2 |
0 | 1.00 | 0 | 0 |
10 | 0.58 | 0.21 | 0.21 |
20 | 0.40 | 0.30 | 0.30 |
30 | 0.40 | 0.30 | 0.30 |
40 | 0.32 | 0.34 | 0.17 |
50 | 0.32 | 0.34 | 0.17 |
①10min~20min以v(CO2)表示的反应速率为_________________。
②根据表中数据,计算T℃时该反应的平衡常数为Kp=___________,(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,保留两位小数)
③一定温度下,随着NO的起始浓度增大,则NO的平衡转化率_________(填“增大”“不变”或“减小”)。
④该反应达到平衡时下列说法正确的是______填序号字母)。
a.容器内压强保持不变 b.2v(NO)=v(N2)
c.容器内CO2的体积分数不变 d.混合气体的密度保持不变
⑤30min时改变某一条件,过一段时间反应重新达到平衡,则改变的条件可能是______。请在图中画出30~40min的变化曲线______。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com