
【题目】根据所学知识,回答下列问题:
(1)现有下列物质;①熔融的NaCl ②液态HCl ③蔗糖 ④汞 ⑤NaOH溶液 ⑥稀硫酸 ⑦CO2 ⑧KCl晶体
其中属于电解质的是__________;属于非电解质的是__________;能导电的有__________。
(2)按要求填空。
①NaHSO4溶液(写出电离方程式)____________________________。
②氯水与KI溶液反应(写出离子方程式)_____________________________。
③苏打和澄清石灰水反应(写出离子方程式)_______________________________
(3)配平下列氧化还原方程式:
①_____Fe+_____HNO3 = _____Fe(NO3)3+_____NO↑+_____H2O
②____CO+____ Fe2O3 ![]() ____Fe+_____CO2
____Fe+_____CO2
【答案】 ①②⑧ ③⑦ ①④⑤⑥ NaHSO4 = Na++H++ SO42- Cl2 +2 I - = I2 + 2Cl - CO32-+Ca2+=CaCO3↓ 1 , 4,1 ,1,2 3,1, 2,3
【解析】试题分析:本题考查电解质和非电解质的判断,电离方程式和离子方程式的书写,氧化还原反应方程式的配平。
(1)①熔融的NaCl是能导电的化合物,属于电解质;②液态HCl中只有HCl分子,不能导电,但其水溶液能导电,液态HCl属于电解质;③蔗糖不能导电,蔗糖溶于水和熔融时都不能导电,蔗糖属于非电解质;④汞能导电,汞属于单质,既不是电解质也不是非电解质;⑤NaOH溶液能导电,NaOH溶液属于混合物,既不是电解质也不是非电解质;⑥稀硫酸能导电,稀硫酸属于混合物,既不是电解质也不是非电解质;⑦CO2不能导电,虽然CO2的水溶液能导电,但导电的离子不是CO2电离产生的,CO2属于非电解质;⑧KCl晶体中阴、阳离子不自由移动,不能导电,KCl晶体溶于水和熔融时都能导电,KCl晶体属于电解质;属于电解质的是①②⑧;属于非电解质的是③⑦;能导电的有①④⑤⑥。
(2)①NaHSO4属于强酸的酸式盐,在水溶液中的电离方程式为NaHSO4=Na++H++SO42-。
②氯水与KI反应的化学方程式为:Cl2+2KI=2KCl+I2,Cl2、I2都不改写,KI、KCl都改成离子,则离子方程式为:Cl2+2I-=2Cl-+I2。
③苏打和澄清石灰水反应的化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,Na2CO3、Ca(OH)2、NaOH都改写成离子,CaCO3难溶于水以化学式保留,则离子方程式为:Ca2++CO32-=CaCO3↓。
(3)①Fe元素的化合价由0价升至Fe(NO3)3中的+3价,升高3价,N元素的化合价由HNO3中的+5价降至NO中的+2价,降低3价,根据元素化合价升降总数相等配平:1Fe+1HNO3→1Fe(NO3)3+1NO↑+H2O;观察Fe(NO3)3中N元素的化合价与HNO3中N元素的化合价一致,根据原子守恒调整HNO3的化学计量数,进而确定H2O的化学计量数,配平为:1Fe+4HNO3=1Fe(NO3)3+1NO↑+2H2O。
②C元素的化合价由CO中的+2价升至CO2中的+4价,升高2价,Fe元素的化合价由Fe2O3中的+3价降至0价,降低3价,根据元素化合价升降总数相等配平:3CO+Fe2O3![]() 2Fe+3CO2。
2Fe+3CO2。


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
【题目】下列各组离子能在溶液中大量共存的是
A. K+、Cu2+、NH4+、OH- B. Na+、SO42-、K+、Cl-
C. Na+、H+、Fe2+、NO3- D. Ba2+、Na+、OH-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备氯气(Cl2)的化学方程式如下:4HCl(浓) + MnO2 ![]() MnCl2 + Cl2↑ +2 H2O
MnCl2 + Cl2↑ +2 H2O
(1)用单线桥表示出电子转移的方向和数目________________________,
(2)将题干中反应改写成离子方程式是___________________________。
(3)在上述过程中,被氧化的元素是_________,还原产物是___________,氧化剂和还原剂的物质的量之比为:__________;该反应中盐酸体现的性质为:__________________
(4)若反应中产生0.5 molCl2,则转移的电子数目为_____,被氧化的HCl的物质的量___mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)按如图所示操作,充分反应后:
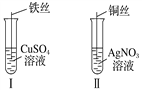
①Ⅰ中铁丝上观察到的现象是______________________;
②Ⅱ中发生反应的离子方程式为_______________________;
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_____________。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热。
①写出制备氢氧化铁胶体的化学方程式____________________.
②向氢氧化铁胶体中逐滴滴入过量盐酸,出现的实验现象为:___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【衡水中学2017年高考押题卷】利用H2和O2制备H2O2的原理为
① H2(g)+ A(1)![]() B(1) ΔH1 ②O2(g)+B(1)
B(1) ΔH1 ②O2(g)+B(1)![]() A(1)+ H2O2(1) ΔH2
A(1)+ H2O2(1) ΔH2
巳知:A、B均为有机物,两个反应均能自发进行,下列说法正确的是
A.ΔH2>0
B.B为H2和O2制备H2O2的催化剂
C.反应①的正反应的活化能大于逆反应的活化能
D.H2(g)+O2(g)![]() H2O2(1) 的ΔH <0
H2O2(1) 的ΔH <0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.写出下列反应的离子方程式:
(1)将鸡蛋壳在醋酸中溶解有气泡产生:______________________________________;
(2)CuSO4溶液与Ba(OH)2溶液混合:________________________________________。
(3)铁片插入硝酸银溶液中:_________________________________________________。
Ⅱ.对一份稀溶液作初步分析后发现,溶液无色、澄清,其可能含有![]() 、Na+、
、Na+、![]() 、H+、
、H+、![]() 、
、![]() 、Cl等离子中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl等离子中的若干种。然后又作了如下分析,以确定这些离子是否存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2 mL溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(1)原溶液中一定存在的离子是__________,一定不存在的离子是____________。
(2)在上述实验操作中,有错误的步骤是_________(填代号)。对该错误改正的方法是(要作较详细的说明)_________________________________________________________。
(3)到目前为止,不能肯定在原溶液中是否存在的离子是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【哈师大附中2017届第四次模拟考试】常温下,在pH=1的某溶液中可能有Na+、Fe3+、Fe2+、I-、Cl- 、CO32-中的几种,现取100mL该溶液进行如下实验。根据实验结果,下列判断正确的是

A.Fe2+、I-、Cl-三种离子一定存在
B.CO32-一定不存在,不能确定Na+和Cl-是否存在
C.Fe3+与Fe2+至少有一种
D.该溶液中c(Cl-)至少为0.2molL1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌—空气电池是金属空气电池的一种,电解质溶液为KOH溶液时,反应为:2Zn+O2+4OH-+2H2O=2Zn(OH)42-。下列有关说法正确的是
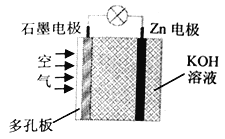
A. 石墨电极上发生氧化反应 B. 正极附近溶液的pH不断减小
C. OH-由锌电极移向石墨电极 D. Zn 电极上发生反应:Zn-2e-+4OH-=Zn(OH)42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com