
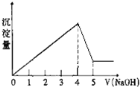
【题目】有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量之比为( )
A. 1:1B. 2:1C. 3:1D. 1:2
【答案】D
【解析】
氢氧化钠的体积为0~4时,发生的反应有:Al3++3OH-=Al(OH)3↓,Mg2++2OH-=Mg(OH)2↓,氢氧化钠的体积为4~5时发生的反应为:Al(OH)3+NaOH=NaAlO2+2H2O,假设氢氧化铝溶解消耗氢氧化钠为1mol,则沉淀最大时消耗NaOH为4mol,结合方程式计算n[Al(OH)3],进而计算n[Mg(OH)2],由原子守恒知n(A1)=n[Al(OH)3],n(Mg)=n[Mg(OH)2].
氢氢化钠的体积为0~4时,发生的反应有:Al3++3OH-=Al(OH)3↓,Mg2++2OH-=Mg(OH)2↓,氢氢化钠的体积为4~5时,发生的反应为:Al(OH)3+NaOH=NaAlO2+2H2O,假设氢氢化铝溶解消耗氢氢化钠为1mol,则沉淀最大时消耗NaOH为4mol,由Al(OH)3+NaOH=NaAlO2+2H2O可知,n [Al(OH)3]=n[NaOH]=1mol ,根据Al3++3OH-=Al(OH)3↓知生成氢氢化镁沉淀消耗NaOH为4mol-3mol=1mol,由Mg2++2OH-=Mg(OH)2↓,可知[Mg(OH)2]=0.5mol,由原子守恒知n(A1)=n[Al(OH)3]=1mol,n(Mg)=n[Mg(OH)2]=0.5mol,故原合金中镁、铝物质的量之比为0.5mol:1mol=1:2,故本题选D。


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
【题目】实验室欲探究CO还原CuO,设计如图所示装置(夹持装置略去)。下列说法正确的是
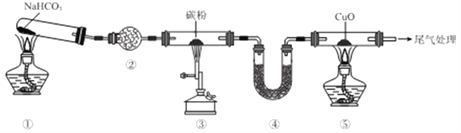
A. ②、④中均可盛装碱石灰
B. 加热的顺序为③、①、⑤
C. ①、③、⑤中均发生氧化还原反应
D. 可将尾气用导管通入到⑤的酒精灯处灼烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
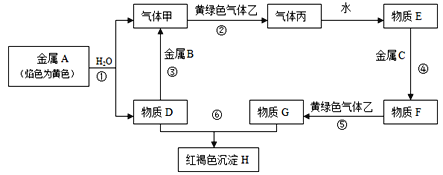
请回答下列问题:
(1)写出下列物质的化学式:B_____________, C_______________,F_____________, 乙_______________,
(2)写出下列反应的离子方程式:反应①____________________;反应⑤____________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光电池在光照条件下可产生电流,如图装置可以实现光能源的充分利用,双极性膜可将水解离为H+和OH-,并实现其定向通过。下列说法不正确的是( )
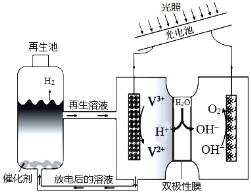
A.该装置可利用光能实现水的分解
B.光照过程中阴、阳极区溶液中的pH均基本不变
C.再生池中的反应为2V2++2H+![]() 2V3++H2↑
2V3++H2↑
D.每有1molOH-通过双极性膜,可产生5.6L(标准状况)的O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳元素在无机物和有机物中均充当了重要的角色,请回答下列问题:
(1)基态碳原子的价层电子排布图(轨道表达式)为__,其电子占据的能量最高的原子轨道的形状为__;C、N、O三种元素第一电离能最大的是__。
(2)有机物![]() 中碳原子的轨道杂化类型为__,分子中两种碳碳单键长的大小关系为①__②(填“>”、“<”或“=”)。
中碳原子的轨道杂化类型为__,分子中两种碳碳单键长的大小关系为①__②(填“>”、“<”或“=”)。
(3)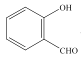 和
和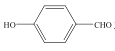 均可以形成氢键,则沸点较高的是__,原因是__。
均可以形成氢键,则沸点较高的是__,原因是__。
(4)石墨的结构及晶胞如图一所示,则石墨的密度为__g·cm-3(用含a、d、NA的表达式表示)。A的原子坐标为(![]() 、
、![]() 、0),则B的原子坐标为__。
、0),则B的原子坐标为__。
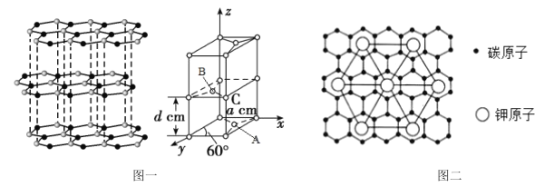
(5)石墨能与熔融的金属K作用,形成一种青铜色的化合物CxK,如图二所示,则x=__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2NO(g)+Br2(g)![]() 2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
①NO(g)+Br2(g)![]() NOBr2(g) 快 ②NO(g)+NOBr2(g)
NOBr2(g) 快 ②NO(g)+NOBr2(g)![]() 2NOBr(g) 慢
2NOBr(g) 慢
下列有关该反应的说法正确的是( )
A. 该反应的速率主要取决于①的快慢
B. NOBr2是该反应的催化剂
C. 正反应的活化能比逆反应的活化能小a kJ·mol-1
D. 增大Br2(g)浓度能增大活化分子百分数, 加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁的氧化物粉末可能含有FeO、Fe2O3中的一种或两种。某化学兴趣小组为验证该氧化物粉末的组成,做了如下实验:
(1)甲同学利用1mol/L的硫酸、KSCN溶液、酸性高锰酸钾溶液来确定其组成
编号 | 实验操作 | 实验现象与结论 |
① | 取少量粉末放入试管中,注入1mol/L的硫酸 | 粉末逐渐溶解,溶液呈黄绿色 |
② | 将①中所得溶液分成两份,向其中一份滴加几滴__________,振荡 | 若溶液________ ,说明有Fe2O3存在 |
③ | 向另一份溶液中加入少量__________,振荡 | 若溶液________ ,说明有FeO存在 |
(2)乙同学称取30.4g固体,按以下步骤进行实验:
步骤一 将固体置于烧杯中,加入1mol/L的硫酸将固体完全溶解
步骤二 往烧杯中先加入足量的氯水,充分反应后再加入足量的氢氧化钠溶液
步骤三 将步骤二所得的物质过滤洗涤后,灼烧至固体质量不再变化,得到32g红棕色固体
①步骤二中加入氯水的目的是__________________________________________;
②步骤三中沉淀洗涤的操作为__________________________________________;
③原固体中FeO和Fe2O3的物质的量之比为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室探究SO2与Fe(NO3)3溶液反应的原理,装置如下图,实验中Y装置产生白色沉淀。下列说法不正确的是
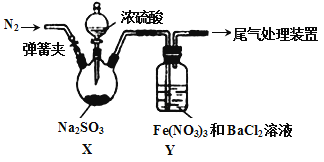
A. 滴加浓硫酸之前应进行的操作是打开弹簧夹,通入一段时间N2
B. Y中产生的白色沉淀是BaSO4或BaSO3
C. 产生白色沉淀的原因可能是在酸性条件下SO2与NO3- 反应生成了SO42-
D. 若将Fe(NO3)3换成FeCl3,Y中也能产生白色沉淀,说明Fe3+也能将SO2氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)是重要的能源物质,其制备、应用与转化是研究的热点。
(1) 利用合成气制备二甲醚主要包含三个反应:
CO(g)+2H2(g)=CH3OH(g);ΔH=-90.4 kJ·mol-1
2CH3OH(g)=CH3OCH3(g)+H2O(g);ΔH=-23.4 kJ·mol-1
CO(g) +H2O(g)=H2(g)+CO2(g);ΔH=-41.0 kJ·mol-1
则3CO(g)+3H2(g)=CH3OCH3(g)+CO2(g);ΔH=________。
(2) 某二甲醚/双氧水燃料电池的工作原理如图1所示。电池工作时,电极A附近溶液pH________(填“减小”“增大”或“不变”);电极B的电极反应式为_____________。

(3) 二甲醚催化羰化制备乙醇主要涉及以下两个反应:
反应Ⅰ:CO(g)+CH3OCH3(g)=CH3COOCH3(g);ΔH1
反应Ⅱ:CH3COOCH3(g)+2H2(g)=CH3CH2OH(g)+CH3OH(g);ΔH2
反应Ⅰ、Ⅱ的平衡常数的对数lg K1、lg K2与温度的关系如图2所示;在固定CO、CH3OCH3、H2的原料比、体系压强不变的条件下,同时发生反应Ⅰ、Ⅱ,平衡时各物质的物质的量分数随温度的变化如图3所示。
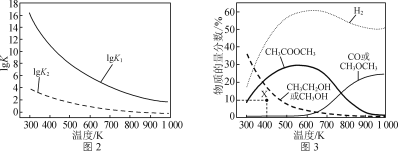
① ΔH1________(填“>”“<”或“=”)0。
②300~400 K时,CH3CH2OH物质的量分数随温度升高而降低的原因是________。
③ 600~700 K时,CH3COOCH3物质的量分数随温度升高而降低的原因是________。
④ 400 K时,在催化剂作用下,反应一段时间后,测得CH3CH2OH物质的量分数为10%(图3中X点)。不改变原料比、温度和压强,一定能提高CH3CH2OH物质的量分数的措施有________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com