
利用下列实验装置进行的相应实验,不能达到实验目的的是

A.图1所示装置可制取氨气
B.图2所示装置可分离CH3CH2OH和CH3COOC2H5混合液
C.图3所示装置可制备Fe(OH)2并容易观察到白色沉淀
D.图4所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂自性、还原性
科目:高中化学 来源:2014-2015吉林省吉林市高一上学期期末考试化学试卷(解析版) 题型:选择题
为了检验某固体物质中是否含有NH4+,下列组合正确的是
①蒸馏水 ②NaOH溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀硫酸
A.①③ B.④⑤ C.①②③ D.①④⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省青岛市高三上学期期末考试化学试卷(解析版) 题型:填空题
(17分)二甲醚是一种重要的清洁燃料。合成二甲醚是解决能源危机的研究方向之一。
(1)用CO2和H2可以合成二甲醚(CH3OCH3)

(2)已知在一定温度下,以下三个反应的平衡常数为k1、k2、k3:
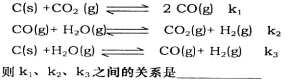
(3)二甲醚(CH3OCH3)燃料电池可以提升能量利用率。利用二甲醚酸性介质燃料电池电解100mL 1mo1 的食盐水(惰性电极),电解一段时间后,收集到标况下的氢气2.24L(设电解后溶液体积不变)
的食盐水(惰性电极),电解一段时间后,收集到标况下的氢气2.24L(设电解后溶液体积不变)
①二甲醚燃料电池的负极反应式为_____________。
②电解后溶液的PH=_________________________
(4)工业合成氨的反应为: mol-1
mol-1
已知合成氨反应在某温度下2L的密闭绝热容器中进行,测得数据如下表:

根据表中数据计算:
①0 min~1 min内N2的平均反应速率为_________
②该条件下反应的平衡常数k=________(保留两位小数)
③反应达到平衡后,若往平衡体系中再加入N2、H2、NH3各1mol,化学平衡向_______(填“正向”、“逆向”或“不移动”),该反应的平衡常数k___________(填“变大”“减小”或“不变”)
(5)常温下,将0.2mol HCOOH和0.1mol
HCOOH和0.1mol NaOH溶液等体积混合,所得溶液的PH<7,说明HCOOH的电离程度____________HCOONa的水解程度(填“大于”或“小于”)。该溶液中[HCOOH]-[OH-]+[H+]=______mol
NaOH溶液等体积混合,所得溶液的PH<7,说明HCOOH的电离程度____________HCOONa的水解程度(填“大于”或“小于”)。该溶液中[HCOOH]-[OH-]+[H+]=______mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省青岛市高三上学期期末考试化学试卷(解析版) 题型:选择题
下列对应化学反应的离子方程式正确的是
A.KIO3与KI在酸性溶液中反应:
B.向碳酸氢铵溶液中加过量氢氧化钠溶液并加热:
C.将过量二氧化硫通入稀氨水中:
D.用稀硝酸洗涤试管内壁的银镜:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省青岛市高三上学期期末考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.1mol氯气参加氧化还原反应,转移的电子数一定为2NA
B.25℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.02NA
C.12 g石墨和C60的混合物中质子总数一定为6NA个
D.常温常压下,22.4L乙烯中C—H键数为4NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省莱芜市高三1月月考化学试卷(解析版) 题型:选择题
关于下列各装置图的叙述中,正确的是

A.装置①阳极有红色物质析出
B.装置②的总反应为Cu+2Fe3+=Cu2++2Fe2+
C.装置③中a为负极,发生的电极反应式为H2+2OH-—2e-=2H2O
D.用装置④精炼铜,则a极为纯铜,电解质溶液可为CuSO4溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期12月月考理综化学试卷(解析版) 题型:填空题
(12分)【化学——化学与技术】
化工厂的设计是将实验室的研究成果转化为工业化生产的重要的基础工作。
(1)以硫铁矿为原料生产硫酸需经过 、 和 三个主要生产阶段。
(2)侯氏制碱法是在索尔维制碱法的基础上创造出的一种新的制造纯碱的方法。具体工艺流程图如下:

①索尔维制碱法的原理是 。(用化学方程式表示)
②侯氏制碱法与索尔维制碱法相比,优点是 。
③侯氏制碱法可以循环使用的物质有 。
(3)食盐也是一种重要的化工原料,氯碱工业就是通过电解饱和食盐水来制备NaOH、H2和C12。海水中得到的粗盐中往往含有一些杂质,必须加入一些化学试剂,使杂质沉淀,处理后的盐水还需进入阳离子交换塔,其原因是 。电解食盐水在离子交换膜电解槽中进行,离子交换膜的作用是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高二上学期期末化学试卷(解析版) 题型:选择题
下图甲和乙是双液原电池装置。由图可判断下列说法错误的是

A.甲图电池反应的离子方程式为:Cd(s)+Co2+(aq)===Co(s)+Cd2+(aq)
B.2Ag(s)+Cd2+(aq)===Cd(s)+2Ag+(aq)反应能够发生
C.盐桥的作用是形成闭合回路,并使两边溶液保持电中性
D.乙图当有1 mol电子通过外电路时,正极有108 g Ag析出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com