
【题目】(1)25°C时,若向a mol·L-1的HA溶液中,滴加等体积的b mol·L-1的NaOH溶液,使溶液呈中性,用含a的代数式表示HA的电离平衡常数Ka=____________。
(2)25°C时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应完后溶液中c(NH4+)=c(Cl-),则溶液显_____性(填“酸”、“碱”或“中”),用含a的代数式表示NH3·H2O的电离平衡常数Kb=____________。
【答案】![]() 中
中 ![]()
【解析】
(1)25°C向a mol·L-1的HA溶液中,滴加等体积的b mol·L-1的NaOH溶液后,溶液中存在电荷守恒c(H+)+c(Na+)= c(OH-)+c(A-),由于溶液呈中性,,则c(A-)= c(Na+)=0.5b mol·L-1;所以电离平衡常数![]() =
=![]() ;
;
(2)25°C时,将氨水与盐酸等体积混合,反应完后溶液中c(NH4+)=c(Cl-),根据溶液中电荷守恒c(H+)+c(NH4+)=c(Cl-)+c(OH-),则溶液显中性;c(OH-)=10-7mol·L-1 ,c(NH4+)=0.005 mol·L-1,由物料守恒可知c(NH3·H2O)=0.5a-0.005 mol·L-1,则NH3·H2O的电离平衡常数 =
=![]() 。
。


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】如图所示,直线交点处的圆圈为NaCl晶体中Na+或Cl-所处的位置。这两种离子在空间三个互相垂直的方向上都是等距离排列的。

(1)请将其中代表Na+的圆圈涂黑(不必考虑体积大小),以完成NaCl晶体的结构示意图_____________。
(2)在晶体中,每个Na+的周围与它最接近且距离相等的Na+共有________个。
(3)晶体中每一个重复的结构单元叫晶胞。在NaCl晶胞中正六面体的顶角上、面上、棱上的Na+或Cl-为该晶胞与其相邻的晶胞所共有,一个晶胞中Cl-的个数等于________,即________(填计算式);Na+的个数等于________,即________(填计算式)。
(4)设NaCl的摩尔质量为M g/mol,食盐晶体的密度为ρ g/cm3,阿伏加德罗常数为NA,食盐晶体中两个距离最近的钠离子间的距离为________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜类化合物广泛存在于动植物体内,关于下列萜类化合物的说法正确的是

A.a和b都属于芳香烃
B.a和c分子中所有碳原子均处于同一平面上
C.在一定条件a、b和c均能与氢气发生加成反应
D.b和c均能与新制Cu(OH)2悬浊液反应生成砖红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高血脂是一种常见的心血管疾病,治疗高血脂的新药I的合成路线如下(A~I)均为有机物):

已知:a. 
b.  RCHO
RCHO
回答下列问题:
(1)反应①的化学方程式为_______;F的官能团名称为______。
(2)反应②的类型是_______。D→E所需试剂、条件分别是_______、______。
(3)G的结构简式为____________。
(4)芳香族化合物W的化学式为C8H8O2, 且满足下列条件的W的结构共有_______种(不考虑立体异构)。
i.遇FeCl3溶液显紫色; ii.能发生银镜反应。
其中核磁共振氢谱显示有5种不司化学环境的氢,峰面积比为2:2:2:1:1的是____________(写出结构简式)。
(5)设计以甲苯和乙醛为原料制备 的合成路线。无机试剂任选,合成路线的表示方式为:
的合成路线。无机试剂任选,合成路线的表示方式为:![]() _____________.
_____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)0.1 mol/L醋酸溶液中,存在电离平衡CH3COOH![]() H++CH3COO-。经测定溶液中c(CH3COO―)为1.4×10-3 mol/L,此温度下醋酸的电离平衡常数Ka=________。
H++CH3COO-。经测定溶液中c(CH3COO―)为1.4×10-3 mol/L,此温度下醋酸的电离平衡常数Ka=________。
(2)已知饱和硫化氢的浓度为0.1 mol/L,硫化氢的电离常数为Ka1=1.0×10-7,Ka2=1.0×10-19,计算饱和硫化氢溶液中氢离子的浓度为__________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】曲美替尼是一种抑制黑色素瘤的新型抗癌药物,下面是合成曲美替尼中间体G的反应路线:
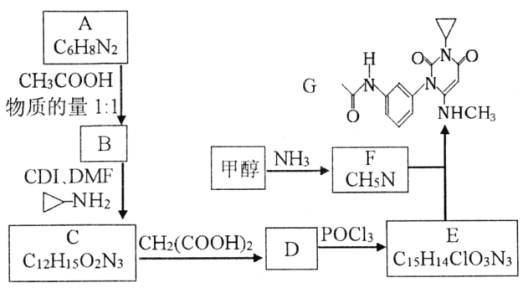
已知:①D分子中有2个6元环;
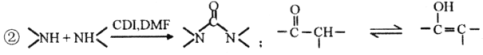
请回答:
(1)化合物A的结构简式___________。A生成B的反应类型___________。
(2)下列说法不正确的是___________。
A.B既能表现碱性又能表现酸性
B.1moC在碱溶液中完全水解最多可以消耗4 molOH-
C.D与POCl3的反应还会生成E的一种同分异构体
D.G的分子式为C16H18O3N4
(3)写出C→D的化学方程式____________________________________________。
(4)X是比A多2个碳原子的A的同系物,写出符合下列条件的X可能的结构简式:_______________________________________________________。
①1H-NMR谱显示分子中有3种氢原子,②IR谱显示分子中有苯环与-NH2相连结构
(5)流程中使用的DMF即N,N-二甲基甲酰胺结构简式为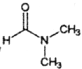 ,是常用的有机溶剂。设计以甲醇和氨为主要原料制取DMF的合成路线(用流程图表示,其他无机试剂任选)。_____________
,是常用的有机溶剂。设计以甲醇和氨为主要原料制取DMF的合成路线(用流程图表示,其他无机试剂任选)。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列关于电解质溶液中的比值问题说法正确的是
A.pH=11的NaOH和pH=3CH3COOH等体积混合:![]() <1
<1
B.向Ba(OH)2和氨水的混合液中加入盐酸:![]() 增大
增大
C.向CaCO3和CaSO4的悬浊液中加入少量Na2CO3固体:![]() 增大
增大
D.向CH3COONa溶液中加水稀释:![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不能用平衡移动原理解释的是( )
A.新制氯水中加入CaCO3固体可增大HClO分子的浓度
B.钢铁在潮湿的空气中比在干燥空气中更容易生锈
C.通入过量的空气与SO2反应可以提高SO2的利用率
D.由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组利用以下装置电解饱和食盐水,同时测定电解时产生的氢气的体积和检验氯气的氧化性。

(1)所选仪器连接时,各接口的顺序是(填各接口的代号字母):A 接_____,_____接_____,B接_____,_______接_____________。
(2)实验时用石墨和铁为电极,则铁电极接电源的_____极,所发生的电极反应式为_____。
(3)实验测得产生的氢气体积(已折算成标准状况)为 5.60 mL,电解后溶液的体积恰好为 50.0 mL,则溶液中 OH-的浓度为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com