
| ||
| ||


科目:高中化学 来源: 题型:
| A、雾 |
| B、氢氧化铁胶体 |
| C、石灰乳 |
| D、KNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 性质 | 与NaOH溶液 | 与银氨溶液 | 与钠 |
| A | 水解 | 不产生银镜 | 不反应 |
| B | 中和 | 不产生银镜 | 产生H2 |
| C | 水解 | 产生银镜 | 不反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
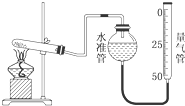 某学生利用高锰酸钾分解制氧气的反应,测定室温下的气体摩尔体积,实验装置如图所示.部分实验步骤:①装好实验装置.②…③把适量的高锰酸钾粉末放入干燥的试管中,准确称量试管和高锰酸钾粉末的质量为a g.④加热,开始反应,直到产生一定量的气体.⑤停止加热.⑥测量收集到的气体的体积.⑦准确称量试管和残留物的质量为b g.⑧测量实验室的温度.回答下列问题.
某学生利用高锰酸钾分解制氧气的反应,测定室温下的气体摩尔体积,实验装置如图所示.部分实验步骤:①装好实验装置.②…③把适量的高锰酸钾粉末放入干燥的试管中,准确称量试管和高锰酸钾粉末的质量为a g.④加热,开始反应,直到产生一定量的气体.⑤停止加热.⑥测量收集到的气体的体积.⑦准确称量试管和残留物的质量为b g.⑧测量实验室的温度.回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)一定条件下,发生反应CO(g)+H2O(g)?CO2(g)+H2(g),向2L密闭容器中通入2mol CO(g)、1mol H2O(g),2min后反应达到平衡时,测得CO的物质的量为1.6mol,用H2O (g)表示该反应速率为
(1)一定条件下,发生反应CO(g)+H2O(g)?CO2(g)+H2(g),向2L密闭容器中通入2mol CO(g)、1mol H2O(g),2min后反应达到平衡时,测得CO的物质的量为1.6mol,用H2O (g)表示该反应速率为查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com