
【题目】V L浓度为0.5 mol·L-1的盐酸,欲使其浓度增大1倍,采取的措施合理的是( )
A.通入标准状况下的HCl气体11.2V L
B.加入10 mol·L-1的盐酸0.1V L,再稀释至1.5V L
C.将溶液加热浓缩到0.5V L
D.加入V L 1.5 mol·L-1的盐酸混合均匀
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】
(1)1.5molCO2的质量是,在标准状况下的体积为,所含氧原子的数目为。(2)现有质量比为11:14的CO2和CO的混合气体,则该混合气体中的CO2和CO物质的量之比为,碳原子和氧原子的个数比为,该混合气体的摩尔质量为。(3)向10mLNa2CO3和Na2SO4的混合溶液中加入足量的氯化钡溶液,生成沉淀的质量为6.27g,向所得沉淀中加入足量稀盐酸,沉淀质量减少到2.33g,并放出气体,试计算:
原混合物中Na2SO4的物质的量浓度;
在标准状况下产生气体的体积。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种。现利用另一种溶液X,用如下图所示的方法即可将它们确定。

试确定A,B,C,D,X各代表何种溶液。
A:___________B:___________C:___________D:___________X:___________
写出加过量的A产生白色沉淀的化学方程式:_________________________________。
写出加过量的C产生白色沉淀的化学方程式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Fe(OH)3和Al(OH)3沉淀的生成与溶解的量如下表。

向FeCl3、Al2(SO4)3的混合溶液中逐有加入Ba(OH)2溶液,形成沉淀的情况如下图所示.以下推断错误的是

A.AB段可能发生的反应:2Ba2++3OH-+2SO42-+Al3+=2BaSO4↓+Al(OH)3↓
B.C点对应的沉淀:Fe(OH)3和BaSO4
C.OA段可能发生的反应:3Ba2++6OH-+3SO42-+Al3++Fe3+=3BaSO4↓+Fe(OH)3↓+Al(OH)3↓
D.据图计算原溶液中:c(Cl-)=c(SO42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】综合题:
氢气是清洁的能源,也是重要的化工原料,根据以下三种制氢方法。完成下列问题:
(1)方法一:H2S热分解法,反应式为:2H2S(g)![]() 2H2(g)+S2(g)△H
2H2(g)+S2(g)△H
在恒容密闭容器中,测定H2S分解的转化率(H2S的起始浓度均为cmol/L),测定结果见下图,图中曲线a表示H2S的平衡转化率与温度关系,曲线b表示不同温度下反应经过相同时间未达到化学平衡时H2S的转化率。
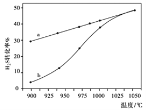
①△H0,(“>”、“<”或“=”)。
②若985℃时,反应经tmin达到平衡,此时H2S的转化率为40%,则tmin内反应速率v(H2)=
(用含c、t的代数式表示)。
③请说明随温度的升高,曲线b向曲线a接近的原因:。
(2)方法二:以CaO为吸收体,将生物材质(以C计)与水蒸气反应制取H2。相关主要反应如下:
I:C(s)+H2O(g)═CO(g)+H2(g)△H=+131.0kJ/mol
Ⅱ:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-43kJ/mol
Ⅲ:CaO(s)+CO2(g)═CaCO3(s)△H=-178.3kJ/mol
①计算反应C(s)+2H2O(g)+CaO(s)![]() CaCO3(s)+2H2(g)的△H=kJ/mol;
CaCO3(s)+2H2(g)的△H=kJ/mol;
若K1、K2、K3分别为反应I、Ⅱ、Ⅲ的平衡常数,该平衡常数K=(用K1、K2、K3表示)。
②对于可逆反应C(s)+2H2O(g)+CaO(s)![]() CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是。(填字母)
CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是。(填字母)
A.降低体系的温度
B.压缩容器的体积
C.增加CaO的量
D.选用适当的催化剂
(3)方法三:利用甲醇可以与水蒸气反应制取H2,反应方程式如下:
CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g)△H=+49.4kJ/mol
CO2(g)+3H2(g)△H=+49.4kJ/mol
一定温度下,向容积为2L的密闭恒容容器中充入1molCH3OH(g)和3molH2O(g),达到平衡状态时,吸收热量19.76kJ。则
①达平衡时混合气体的压强是反应前的倍。
②此温度下的该反应的平衡常数是(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是
A.2mol水和1mol水的摩尔质量
B.1mol·L-1CaCl2溶液与2mol·L-1KCl溶液中Cl-的物质的量
C.50Ml.1mol·L-1MgCl2溶液与100Ml.1mol·L-1NaCl溶液中Cl-物质的量浓度
D.20%NaOH溶液与10%NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下所示(用于沉淀的试剂稍过量):
![]()
(1)检验粗盐中存在SO42-的方法是(用化学方程式表示)_______________,第①步操作的名称是______________。
(2)第④步中加入试剂的化学式为_____________________。
(3)第⑦步操作所需要玻璃仪器的名称是___________。
(4)若⑤步、第⑥步顺序颠倒,将对实验结果产生影响,其原因是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)3.6gH2O物质的量为______mol,约含有_________个原子。
(2)已知1.204×1023个X气体的质量是6.4g。则X气体的摩尔质量是______。
(3)2molNH3与_________L(标准状况)CH4所含氢原子数目相同。
(4)同温同压下,同体积的甲烷(CH4)和CO2分子数之比为________,物质的量之比_______,原子总数之比_________,质量之比为________,密度之比_________。
(5)VLAl2(SO4)溶液中含Al3+amol,溶液的物质的量浓度为__________,取出V/2L再加入水稀释到4VL。则稀释后溶液中SO42-的物质的量浓度是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com