
����Ŀ���ۺ��⣺
������������Դ��Ҳ����Ҫ�Ļ���ԭ�ϣ����������������ⷽ��������������⣺
��1������һ��H2S�ȷֽⷨ����ӦʽΪ��2H2S��g��![]() 2H2��g��+S2��g����H
2H2��g��+S2��g����H
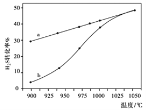
�ں����ܱ����������ⶨH2S�ֽ��ת������H2S����ʼŨ�Ⱦ�Ϊcmol/L�����ⶨ�������ͼ��ͼ������a��ʾH2S��ƽ��ת�������¶ȹ�ϵ������b��ʾ��ͬ�¶��·�Ӧ������ͬʱ��δ�ﵽ��ѧƽ��ʱH2S��ת���ʡ�
�١�H0��������������������=������
����985��ʱ����Ӧ��tmin�ﵽƽ�⣬��ʱH2S��ת����Ϊ40%����tmin�ڷ�Ӧ����v��H2��=
���ú�c��t�Ĵ���ʽ��ʾ����
����˵�����¶ȵ����ߣ�����b������a�ӽ���ԭ��
��2������������CaOΪ�����壬�������������C������ˮ������Ӧ��ȡH2�������Ҫ��Ӧ���£�
I��C��s��+H2O��g���TCO��g��+H2��g����H=+131.0kJ/mol
��CO��g��+H2O��g���TCO2��g��+H2��g����H=-43kJ/mol
��CaO��s��+CO2��g���TCaCO3��s����H=-178.3kJ/mol
�����㷴ӦC��s��+2H2O��g��+CaO��s��![]() CaCO3��s��+2H2��g������H=kJ/mol��
CaCO3��s��+2H2��g������H=kJ/mol��
��K1��K2��K3�ֱ�Ϊ��ӦI����������ƽ�ⳣ������ƽ�ⳣ��K=����K1��K2��K3��ʾ����
�����ڿ��淴ӦC��s��+2H2O��g��+CaO��s��![]() CaCO3��s��+2H2��g������ȡ���´�ʩ�������H2���ʵ��ǡ�������ĸ��
CaCO3��s��+2H2��g������ȡ���´�ʩ�������H2���ʵ��ǡ�������ĸ��
A��������ϵ���¶�
B��ѹ�����������
C������CaO����
D��ѡ���ʵ��Ĵ���
��3�������������ü״�������ˮ������Ӧ��ȡH2����Ӧ����ʽ���£�
CH3OH��g��+H2O��g��![]() CO2��g��+3H2��g����H��+49.4kJ/mol
CO2��g��+3H2��g����H��+49.4kJ/mol
һ���¶��������ݻ�Ϊ2L���ܱպ��������г���1molCH3OH��g����3molH2O��g�����ﵽƽ��״̬ʱ����������19.76kJ����
����ƽ��ʱ��������ѹǿ�Ƿ�Ӧǰ�ı���
�����¶��µĸ÷�Ӧ��ƽ�ⳣ������������λ��Ч��������
���𰸡���1��������![]() mol/��L��min�������¶����ߣ���Ӧ���ʼӿ죬�ﵽƽ������ʱ�����̣���2��-90.3��K1��K2��K3����A��
mol/��L��min�������¶����ߣ���Ӧ���ʼӿ죬�ﵽƽ������ʱ�����̣���2��-90.3��K1��K2��K3����A��
��3����1.2��0.11mol2/L2
��������
�����������1������ͼ���֪���¶����ߣ�ת����������ƽ�����ƣ�����������Ϊ���ȷ�����H��0��
��H2S����ʼŨ�Ⱦ�ΪcmolL-1����985��ʱ����Ӧ��tmin�ﵽƽ�⣬��ʱH2S��ת����Ϊ40%����μӷ�Ӧ������ΪcmolL-1��40%��0.4cmolL-1��v����c�¡�t��0.4c/tmol��L��1��min��1��
�������¶����ߣ���Ӧ�����ӿ죬�ﵽƽ������ʱ�����̣���������b������a�ƽ���
��2������֪��
I��C��s��+H2O��g���TCO��g��+H2��g����H=+131.0kJ/mol
��CO��g��+H2O��g���TCO2��g��+H2��g����H=-43kJ/mol
��CaO��s��+CO2��g���TCaCO3��s����H=-178.3kJ/mol
����ݸ�˹���ɿ�֪I+��+�����õ���ӦC��s��+2H2O��g��+CaO��s��![]() CaCO3��s��+2H2��g����H��-90.3kJ/mol��ƽ�ⳣ��K��K1K2K3��
CaCO3��s��+2H2��g����H��-90.3kJ/mol��ƽ�ⳣ��K��K1K2K3��
�����H2����������ʹƽ�������ƶ�����֪C��s��+2H2O��g��+CaO��s��![]() CaCO3��s��+2H2��g���ġ�H��-87.9kJmol-1��A���÷�ӦΪ���ȷ�Ӧ��������ϵ���¶ȣ�ƽ�����ƣ��������H2������A��ȷ��B���÷�Ӧǰ������������䣬ʹ���������Ũ�Ⱦ��ӱ�����ѹǿ����ƽ�ⲻ�ƶ�������H2�������䣬B����C������CaO��������ƽ����Ӱ�죬����H2�������䣬C������D���������ܸı�ƽ��״̬��D����ѡA��
CaCO3��s��+2H2��g���ġ�H��-87.9kJmol-1��A���÷�ӦΪ���ȷ�Ӧ��������ϵ���¶ȣ�ƽ�����ƣ��������H2������A��ȷ��B���÷�Ӧǰ������������䣬ʹ���������Ũ�Ⱦ��ӱ�����ѹǿ����ƽ�ⲻ�ƶ�������H2�������䣬B����C������CaO��������ƽ����Ӱ�죬����H2�������䣬C������D���������ܸı�ƽ��״̬��D����ѡA��
��3���ﵽƽ��״̬ʱ����������19.76kJ��������Ȼ�ѧ����ʽ��֪���ļ״������ʵ�����19.76kJ��49.4kJ/mol��0.4mol����
CH3OH��g��+H2O��g��![]() CO2��g��+3H2��g��
CO2��g��+3H2��g��
��ʼ����mol��1300
ת������mol��0.40.40.41.2
ƽ������mol��0.62.60.41.2
ƽ��Ũ����mol/L��0.31.30.20.6
����ƽ��ʱ��������ѹǿ�Ƿ�Ӧǰ��![]() ����
����
�����¶��µĸ÷�Ӧ��ƽ�ⳣ��K��![]() ��0.11mol2/L2��
��0.11mol2/L2��


 99��1������ĩ��ѵ��ϵ�д�
99��1������ĩ��ѵ��ϵ�д� ��ǿ��У��ĩ���100��ϵ�д�
��ǿ��У��ĩ���100��ϵ�д� �óɼ�1��1��ĩ���100��ϵ�д�
�óɼ�1��1��ĩ���100��ϵ�д� ��״Ԫ���źþ�ϵ�д�
��״Ԫ���źþ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧϰ�������ļ����ʱ��ij��ѧС����ʵ���ҷ���һƿ���Լ�ƿ����һЩ��ɫ�������ʡ��κ�ͬѧ�Ƕ���ƿʯ��ˮ�Ƿ���ʽ�����̽����
���������ݼ�ͬѧ��Ϊ��ʯ��ˮ��ȫ���ʣ���ͬѧ��Ϊ��ʯ��ˮ���ֱ��ʣ�
��ͬѧ��Ϊ��____________��
��ʵ�鷽����

�۷��������ۣ�
���ͨ��������������Ϊ�������ͬѧ�IJ���Ҳ��ȷ����ƿ�İ�ɫ����������____________(�ѧʽ)���������ԭ����(�û�ѧ����ʽ��ʾ)____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������������������������ȵ��ǣ� ��
A ��H3O+��OH�� B��CO��N2 C��NH3�� F�� D��CH4��NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤��������ֵ�������й�˵������ȷ����
A�������£�48gO3���е���ԭ����3NA
B����״���£�33.6LCO�к��е�ԭ������3NA
C��0.5mol��L-1CaCl3��Һ�к�Cl-��ĿΪNA
D��17gNH3�����ĵ�����Ϊ10NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��V LŨ��Ϊ0.5 mol��L��1�����ᣬ��ʹ��Ũ������1������ȡ�Ĵ�ʩ��������( )
A��ͨ���״���µ�HCl����11.2V L
B������10 mol��L��1������0.1V L����ϡ����1.5V L
C������Һ����Ũ����0.5V L
D������V L 1.5 mol��L��1�������Ͼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽΪC5H11Cl��ͬ���칹�干�У������������칹��
A��6�� B��7�� C��8�� D��9��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijҺ̬����������Է�������Ϊ106������ӽṹ�к���һ���������������ֽṹ��ͬ���칹�干�У� ��
A. 2�� B. 5�� C. 4�� D. 3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
(1)����240mL0.1mol/L��������Һ,Ӧ��ȡ������� mL,ʵ�����õ������������ձ�������������Ͳ��У�
(2)����ʱ������ȷ�IJ���˳����(��ĸ��ʾ��ÿ����ĸֻ����һ��) ��
A����30mLˮϴ���ձ�2��3�Σ�ϴ��Һ��ע������ƿ����
B������Ͳ��ȷ��ȡ�����Ũ�����������ز����������ձ��У��ټ�������ˮ(Լ30mL)���ò���������������ʹ���Ͼ���
C��������ȴ�������ز�����ע������ƿ��
D��������ƿ�ǽ�����ҡ��
E�����ý�ͷ�ιܼ�ˮ��ʹ��Һ����ǡ����̶�������
F������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶�1��2cm��
(3)�����ƹ����У�����ʵ�������ʹ�����Ƶ�ϡ��������ʵ���Ũ��ƫ�ߵ���________
A��ҡ�Ⱥ��ã�����Һ����ڿ̶��ߣ�������ˮ����̶�������
B����ȡŨ����ʱ���Ӷ���
C������ʱ����
D��������ǰ����֪Ũ�ȵ�ϡ������ϴ����ƿ
E��ϴ����ȡŨ�������Ͳ������ϴ��Һһ��ת���ձ���
F����Һû�лָ������¾ͽ��ж���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����

A����ͼ�ɱ�ʾˮ�ֽ�����е������仯
B����2C(s)+O2(g)=2CO(g) ��=��221.0kJ/mol����̼��ȼ����Ϊ110.5kJ/mol
C����Ҫ���ȵķ�Ӧһ�������ȷ�Ӧ���������ܷ����ķ�Ӧһ���Ƿ��ȷ�Ӧ
D����֪I����ӦH2(g)+Cl2(g)=2HCl(g) ��=��akJ/mol
II�� ![]()
��a��b��c�������㣬��Ͽ�1mol H��Cl�����������Ϊ����a��b��c��kJ/mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com