
【题目】下列离子方程式能用来解释相应实验现象的是 ( )
A.向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解:![]()
B.向沸水中滴加饱和氯化铁溶液得到红褐色液体:![]()
C.二氧化硫使酸性高锰酸钾溶液褪色:![]()
D.用铜做电极电解NaCl溶液: 2Cl﹣+2H2O![]() H2↑+Cl2↑+2OH﹣
H2↑+Cl2↑+2OH﹣
【答案】A
【解析】
A.向氢氧化镁悬浊液中滴加氯化铵溶液,反应生成氯化镁和一水合氨,氢氧化镁沉淀溶解,该反应的离子方程式为:Mg(OH)2+2NH4+═Mg2++2NH3H2O,故A正确;
B.向沸水中滴加饱和氯化铁溶液得到红褐色液体,说明反应生成氢氧化铁胶体,正确的离子方程为:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+,故B错误;
Fe(OH)3(胶体)+3H+,故B错误;
C.二氧化硫与酸性高锰酸钾溶液发生氧化还原反应,正确的离子方程式为:5SO2+2H2O+2MnO4-═5SO42-+2Mn2++4H+,故C错误;
D.用铜做电极电解NaCl溶液时,阳极上Cu失电子发生氧化反应,离子方程式为Cu+2H2O![]() Cu(OH)2↓+H2↑,故D错误;
Cu(OH)2↓+H2↑,故D错误;
故答案为A。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案科目:高中化学 来源: 题型:
【题目】国际计量大会第26次会议新修订了阿伏加德罗常数(Na = 6. 022214076×l023mol-1),并于2019年5月20日正式生效。下列说法不正确的是
A. 标准状况下11. 2 L的CH3Cl中含有氢原子的数目为1. 5NA
B. lmol Na2O2固体中含有阴、阳离子的总数目为3NA
C. l00mL lmolL-1 NH4Cl溶液中含有阳离子的数目大于0.1 NA
D. 18gD2O和H2O的混合物中含有的中子数为9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水化学资源开发利用的部分过程如图所示,下列说法正确的是( )
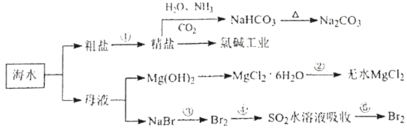
A.用澄清的石灰水可鉴别NaHCO3和Na2CO3
B.从海水中得到粗盐主要是通过蒸发操作实现的
C.在步骤③,中可通入Cl2使溴离子被还原为Br2
D.在步骤④中,SO2水溶液吸收Br2后,溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为中学化学中几种常见物质的转化关系(部分产物已略去)。已知:A、C、D是常见的气体单质,F气体极易溶于水,且液态常做制冷剂。
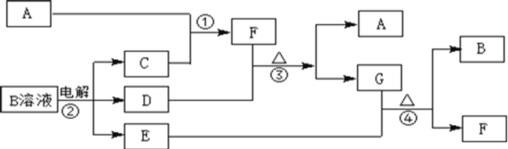
(1)写出化学式A_______,D_________,F_______;
(2)鉴定G中阳离子的实验方法和现象_____________________________;
(3)D单质和E溶液反应,生成一种常见的消毒剂和漂白剂的有效成分,写出D+E溶液反应的离子方程式和③的化学方程式_________、_______。
(4)常温下,电解B溶液制得pH = 12的烧碱溶液1000mL则反应中转移的电子数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 时,用
时,用![]() 二元弱酸
二元弱酸![]() 溶液滴定
溶液滴定![]() 溶液所得滴定曲线如图。下列说法不正确的是
溶液所得滴定曲线如图。下列说法不正确的是![]()
![]()

A.点![]() 所示溶液中:
所示溶液中:![]()
B.点![]() 所示溶液中:
所示溶液中:![]()
C.点![]() 所示溶液中:
所示溶液中:![]()
D.滴定过程中可能出现:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物1是一种常见的植物两味油,常用脂肪烃A和芳香烃D按如下路线合成:

已知:①R1CHO+R2CH2CHO![]()

![]()

②通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
回答下列问题:
(1)A的名称是___,H含有的官能团名称是_____。
(2)②的反应条件是___。⑦的反应类型是______。
(3)I的结构简式是________。
(4)④的化学方程式是_________。
(5)L是I的同分异构体且含有相同官能团,其结构中苯环上只有两个处于对位的取代基,则L共有_种(不考虑立体异构)
(6)参照以上合成路线,设计以C为原料制备保水树脂 的合成路线(无机试剂任选)__ 。
的合成路线(无机试剂任选)__ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A.由图1所示曲线可知,化学催化比酶催化的效果好
B.在H2S溶液导电性实验中,由图2所示曲线可确定通入的气体X可能是SO2,不可能为Cl2
C.在其它条件不变时,2SO2(g)+ O2(g)![]() 2SO3(g)转化关系(图3)中,纵坐标表示O2的转化率
2SO3(g)转化关系(图3)中,纵坐标表示O2的转化率
D.图4是用0.l000 mol/L的盐酸滴定20.00 mL 0.l000mol/LNa2CO3溶液的曲线,从a→b点反应的离子方程式为:CO32--+2H+=CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上电解NO制备NH4NO3,其工作原理如图所示(图中电极均为石墨电极)。下列说法错误的是

A. a 极连接电源的负极
B. 阳极反应为NO+5e-+6H+=NH4++H2O
C. 总反应方程式为8NO+7H2O![]() 3NH4NO3+2HNO3
3NH4NO3+2HNO3
D. 为使电解产物全部转化为NH4NO3,需补充物质A,A 是NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO与CO在金属铑(Rh)的催化下发生反应2NO(g)+CO(g)=N2O(g)+CO2(g) ΔH,该反应过程经历如下两步:
反应Ⅰ:NO(g)+CO(g)+Rh(s)=RhN(s)+CO2(g) ΔH1=-33.44 kJ·mol-1;
反应Ⅱ:RhN(s)+NO(g)=Rh(s)+N2O ΔH2=-319.35 kJ·mol-1。
如图所示为该反应在无催化剂(a)和有催化剂(b)时反应过程的能量变化对比图:

下列有关判断正确的是( )
A.ΔH=-285.91 kJ·mol-1
B.E1为反应2NO(g)+CO(g)=N2O(g)+CO2(g)的活化能
C.E2为使用催化剂后降低的活化能
D.使用合适的催化剂可降低反应的活化能,提高反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com