
【题目】常温下,在丙酮-盐酸混合溶液中,Fe3+比Cu2+的溶解度更大,用该溶液作展开剂分离Fe3+ 和Cu2+的装置如右图。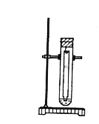
以下叙述错误的是
A.该方法为径向纸上层析法B.试样点晾干后才能补滴
C.试样点不能接触展开剂D.可喷KSCN溶液检验分离出来的Fe3+
科目:高中化学 来源: 题型:
【题目】生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)①上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Cu原子的核外电子排布式:______。
②铜的一种氧化物晶胞中(结构如图所示),所包含的Cu原子数目为______。
③其中O原子的配位数为______。
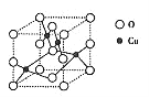
(2)根据等电子原理,写出CO分子的结构式______。
(3)甲醇催化氧化可得到甲醛(HCHO),甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇沸点比甲醛高得多的原因是______。
②甲醇分子中原子轨道的杂化类型为sp3的原子个数为______。
③甲醛分子的空间构型是______;1mol甲醛分子中σ键的数目为______。
④甲醇中C、H、O三种元素电负性由大到小的顺序为______。
⑤Cu2O的熔点比Cu2S高的原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应:K2Cr2O7 + 14HCl → 2KCl + 2CrCl3 + 3Cl2↑+ 7H2O ,若有0.1mol K2Cr2O7参加反应,下列说法正确的是( )
A.被氧化的HCl为51.1molB.转移电子1.806×1023个
C.氧化产物为7.3gD.还原剂占参加反应HCl的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物对环境具有显著影响。
(1)已知汽车气缸中氮及其化合物发生如下反应:
N2(g)+O2(g)![]() 2NO(g) △H=+180 kJ/mol
2NO(g) △H=+180 kJ/mol
N2(g)+2O2(g)![]() 2NO2(g) △H=+68 kJ/mol
2NO2(g) △H=+68 kJ/mol
则 2NO(g)+O2(g)![]() 2NO2(g) △H=__________ kJ/mol
2NO2(g) △H=__________ kJ/mol
(2)对于反应2NO(g)+O2(g)![]() 2NO2(g)的反应历程如下:
2NO2(g)的反应历程如下:
第一步:2NO(g)![]() N2O2(g)(快速平衡)
N2O2(g)(快速平衡)
第二步:N2O2(g)+O2(g)![]() 2NO(g)(慢反应)
2NO(g)(慢反应)
其中可近似认为第二步反应不影响第一步的平衡,第一步反应中:υ正=k1 正·c2(NO),υ 逆=k1 逆·c(N2O2),k1正、k1 逆为速率常数,仅受温度影响。下列叙述正确的是__________
A. 整个反应的速率由第一步反应速率决定
B. 同一温度下,平衡时第一步反应的![]() 越大,反应正向程度越大
越大,反应正向程度越大
C. 第二步反应速率慢,因而平衡转化率也低
D. 第二步反应的活化能比第一步反应的活化能高
(3)在密闭容器中充入一定量的CO和NO气体,发生反应2CO(g)+2NO(g)![]() 2CO2(g)+N2(g) △H<0,图为平衡时NO的体积分数与温度、压强的关系:
2CO2(g)+N2(g) △H<0,图为平衡时NO的体积分数与温度、压强的关系:
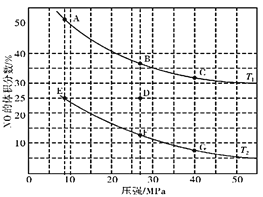
①温度:T1__________T2(填“>”、“<”或“=”)。
②若在D点对反应容器升温,同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中A~G点中的__________点(填字母)。
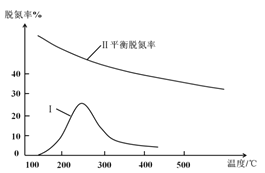
③某研究小组探究该反应中催化剂对脱氮率(即NO转化率)的影响。将相同量的NO和CO 以一定的流速分别通过催化剂a和b,相同时间内测定尾气,a结果如图中曲线I所示。已知:催化效率 b>a;b的活性温度约450℃。在图中画出b所对应的曲线(从300℃开始画) _______。
(4)在汽车的排气管上加装催化转化装置可减少NOx的排放。研究表明,NOx的脱除率除与还原剂、催化剂相关外,还取决于催化剂表面氧缺位的密集程度。以La0.8A0.2BCoO3+X(A、B 均为过渡元素)为催化剂,用H2还原NO的机理如下:
第一阶段:B4+(不稳定)+H2→低价态的金属离子(还原前后催化剂中金属原子的个数不变)
第二阶段:I . NO(g)+□→NO(a)
II . 2NO(a)→2N(a)+O2(g) III. 2N(a)→N2(g)+2□
IV. 2NO(a)→N2(g)+2O(a) V. 2O(a)→O2(g)+2□
注:□表示催化剂表面的氧缺位,g表示气态,a表示吸附态
第一阶段用氢气还原 B4+得到低价态的金属离子越多,第二阶段反应的速率越快,原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚乙烯醇肉桂酸酯(M)可用作光刻工艺中的抗腐蚀涂层,其合成路线如图:
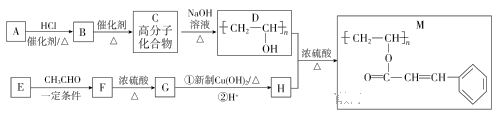
已知:R1—CHO+R2—CH2CHO![]()
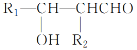 。
。
请回答:
(1)C的化学名称为__;M中含氧官能团的名称为__。
(2)F→G的反应类型为__。
(3)C→D的化学反应方程式为___。
(4)E能与新制的Cu(OH)2反应,该反应的化学方程式是__。
(5)关于H的性质下列说法正确的是__(填字母)。
a.存在顺反异构
b.溶液呈酸性,能与Na和NaOH溶液反应
c.能使KMnO4(H+)溶液和Br2(CCl4)溶液褪色
d.能发生银镜反应、酯化反应、加成反应和消去反应
(6)符合下列条件的F的同分异构体有__种。
①属于芳香族化合物 ②能与NaHCO3反应放出CO2
其中核磁共振氢谱有4种吸收峰的物质的结构简式为__(任写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是
A.加入合金的质量可能为6.4g
B.参加反应的硝酸的物质的量为0.1mol
C.沉淀完全时消耗NaOH溶液的体积为150mL
D.溶解合金时收集到NO气体的体积为2.24L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知硝酸与金属反应时,在不同条件下有不同的还原产物,甚至在同一反应中可同时得到多种还原产物。现有HNO3、NH4NO3、N2O、H2O、Zn、Zn(NO3)2六种物质。
(1)请利用其中五种物质组成一个完整的化学反应,写出该化学反应方程式:
________________________________________________________________;
(2)上述所写反应中,硝酸表现出的化学性质是_____,被还原的元素是_______。
(3)若六种物质组成一个完整的化学反应,则反应中的还原产物是______(填化学式),若该反应中NH4NO3与N2O物质的量之比为1︰1,那么该反应中氧化剂与还原剂的物质的量之比为____________。
(4)若六种物质组成一个完整的化学反应,且没有对该反应中的某些物质的比例作限定,则方程式可能的配平系数有许多组。原因是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科技的进步,合理利用资源、保护环境成为当今社会关注的焦点。甲胺铅碘(CH3NH3PbI3)用作全固态钙钛矿敏化太阳能电池的敏化剂,可由CH3NH2、PbI2及HI为原料合成,回答下列问题:
(1)制取甲胺的反应为CH3OH(g)+NH3(g) ![]() CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
共价键 | C-O | H-O | N-H | C-N |
键能/kJ·mol-1 | 351 | 463 | 393 | 293 |
则该反应的ΔH=_______。
(2)上述反应中所需的甲醇工业上利用水煤气合成,反应为CO(g)+2H2(g) ![]() CH3OH(g) ΔH<0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
CH3OH(g) ΔH<0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:

①平衡时,M点CH3OH的体积分数为10%,则CO的转化率为________。
②X轴上a点的数值比b点________(填“大”或“小”)。某同学认为上图中Y轴表示温度,你认为他判断的理由是_____________________。
(3)实验室可由四氧化三铅和氢碘酸反应制备难溶的PbI2,则每生成3 mol PbI2的反应中,转移电子的物质的量为__________。
(4)常温下,PbI2饱和溶液(呈黄色)中c(Pb2+)=1.0×10-3mol·L-1,则Ksp(PbI2)=_________;已知Ksp(PbCl2)=1.6×10-5,则转化反应PbCl2(s)+2I-(aq) ![]() PbI2(s)+2Cl-(aq)的平衡常数K=_________。
PbI2(s)+2Cl-(aq)的平衡常数K=_________。
(5)分解HI曲线和液相法制备HI反应曲线分别如图1和图2所示:

①反应H2(g)+I2(g) =2HI(g) 的ΔH__________(填大于或小于)0。
②将二氧化硫通入碘水中会发生反应:SO2+I2+2H2O=3H++HSO4-+2I-,I2+I-![]() I3-,图2中曲线a、b分别代表的微粒是________、_________(填微粒符号);由图2 知要提高碘的还原率,除控制温度外,还可以采取的措施是___________________________________。
I3-,图2中曲线a、b分别代表的微粒是________、_________(填微粒符号);由图2 知要提高碘的还原率,除控制温度外,还可以采取的措施是___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是 ( )
A.向Na2CO3溶液中逐滴加入HCl,直到不再生成CO2气体为止,在此过程中,溶液中的HCO3-浓度变化是先变大后变小(溶液体积变化均忽略不计)
B.向NaHCO3溶液中加入Ba(OH)2固体,CO32-的浓度变化是先变大后变小(溶液体积变化均忽略不计)
C.将等质量的Na2O和Na2O2样品分别放入等量的水中,所得溶液的质量分数分别为a%和b%,则a、b的关系是:a=b
D.有含0.2 mol Na2CO3和含0.3 mol HCl的两种溶液:①将Na2CO3溶液逐滴滴入HCl溶液中;②将HCl溶液逐滴滴入Na2CO3溶液中;①②两种操作生成的CO2体积之比为3∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com