
【题目】某学习小组研究NaOH与某些酸之间的反应。
Ⅰ.中和热的测定
在25℃、101kPa条件下,强酸与强碱的稀溶液中和热可表示为:H+(aq)+OH─(aq)=H2O(l) △H=-57.3kJ ·mol-1。按照图1所示装置进行实验。
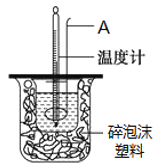
(1)仪器A的名称是________。
(2)碎泡沫塑料的作用是________。
(3)在25℃、101kPa条件下,取50mL 0.50 mol·L-1 CH3COOH溶液、50mL 0.55 mol·L-1 NaOH溶液进行实验,测得的中和热△H________-57. 3 kJ ·mol-1(填“>”“=”或“<”),原因是 ________。
Ⅱ.中和滴定
(1)用_______量取20.00 mL待测稀盐酸溶液放入锥形瓶中,并滴加1~2滴酚酞作指示剂,用0.20 mol·L—1NaOH标准溶液进行滴定。为了减小实验误差,该同学一共进行了三次实验,假设每次所取稀盐酸体积均为20.00 mL,三次实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗NaOH溶液体积/mL | 19.00 | 23.00 | 23.02 |
该盐酸的浓度约为________ (保留两位有效数字)。滴定达到终点的标志是________。
(2)若某次滴定结束时,滴定管液面如图2所示,则终点读数为________mL。

【答案】 环形玻璃搅拌棒 保温、隔热,减少实验过程中热量损失 > CH3COOH是弱酸,在反应过程中会继续电离吸收热量,使放出的热量减少,△H>-57.3 kJ/mol 酸式滴定管 0.23mol·L—1 滴入最后一滴氢氧化钠溶液,溶液由无色恰好变成红色,半分钟内不褪色 23.10
【解析】试题分析:Ⅰ.(1)根据装置图分析仪器A的名称。(2)碎泡沫塑料具有隔热的作用;(3)CH3COOH是弱酸,弱电解质电离吸热;Ⅱ.(1)量取盐酸的体积是20.00mL,精度为0.01mL,所以用酸式滴定管量取;第一次实验数值偏离正常的误差范围,所以根据第二次、第三次实验数值计算平均消耗氢氧化钠溶液的体积是23.01mL;根据![]() 计算盐酸浓度;(2)根据滴定管液面图2所示,凹液面最低处所示的刻度为终点读数;
计算盐酸浓度;(2)根据滴定管液面图2所示,凹液面最低处所示的刻度为终点读数;
解析:Ⅰ.(1)根据装置图仪器A的名称是环形玻璃搅拌棒。(2)碎泡沫塑料的作用是保温、隔热,减少实验过程中热量损失; (3)CH3COOH是弱酸,在反应过程中会继续电离吸收热量,使放出的热量减少,△H>-57.3 kJ/mol;Ⅱ.(1)量取盐酸的体积是20.00mL,精度为0.01mL,所以用酸式滴定管量取;第一次实验数值偏离正常的误差范围,所以根据第二次、第三次实验数值计算平均消耗氢氧化钠溶液的体积是23.01mL;根据![]() ,
, ![]() ,所以盐酸的浓度约为0.23mol·L—1;滴定达到终点的标志是滴入最后一滴氢氧化钠溶液,溶液由无色恰好变成红色,半分钟内不褪色;(2)根据滴定管液面图2所示,凹液面最低处所示的刻度为23.10mL。
,所以盐酸的浓度约为0.23mol·L—1;滴定达到终点的标志是滴入最后一滴氢氧化钠溶液,溶液由无色恰好变成红色,半分钟内不褪色;(2)根据滴定管液面图2所示,凹液面最低处所示的刻度为23.10mL。


科目:高中化学 来源: 题型:
【题目】作为“血迹检测小王子”,鲁米诺反应在刑侦中扮演了重要的角色,其一种合成原理如图所示。下列有关说法正确的是

A. 鲁米诺的化学式为C8H6N3O2
B. 1 mol A分子最多可以与5 mol氢气发生加成反应
C. B中处于同一平面的原子有9个
D. (1)、(2)两步的反应类型分别为取代反应和还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标况下将CO2气体缓缓地通入到含2 mol KOH、1 mol Ba(OH)2和2 mol KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示。下列关于整个反应进程中的各种描述正确的是
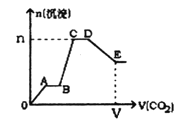
A.A~B段和C~D段发生的反应相同
B.B~C段反应的离子方程式是A1O2-+2H2O+CO2=Al(OH)3↓+HCO3-
C.V=134.4 L,n=3mol
D.D点所得溶液中离子浓度的关系为:c(K+)>c(CO32-)>c(OH﹣)>c(HCO3-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4(绿色)、Cr2O72(橙红色)、CrO42(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
(1)Cr3+与Al3+的化学性质相似。在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是_________。
(2)+6价铬的化合物毒性较大,常用NaHSO3将酸性废液中的Cr2O72还原成Cr3+,该反应的离子方程式为______________。
Ⅱ、以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
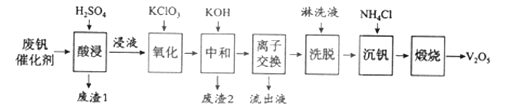
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________
(2)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。
III、氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌(含有Fe(Ⅱ), Mn(Ⅱ), Ni(Ⅱ)等杂质)的流程如下:

在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是MnO2,回答下列问题:
反应②中发生反应的离子方程式为___________,___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化钛是无色液体,沸点为136℃,极易水解。在800℃下,将氯气通过二氧化钛和炭粉的混合物可制得四氯化钛,同时产生一种有毒气体。装置如下图。
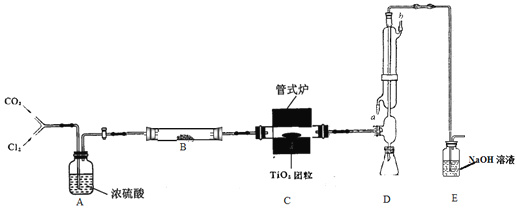
(1)实验步骤:
先将适量TiO2、炭粉混合均匀,制成多孔状TiO2团粒。然后进行如下操作,正确的顺序为____________________(填序号)。
①通入CO2气体并开始加热;
②观察反应已基本完成,停止加热,改通CO2气体直至冷却至室温;
③将TiO2团粒放入瓷管中适当位置,并连接好整套装置;
④当管式炉升温到800℃后改通Cl2,同时在冷凝管中通冷凝水;
⑤取下锥形瓶,立即用塞子塞紧。
实验中不直接使用二氧化钛和炭粉,而是先制成多孔状TiO2团粒的原因是_________。
(2)冷凝管冷凝水的入口为________(填标号)。
(3)装置B所装的药品为_____________,作用为________________;实验中两次通入CO2,其中第二次通入CO2的作用是______________;可用_______气体代替CO2(任填一种)。
(4)以上步骤②,观察到(填现象)________________时,可确定反应已基本完成。
(5)制备反应的主要化学方程式为_________________________________________。
(6)该装置存在明显的缺陷,提出改进措施__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。下列说法正确的是

A. O2所在的铂电极处发生氧化反应
B. H+透过质子交换膜流向呼气所在的铂电极
C. 电路中流过2mol电子时,消耗标准状况下11.2LO2
D. 该电池的负极反应式为:CH3CH2OH+3H2O-12e-=2CO2+12H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:HCl + NH3= NH4Cl(固体)如下图所示,抽去装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度。下列说法正确的是( )
![]()
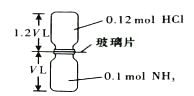
A. 反应后瓶内压强是反应前的1/10 B. 装置中氢元素的总质量为0.42 g
C. 生成物的分子数目为0.1 NA D. 反应结束后,两个集气瓶很容易分开
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室配制 500mL 0.2mol/L 的 NaOH溶液,在下图所示仪器中,配制上述溶液肯定不需要的是____(填序号),除图中已有仪器外, 配制上述溶液还需要的玻璃仪器是_________。
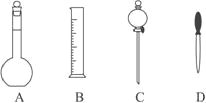
具体过程如下:
①计算需要称量 NaOH 固体的质量_____;
②用少量蒸馏水洗涤烧杯内壁 2~3 次,洗涤液也都注入容量瓶,轻轻晃动容量瓶,使溶液混合均匀;
③用托盘天平称量 NaOH 固体;
④将 NaOH 溶液沿玻璃棒注入_____中;
⑤将称好的 NaOH 固体放入烧杯中,用适量蒸馏水溶解,并____________;
⑥盖好瓶塞,反复上下颠倒,摇匀;
⑦将蒸馏水注入容量瓶,液面离刻度线下_____cm 时,改用_______滴加蒸馏水至液面于刻度线相切;
试回答下列问题:
(2)上述过程的正确顺序为___________(填步骤序号);
(3)经精确测量,最后所得溶液物质的量浓度为 0.192mol/L,原因可能是____________。
A、使用滤纸称量 NaOH 固体; B、未冷却直接转移至容量瓶,立即配好;
C、容量瓶中原来有少量蒸馏水; D、称量时所用的砝码生锈;
E、溶解 NaOH 后的烧杯未经多次洗涤; F、定容时俯视刻度。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com