
【题目】下列物质或结构中含有糖类的是()
①RNA ②染色体 ③脂肪 ④淀粉酶
A. ①② B. ③④ C. ②③ D. ②④
科目:高中化学 来源: 题型:
【题目】海水是资源的宝库:合理利用海水资源是当今是世界研究的重点课题。结合所学知识回答下列问题:
(1)列举一项海水中的能源:__________ ,海水中储量最大的资源是________ ,获得该资源最古老的方法是____________。
(2)海水中还有大量NaCl,MgCl2等盐类物质,从海水中获得纯净NaCl的分离提纯方法有过滤、______。
(3)目前世界上60%的镁是从海水提取的。海水提镁的主要流程如下:
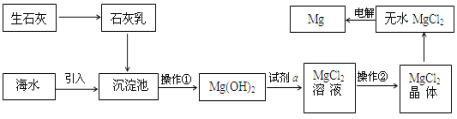
提示: MgCl2晶体的化学式为MgCl26H2O; MgO的熔点为2852℃,无水MgCl2的熔点为714℃。
①操作②的名称___________、冷却结晶、过滤。
②用氯化镁电解生产金属镁的化学方程式为:_____________________。
(4)粗盐提纯后的的卤水中含有大量的溴,从中提取溴的部分过程如下:

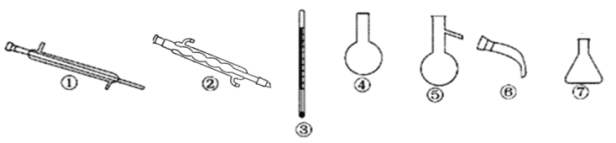
实验室模拟上述过程设计以下装置进行实验(所有橡胶制品已被保护,夹持装置已略去)

①A装置中通入a气体的目的是(用离子方程式表示) __________________________________________;
②A装置中先通入a气体后改通热空气。通入热空气的目的是______________________________________;
③B装置中b气体是SO2,目的是吸收富集Br2,此处离子方程式为___________________________________;
④向B装置中再次通入Cl2得到单质溴,对液体进行蒸馏,收集液溴。蒸馏应该选择下列仪器_____(填序号) 。
 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性高锰酸钾溶液可以将FeSO4氧化,化学方程式为2KMnO4+10FeSO4+8H2SO4===K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示。则下列有关说法不正确的是( )
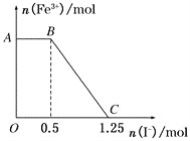
A. 图中AB段主要是高锰酸钾和碘化钾溶液反应
B. 图中BC段发生的反应为2Fe3++2I-===2Fe2++I2
C. 根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25 mol
D. 根据OC段的数据可知开始加入的硫酸亚铁的物质的量为1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
2R—C≡C—H![]() R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)B的结构简式为______,D 的化学名称为______。
(2)①和③的反应类型分别为______、______。
(3)E的结构简式为______。用1 mol E合成1,4二苯基丁烷,理论上需要消耗氢气_______mol。
(4)化合物(![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中3种的结构简式_______________________________。
(6)写出用2苯基乙醇为原料(其他无机试剂任选)制备化合物D的合成路线___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验是化学学习的重要内容。根据你掌握的知识,完成下面内容。
![]() 实验室需要配制0.1 mol·L-1NaOH溶液230mL,请回答下列问题:
实验室需要配制0.1 mol·L-1NaOH溶液230mL,请回答下列问题:
![]() 应选择____mL的容量瓶,用天平称取____g NaOH。
应选择____mL的容量瓶,用天平称取____g NaOH。
![]() 溶解NaOH后的溶液需冷却到室温后方能转移入容量瓶中。若趁热转移会使溶液的浓度______(填“偏大”或“偏小”,下同);在洗涤烧杯和玻璃棒的过程中,每次洗涤液均需注入容量瓶,不能损失点滴液体,否则会导致溶液的浓度______。
溶解NaOH后的溶液需冷却到室温后方能转移入容量瓶中。若趁热转移会使溶液的浓度______(填“偏大”或“偏小”,下同);在洗涤烧杯和玻璃棒的过程中,每次洗涤液均需注入容量瓶,不能损失点滴液体,否则会导致溶液的浓度______。
![]() 有人认为,用这种方法只能配置0.1 mol·L-1的NaOH溶液,而无法得到0.1000 mol·L-1的NaOH溶液,你觉得他的理由是__________________________________________。
有人认为,用这种方法只能配置0.1 mol·L-1的NaOH溶液,而无法得到0.1000 mol·L-1的NaOH溶液,你觉得他的理由是__________________________________________。
![]() 选择下列实验方法分离物质,将分离方法的序号填在横线上。
选择下列实验方法分离物质,将分离方法的序号填在横线上。
![]() 萃取分液
萃取分液 ![]() 升华
升华 ![]() 结晶
结晶 ![]() 过滤
过滤 ![]() 蒸馏
蒸馏 ![]() 分液
分液
![]() 分离饱和食盐水与沙子的混合物______;
分离饱和食盐水与沙子的混合物______;
![]() 从硝酸钾和氯化钠的混合液中获得硝酸钾______;
从硝酸钾和氯化钠的混合液中获得硝酸钾______;
![]() 从碘水中提取碘单质______;
从碘水中提取碘单质______;
![]() 分离水和汽油的混合物______;
分离水和汽油的混合物______;
![]() 分离
分离![]() 沸点为
沸点为![]() 和甲苯
和甲苯![]() 沸点为
沸点为![]() 的混合物______。
的混合物______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体③溶液呈现蓝色。据此判断下列说法正确的是
与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体③溶液呈现蓝色。据此判断下列说法正确的是
A. 反应中硫酸作氧化剂
B. ![]() 中硫元素被氧化
中硫元素被氧化
C. 刺激性气味的气体是氨气
D. 1mol![]() 完全反应转移0.5mol电子
完全反应转移0.5mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯元素是生产生活中常见的非金属元素。
(1)生物质混煤燃烧是当今能源燃烧利用的最佳方式之一,但生物质中氯含量较多,燃烧过程中会形成金属氯化物(如NaCl)和Cl2等物质,对金属炉壁造成腐蚀。
①NaCl和Cl2中化学键的类型分别是________和________。
②燃煤过程中生成的SO2会与NaCl等物质发生反应,生成硫酸盐和Cl2。若生成Cl2 22.4 L(标况)时转移电子数为4×6.02×1023,该反应的化学方程式是__________________
(2)已知:2H2O2(l)===2H2O(l)+O2(g) ΔH1=-196.46 kJ·mol-1
H2(g)+1/2O2(g)===H2O(l) ΔH2=-285.84 kJ·mol-1
Cl2(g)+H2(g)===2HCl(g) ΔH3=-184.60 kJ·mol-1
在催化剂作用下,用H2O2(l)可除去上述燃烧过程中产生的Cl2。依据上述已知反应,写出该反应的热化学方程式:________________________________。
(3)使用“催化转化器”可以减少尾气中的CO和NOx,转化过程中发生反应的化学方程式为CO+NOx→N2+CO2(未配平),若x=1.5,则化学方程式中CO2和N2的化学计量数之比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石墨烯锂硫电池是一种高容量、长循环寿命、低成本及环境友好的新型二次电池,其工作原理如图所示,电池反应为2Li+nS![]() Li2Sn。下列说法错误的是
Li2Sn。下列说法错误的是

A. 放电时,Li+向正极移动
B. 充电时,A电极连接直流电源的正极
C. 充电时,每生成nmolS,外电路中流过2nmol电子
D. 放电时,正极上可发生反应2Li++Li2S4+2e-=2Li2S2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体免疫球蛋白中, IgG 由 4 条肽链构成,共有 764 个氨基酸,则该蛋白分子中至少含有游离的氨基和羧基数分别是( )
A. 746 和 764 B. 760 和 760 C. 762 和 762 D. 4 和 4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com