
����Ŀ��(1)�һ��嶡����(��ETBE��ʾ)��һ�����������ĸ�����ֵ���͵��ͼ������Ҵ����춡ϩ(��IB��ʾ)�ڴ���HZSM��5���ºϳ�ETBE����Ӧ�Ļ�ѧ����ʽΪ��C2H5OH(g)+IB(g)=ETBE(g) ��H���ش��������⣺
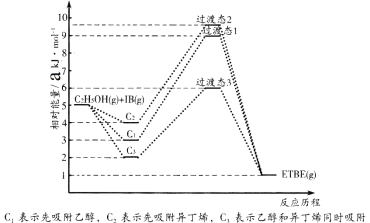
��Ӧ�ﱻ����HZSM��5������˳���뷴Ӧ���̵Ĺ�ϵ��ͼ��ʾ���÷�Ӧ�ġ�H=__________ kJ��mol-1����Ӧ���̵�����;����________(��C1��C2��C3)��
(2)���������Դ�ǵ����о���һ���ȵ����⡣������(CH3OCH3)��δ������������ͺ�Һ������Ϊ�ྻҺ��ȼ��ʹ�ã���ҵ����CO��H2Ϊԭ������CH3OCH3����ҵ�Ʊ��������ڴ���Ӧ����(ѹ��2.0��10.0Mpa���¶�230��280��)�������з�Ӧ��
��Ӧ����CO(g)+2H2(g)CH3OH(g) ��H1=-99kJ��mol1
��Ӧ����2CH3OH(g)CH3OCH3(g)+H2O(g) ��H2=-23.5kJ��mol1
��Ӧ����CO(g)+H2O(g)CO2(g)+H2(g) ��H3=-41.2kJ��mol1
���ڸ������£�����Ӧ1����ʼŨ�ȷֱ�Ϊ��c(CO)=0.6mol��L1��c(H2)=1.4mol��L1��8min��ﵽƽ�⣬CO��ת����Ϊ50%����8min��H2��ƽ����Ӧ����Ϊ__________��
����t��ʱ����Ӧ2��ƽ�ⳣ��Ϊ400�����¶��£���1L���ܱ������м���һ���ļ״�����Ӧ��ijʱ�̲�ø���ֵ����ʵ���Ũ�����£�
���� | CH3OH | CH3OCH3 | H2O |
c(mol��L1) | 0.46 | 1.0 | 1.0 |
��ʱ��v��___v��(���������������)��ƽ��ʱc(CH3OCH3)�����ʵ���Ũ����___��
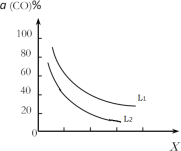
�۴���Ӧ�ҵ��ܷ�Ӧ3CO(g)+3H2(g)CH3OCH3(g)+CO2(g)��CO��ƽ��ת������(CO)���¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��ͼ��X����___(��¶ȡ���ѹǿ��)����L1___L2(���������������)��
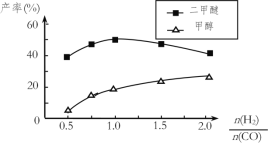
���ڴ�����������ͬʱ����������Ӧ������������ʼͶ�ϱ�![]() �ĸı䣬�����Ѻͼ״��IJ���(�����е�̼ԭ��ռ��ʼCO��̼ԭ�ӵİٷ���)������ͼ�ı仯���ơ��Խ���Ͷ�ϱȴ���1.0֮������Ѳ��ʺͼ״����ʱ仯��ԭ��______________��
�ĸı䣬�����Ѻͼ״��IJ���(�����е�̼ԭ��ռ��ʼCO��̼ԭ�ӵİٷ���)������ͼ�ı仯���ơ��Խ���Ͷ�ϱȴ���1.0֮������Ѳ��ʺͼ״����ʱ仯��ԭ��______________��
���𰸡�-4a C3 0.075mol��L-1��min-1 �� 1.2mol��L-1 �¶� �� ��Ͷ�ϱȴ���1ʱ������c(H2)����Ӧ�����ٽ�������Ӧ�������ƣ�c(H2O)�����������Ʒ�Ӧ������˼״��IJ��ʼ�������������ѵIJ��ʼ�С
��������
(1)��ͼ��֪����Ӧ���������Ϊ5a kJ��mol-1���������������Ϊa kJ��mol-1�����Է�Ӧ�ġ�H= - 4 kJ��mol-1����Ӧ���̵�����;����C3��������Ҫ�Ļ����С��
(2)���ڸ������£�����Ӧ������ʼŨ�ȷֱ�Ϊ��c(CO)=0.6mol��L1��c(H2)=1.4mol��L1��8min��ﵽƽ�⣬CO��ת����Ϊ50%����8min��H2��ƽ����Ӧ����Ϊ��![]() ��
��
����t��ʱ����ʱ��Ӧ���У�![]() �����Դ�ʱ��v����v�����ɱ������ݼ���Ӧ���г�����ʽ�����������ļ״�����Ϊ2.46 mol��ƽ��ʱ��c(CH3OCH3)�����ʵ���Ũ��Ϊx mol/L������
�����Դ�ʱ��v����v�����ɱ������ݼ���Ӧ���г�����ʽ�����������ļ״�����Ϊ2.46 mol��ƽ��ʱ��c(CH3OCH3)�����ʵ���Ũ��Ϊx mol/L������![]() �����x=1.2��
�����x=1.2��
�۴���Ӧ�ҵ��ܷ�Ӧ3CO(g)+3H2(g)CH3OCH3(g)+CO2(g)���ɷ�Ӧʽ����2+��+�����ã��ʸ��ܷ�Ӧ����H=��H1��2+��H2+��H3= -262.7 kJ��mol1��0���÷�Ӧ�Ƿ��ȷ�Ӧ�������£���CO��ƽ��ת���ʻή�ͣ����ܷ�Ӧ������ϵ����С�ķ�Ӧ������ѹ����CO��ƽ��ת���ʻ�������ͼ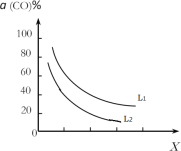 �������֪��������X���������¶ȣ���ôL��������ѹǿ������ѹǿ����CO��ƽ��ת����Ҳ������жϣ�L1��L2��
�������֪��������X���������¶ȣ���ôL��������ѹǿ������ѹǿ����CO��ƽ��ת����Ҳ������жϣ�L1��L2��
�ܵ�Ͷ�ϱȴ���1ʱ������c(H2)����Ӧ�����ٽ�������Ӧ�������ƣ�c(H2O)�����������Ʒ�Ӧ������˼״��IJ��ʼ�������������ѵIJ��ʼ�С��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵�����ʾ������ȷ����
A.�����ʵ������������������ֱ���ȫȼ������SO2���壬�ų�������һ����
B.��C(ʯī)=C(���ʯ) ��H=+1.90kJ��mol-1��֪�����ʯ��ʯī�ȶ�
C.2CO(g)+O2(g)=2CO2(g) ��H��0����56gCO��32gO2���������������88gCO2�����������
D.��֪��N2(g)+3H2(g)![]() 2NH3(g) ��H=-92.4kJ��mol-1������ͬ�����£����ܱ������У�1molN2��3molH2��ϳ�ַ�Ӧ��ų�92.4kJ������
2NH3(g) ��H=-92.4kJ��mol-1������ͬ�����£����ܱ������У�1molN2��3molH2��ϳ�ַ�Ӧ��ų�92.4kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ѿ�ѧ���Ļ�ѧ֪ʶ���ش��������⡣
I.(1)��������ʮ�����ʣ������� ������KNO3 ��ʯī ��ͭ˿ ��NaOH���� ��SO3 ��BaSO4���� ��K2O���� ��Һ̬H2SO4 ��Һ�� ���������пɵ������____________(����ţ���ͬ)�����������в��ܵ��磬�����ڵ���ʵ���_______________________��
(2)NaHSO4��һ����ʽ�Σ�����д���пհף�
��д��NaHSO4��ˮ�еĵ��뷽��ʽ____________________________________��
����0.1 mol��L��1��NaHSO4��Һ�ĵ���������ͬ����������Һ�����ʵ���Ũ��Ϊ��_____��
��NaHSO4��Һ��NaHCO3��Һ��Ӧ�����ӷ���ʽΪ______________________________��
(3)�����к�������CaCl2��MgCl2��һЩ�����Σ���ȥ��Щ���ʵ��Լ���ѡ�ã���Na2CO3����NaOH����BaCl2����HCl������ű�ʾ������Ⱥ�˳��������_________��
II��A��B��C��X��Ϊ��ѧ�������ʣ�������һ��������������ת����ϵ(����������ȥ)��
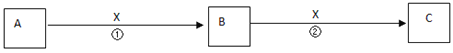
(1)��X����������A������ ______(�����)
A��C B��SiC��NaD��Mg
(2)��X�ǽ������ʣ���dz��ɫ��ҺC�е���AgNO3��Һ�������˲�����ϡHNO3�İ�ɫ��������B�Ļ�ѧʽΪ__________��C��Һ������ʱӦ��������X��������(�����ӷ���ʽ��ʾ)________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ�� W��X��Y��Z ��ԭ����������������Ԫ���γɵĻ�����Ľṹ��ͼ��ʾ���� W �� X��Y��Z �����γɵ�������ȵķ��ӣ�W2Z���³�ѹ��ΪҺ�塣����˵����ȷ����
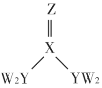
A.YW3 �����еļ���Ϊ120��
B.W2Z ���ȶ��Դ���YW3
C.1mol�������2mol Y-W��
D.Y Ԫ�ص��������Ӧ��ˮ����Ϊǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾװ�ã�������ָ�뷢��ƫת��ͬʱA����֣�B����ϸ��CΪ�������Һ����A��B��C���������и����е�

A.A��Ag��B��Fe��CΪϡAgNO3��Һ
B.A��Cu��B��Zn��CΪϡH2SO4
C.A��Fe��B��Ag��CΪϡAgNO3��Һ
D.A��Zn��B��Cu��CΪϡH2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ���(HSO3Cl)���Ǿ����ǰ�ҩ������������Ҫ��Ӧ�á����³�ѹ���Ȼ���Ϊ��ɫ��״Һ�壬�е�ԼΪ152�棬��ʪ�Ժ�ʴ�Լ�ǿ���ڿ����з��̡�ѧϰС����ʵ������SO3��HCl���Ʊ�HSO3Cl���ⶨ��Ʒ���ȡ��������ʵ��(�г�װ����ȥ)����ش��������⣺
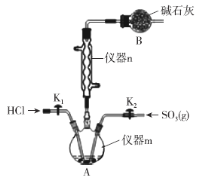
��1������m������Ϊ___��
��2����֪��HSO3Cl����Ԫ��Ϊ��6�ۣ�Oԭ�Ӻ�Clԭ�ӵ�����������8�����ȶ��ṹ����HSO3Cl�еĻ�ѧ��Ϊ___ (�������Ӽ����������Լ��������Ǽ��Լ���)��
��3��SO3����������������Ũ���Ṳ���Ʊ���������Ӧ�Ļ�ѧ����ʽΪ___��
��4��װ��B������Ϊ___��������n��֪�Ʊ�HSO3Cl�ķ�ӦΪ___ (�������ȷ�Ӧ���������ȷ�Ӧ��)��
��5��HSO3Cl���ȵIJⶨ(����m�еõ���HSO3Cl�г�����������SO3)��
i.ȡ25.0g��Ʒ����ˮ�У����������Ba(NO3)2��Һ��ַ�Ӧ���ˡ�
ii.����Һ�м��������AgNO3��Һ�����ˡ�ϴ�ӡ�����������������ó���AgCl������Ϊ28.7g��
��HSO3Cl��ˮ������Ӧ�Ļ�ѧ����ʽΪ___��
�ڲ�ƷHSO3Cl�Ĵ���Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(SO2Cl2)�����Ȼ������Ȼǻ�������������ҩƷ��Ⱦ�ϡ�������Լ��ȡ��й����ʵIJ����������±���
���� | �۵�/�� | �е�/�� | �������� |
SO2Cl2 | -54.1 | 69.1 | ����ˮ�⣬������������ ���ֽ⣺SO2Cl2 |
H2SO4 | 10.4 | 338 | ��ˮ���Ҳ��ֽ� |
ʵ�����ø�������Ķ�������������ϳ������ȣ�װ����ͼ��ʾ���г�������ʡ�ԣ�����ش��й����⣺

��1������A��ȴˮ�Ľ�ˮ��Ϊ________������a������b������
��2������B��ʢ�ŵ�ҩƷ��________����Ŀ����________________________��
��3��ʵ��ʱ��װ�ö��з�����Ӧ�����ӷ���ʽΪ______________________________��������6.72L������������£���ת�Ƶ��ӵ����ʵ���Ϊ________��
��4��װ�ñ���ʢ�ŵ��Լ���________����ȱ��װ���ң���ʵ����ɵ�Ӱ����_______________��
��5������������Ҳ����Һ̬�Ȼ��ᣨClSO3H�����´��ֽ��ã��÷�Ӧ�Ļ�ѧ����ʽΪ��2ClSO3H��H2SO4 +SO2Cl2���ӷֽ�����з���������ȵIJ�����______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10 mL 0.21 molL��1�������10 mL 0.1 molL��1Ba(OH)2��Һ��ϣ�����ˮϡ����5 L��ȡ��10 mL��������Լ�������Һ��ʾ����ɫ��(����)
A. ��ɫB. ��ɫC. ��ɫD. ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ķ��ӽṹ�ɼ�д�ɼ���ʽ�ṹ![]() ���л���A�ļ���ʽ�ṹΪ
���л���A�ļ���ʽ�ṹΪ![]() ���л���B������ʵ�����H2�����ӳɷ�Ӧ�ɵõ��л���A�������й�˵��������ǣ�������
���л���B������ʵ�����H2�����ӳɷ�Ӧ�ɵõ��л���A�������й�˵��������ǣ�������
A. ��ϵͳ�����������л���A������Ϊ2��2��3����������
B. �л���A��һ��ȡ����ֻ��4��
C. �л���A�ķ���ʽΪC8H18
D. B�Ľṹ������3�֣�����һ������Ϊ3��4��4��������2����ϩ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com