
����Ŀ����֪A��B��C��D��E�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵����A��B��C��D��E������A��B��C��ͬһ���ڵķǽ���Ԫ�ء�������DC�ľ���Ϊ���Ӿ��壬D�Ķ�����������C�������Ӿ�����ͬ�ĵ��Ӳ�ṹ��AC2Ϊ�Ǽ��Է��ӡ�B��C���⻯��ķе������ͬ����������Ԫ���⻯��ķе�ߡ�E��ԭ������Ϊ24��ECl3����B���⻯���γ�����λ������������������λ����硣
���������������ش��������⣺������ʱ��A��B��C��D��E������Ӧ��Ԫ�ط��ű�ʾ��
��1��A��B��C�ĵ�һ��������С�����˳��Ϊ____��
��2��B���⻯��ķ��ӿռ乹����____��
��3��д��AC2�ĵ���ʽ____��������ԭ�Ӳ�ȡ____�ӻ���
��4��ECl3�γɵ������Ļ�ѧʽΪ____��1mol��������ЦҼ���ĿΪ____mol��
��5��B���⻯����Һ����ԭ����____��
���𰸡�C<O<N������![]() sp[Cr(NH3)5Cl]Cl221NH3���Ӽ��γ����
sp[Cr(NH3)5Cl]Cl221NH3���Ӽ��γ����
��������
A��B��C��D��E�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵����A��B��C��D��E������DC�ľ���Ϊ���Ӿ��壬D�Ķ�����������C�������Ӿ�����ͬ�ĵ��Ӳ�ṹ��C�γ�-2�������ӣ���Dλ��C����һ���ڣ�B��C���⻯��ķе������ͬ����������Ԫ���⻯��ķе�ߣ������д��������C�γ�-2�������ӣ���CΪ��Ԫ�أ�DΪþԪ�أ��˵����B��C����BΪ��Ԫ�أ�����A��B��C��ͬһ���ڵķǽ���Ԫ�أ�AC2Ϊ�Ǽ��Է��ӣ���AΪ̼Ԫ�أ�E��ԭ������Ϊ24����EΪCrԪ�أ�CrCl3����NH3�γ�����λ����������������λ����磬����������5��NH3��1��Cl-���������Ϊ[Cr(NH3)5Cl]Cl2���ݴ˷����ɵý��ۡ�
��1��AΪ̼Ԫ�ء�BΪ��Ԫ�ء�CΪ��Ԫ�أ�ͬ����������ҵ�һ����������Ԫ��ԭ��2p�ܼ���3�����ӣ����ڰ����ȶ�״̬�����������ͣ���Ԫ�ص�һ�����ܸ������ڵ�Ԫ�صģ����Ե�һ��������С�����˳��ΪC��O��N���ʴ�Ϊ��C��O��N��
��2��BΪ��Ԫ�أ����⻯��ΪNH3�������к���3��N-H����Nԭ����1�Թ¶Ե��Ӷԣ��ӻ������Ϊ4��Nԭ�Ӳ�ȡsp3�ӻ����ռ乹��Ϊ���������ʴ�Ϊ�������ͣ�
��3��������AC2��CO2��������̼ԭ������ԭ��֮���γ�2�Թ��õ��Ӷԣ�����ʽΪ![]() ��CO2��������ԭ�ӵļ۲���Ӷ���Ϊ
��CO2��������ԭ�ӵļ۲���Ӷ���Ϊ![]() ��4=2����sp�ӻ�����ɼ��� �ʴ�Ϊ��
��4=2����sp�ӻ�����ɼ��� �ʴ�Ϊ��![]() ��sp��
��sp��
��4��CrCl3����NH3�γ�����λ����������������λ����磬����������5��NH3��1��Cl-���������Ϊ[Cr(NH3)5Cl]Cl2��[Cr(NH3)5Cl]Cl2�к���21������������������ĿΪ21���ʴ�Ϊ��[Cr(NH3)5Cl]Cl2��21��
��5��B���⻯����Ӽ����γ��������Һ�����ʴ�Ϊ��NH3���Ӽ��γ������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����300mL2.0 mol/L�����м��뼸С�����ʯ����������������ʱ��ı仯��������ͼ��ʾ(��������ڱ�״���²ⶨ)�Իش��������⣺

(1)���Է�Ӧ�����ĵ�HCl��ʾ��Ӧ���ʣ���OE�εķ�Ӧ����Ϊv1��EF�εķ�Ӧ����Ϊv2��FG�εķ�Ӧ����Ϊv3����v1��v2��v3�Ӵ�С��˳��Ϊ_______���������v1��v2��С��ϵ����Ҫԭ����__________��
(2)Ϊ�˼���������Ӧ�����ʣ��������Һ�м����������ʣ�����Ϊ���е���_____(����)
A.Ũ���� B.Na2CO3 C.����ˮ D.Ũ����
(3)����Ӧ��������Һ����ı仯���Բ��ƣ��������ʾ�Ļ�ѧ��Ӧ����v(HCl)=________mol/(Lmin)��.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ԭ��Ӧ��Zn(s)��Cu2��(aq)===Zn2��(aq)��Cu(s)��Ƶ�ԭ�������ͼ��ʾ��
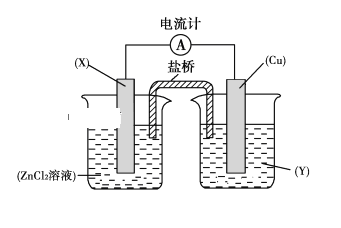
��ش��������⣺
��1���缫X�IJ�����________���������ҺY��________��
��2��ͭ�缫Ϊ��ص�________���������ĵ缫��ӦΪ______________________��X���Ϸ����ĵ缫��ӦΪ________________��
��3�����·�еĵ����Ǵ�________������________����
��4�������е�Cl����________���ƶ����罫���ų����������Ƶ�ָ�뽫________ƫת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������̼��Ӧ�������������ĺ�����С����Ա̫������ʱ���ĺ�����С���DZͧ�о�ʹ�ù��������������������˺���֮�á�ijѧ��ѡ�ô���ʯ�������һ������������ҩƷ���ʵ�飬��֤��һ��ʵ��
���������װ�ûش��������⣺

��1��A����ȡCO2��װ�ã����ѡ������װ���е�______________ (�����)��

��2��Bװ���з��������ӷ���ʽ��_______________________��Cװ�õ�������_______________________��
��3��Dװ���з�����Ӧ�Ļ�ѧ����ʽ��_________________��
��4��Ҫ��õ��ϴ���������������װ��D��E֮������һʢ��________(��д�Լ�����)��________(��дװ������)��
��5����μ��鼯��ƿ���ռ���������______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڻ�ʯȼ�ϵ�˵����ȷ����
A.ʯ�ͷ���ɻ��ʯ���������͡�������ͬϵ���
B.ʯ�ʹ��ѻ���Ҫ�õ���ϩ����Ȳ��
C.ú���б��ͼױ����ɸ�����ñ��ͼױ�
D.ú��Һ�����������ھ����ڻ�ѧ�仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£�A������B���巴Ӧ����C���塣��Ӧ�����У���Ӧ�����������Ũ����ʱ��仯��������ͼ���ش��������⣺

��1���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��2��0��t1 s��A����ķ�Ӧ����Ϊ ��
��3����Ӧ���뷴Ӧǰ��ѹǿ֮��Ϊ ��
��4��(t1��10)sʱ��A������������Ϊ ����ʱv(A)�� v(B)�棨����>������<������=������
��5�����ڸ÷�Ӧ��˵����ȷ���� ��
a������t1ʱ�̸÷�Ӧ��ֹͣ
b����t1ʱ��֮ǰB������������ʴ���������������
c����t1ʱ��C���������Ӧ���ʵ����淴Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й���Ϣ������и��⣺
��1���л���A���л���B(![]() )��ͬ���칹�壬�˴Ź������ײ���������ֻ�����ֲ�ͬ��ѧ�������⣬����Ŀ��Ϊ1��3��д���������ֵĽṹ��ʽ��____��____��____��
)��ͬ���칹�壬�˴Ź������ײ���������ֻ�����ֲ�ͬ��ѧ�������⣬����Ŀ��Ϊ1��3��д���������ֵĽṹ��ʽ��____��____��____��
��2���л���B��һ�������·�Ӧ�����л���C��1mol�л���C�����Ժ�2molBr2�����ӳɷ�Ӧ��д���л���B��һ�������·�Ӧ�����л���C�Ļ�ѧ����ʽ��____��
��3����֪��![]() ��
��
д����![]() Ϊԭ�ϣ��������Լ���ѡ���Ʊ��߷���
Ϊԭ�ϣ��������Լ���ѡ���Ʊ��߷��� �ĺϳ�·��____���ϳɷ�Ӧ����ͼ��ʾ�������磺
�ĺϳ�·��____���ϳɷ�Ӧ����ͼ��ʾ�������磺![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ����֤Fe3�������ʣ�ij��ѧ��ȤС���������ͼ��ʾ��һ��ʵ�飬����ʵ�鷽����ƴ������(����)

A. ֻ�Т� B. ֻ�Т�
C. �ۺܾ͢����� D. ȫ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(SO2Cl2)�������Ȼ������Ȼǻ�������Ⱦ�ϡ�ҩƷ�����ݼ���ũ��ɱ�������������������Ҫ���á��������ø����Cl2��SO2�ڻ���̿������ȡ�����ȡ���Ӧ�Ļ�ѧ����ʽΪ��SO2(g)+ Cl2(g) =SO2Cl2(l) ��H =97.3 kJ��mol1��ʵ��װ����ͼ��ʾ(���ּг�װ��δ����)��
��֪��������ͨ��������Ϊ��ɫҺ�壬�۵�54.1�棬�е�69.1�档�ڳ�ʪ�����С����̡������ڷ��û���100��C���Ϸ����ֽ⣬���ɶ��������������
�ش��������⣺
��1������C��������_______________�������ܵĽ�ˮ����______���a����b������
��2�����в�����������ȷ����_________________��
A����70%���ỻ��98.3%���ᣬ���Լӿ���ȡSO2������
B��ʵ����ͨ���۲��ҡ������ܿڲ������ݵ�������ȣ��ɿ������ַ�Ӧ��������
C��װ�����Ϸ���Һ©�������ѡ��0.10 molL-1NaCl��Һ����С�������ܽ��
D��װ�ü���ֹ��Ⱦ���ַ�ֹ�����ȱ���
��3���Ȼ���(ClSO3H)���ȷֽ⣬Ҳ���Ƶ������ȣ�д����Ӧ����ʽ��_____________��
��4�����ڴ���������Ȼᷢ�ƣ����ܵ�ԭ����_________________________(�û�ѧ����ʽ�ͱ�Ҫ�����ּ��Խ���)��
��5������Ӧ�����ĵ��������Ϊ896 mL(��״����)����������ᴿ�õ�4.05 g�����������ȣ��������ȵIJ���Ϊ_______�������ʣ�![]() ��100%��
��100%��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com