
【题目】溴化锂是一种高效的水汽吸收剂,其一种绿色工业合成工艺如下(部分操作和条件已略去)。
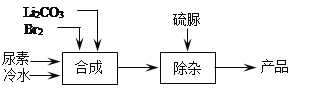
已知:碳酸锂微溶于水,水溶液显碱性。
(1)Br2的电子式是______。
(2)合成过程中发生的反应如下,请写出ii反应的化学方程式并将iii补充完整。
ⅰ. Br2 +H2O![]() HBr +HBrO;
HBr +HBrO;
ⅱ._____;
ⅲ. 3LiBrO + CO(NH2)2(尿素)=3LiBr+_____。
(3)LiBrO3是生产过程中的副产物。
①用化学方程式表示生成改副产物的原因:______。
②为了提高原料的利用率,减少副产物的生成,必须调控体系的pH在3~5之间,通过合理的加料方法来实现:将碳酸锂粉末溶解于冷的溴水中至饱和,并一次性加入尿素,然后再______,直到尿素完全转化。
③常用硫脲除去LiBrO3,反应的化学方程式是4LiBrO3 +3CS(NH2)2(硫脲) +3H2O=4LiBr +3CO(NH2)2 +3H2SO4 ,选用硫脲除杂的优点是_______;缺点是引入新杂质且溶液酸性增强,为解决该问题需要加入的试剂是_______。
【答案】 ![]() Li2CO3 +2HBr= 2LiBr +H2O +CO2 ↑ CO2↑+N2↑+2H2O 3Br2 + 3Li2CO3 = 2LiBrO3 +5LiBr +3CO2 ↑ 少量多次交替加入Br2 和Li2CO3 可将LiBrO3转化为LiBr,并得到可以循环使用的CO(NH2)2 BaCO3
Li2CO3 +2HBr= 2LiBr +H2O +CO2 ↑ CO2↑+N2↑+2H2O 3Br2 + 3Li2CO3 = 2LiBrO3 +5LiBr +3CO2 ↑ 少量多次交替加入Br2 和Li2CO3 可将LiBrO3转化为LiBr,并得到可以循环使用的CO(NH2)2 BaCO3
【解析】(1)溴最外层有7个电子,Br2的电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(2)合成过程中发生的反应如下:ⅰ. Br2 +H2O![]() HBr +HBrO;ⅱ.反应生成氢溴酸能够与碳酸锂生成溴化锂和二氧化碳,反应的方程式为Li2CO3 +2HBr= 2LiBr +H2O +CO2 ↑,ⅲ.HBrO与碳酸锂反应生成LiBrO,LiBrO具有强氧化性,将CO(NH2)2氧化生成二氧化碳和氮气,反应的方程式为3LiBrO + CO(NH2)2=3LiBr+ CO2↑+N2↑+2H2O,故答案为:Li2CO3 +2HBr= 2LiBr +H2O +CO2 ↑;CO2↑+N2↑+2H2O;
HBr +HBrO;ⅱ.反应生成氢溴酸能够与碳酸锂生成溴化锂和二氧化碳,反应的方程式为Li2CO3 +2HBr= 2LiBr +H2O +CO2 ↑,ⅲ.HBrO与碳酸锂反应生成LiBrO,LiBrO具有强氧化性,将CO(NH2)2氧化生成二氧化碳和氮气,反应的方程式为3LiBrO + CO(NH2)2=3LiBr+ CO2↑+N2↑+2H2O,故答案为:Li2CO3 +2HBr= 2LiBr +H2O +CO2 ↑;CO2↑+N2↑+2H2O;
(3)①LiBrO3是生产过程中的副产物,生成LiBrO3的反应方程式为3Br2 + 3Li2CO3 = 2LiBrO3 +5LiBr +3CO2 ↑,故答案为:3Br2 + 3Li2CO3 = 2LiBrO3 +5LiBr +3CO2 ↑;
②为了提高原料的利用率,减少副产物的生成,必须调控体系的pH在3~5之间,通过合理的加料方法来实现:将碳酸锂粉末溶解于冷的溴水中至饱和,并一次性加入尿素,然后再少量多次交替加入Br2 和Li2CO3,直到尿素完全转化,故答案为:少量多次交替加入Br2 和Li2CO3;
③常用硫脲除去LiBrO3,反应的化学方程式是4LiBrO3 +3CS(NH2)2(硫脲) +3H2O=4LiBr +3CO(NH2)2 +3H2SO4 ,选用硫脲除杂的优点有可将LiBrO3转化为LiBr,并得到可以循环使用的CO(NH2)2;缺点是引入新杂质硫酸,且溶液酸性增强,为解决该问题,可以加入BaCO3除去硫酸,同时又不会引入新杂质,故答案为:可将LiBrO3转化为LiBr,并得到可以循环使用的CO(NH2)2;BaCO3。


科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.所有烷烃和蛋白质中都存在碳碳单键
B.乙醇与乙酸存在相同官能团
C.乙烷能发生加聚反应
D.米酒变酸的过程涉及了氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Na+、Ca2+、NO、CO![]() 、SO
、SO![]() 、Cl-等离子。为了鉴别这些离子,分别取少量溶液进行以下实验:
、Cl-等离子。为了鉴别这些离子,分别取少量溶液进行以下实验:
①加稀盐酸后,生成无色无味的气体,该气体能使澄清石灰水变浑浊。
②加足量的BaCl2产生白色沉淀,过滤,在沉淀中加入足量的盐酸,沉淀不能完全溶解。
③取②中滤液,加硝酸酸化后,再加过量的AgNO3溶液,析出白色沉淀。
(1)上述3个实验证明一定存在的离子是__________,一定不存在的离子是________,可能存在的离子为_______________。
(2)写出①中涉及反应的离子反应方程式: _____________________________。
(3)实验室中常用于检验Na+是否存在的方法叫___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.1molCH3COONa和0.05molHCl溶于水配成1L溶液(pH<7).
(1)用离子方程式表示该溶液中存在的三个平衡体系______________、_______________、___________________
(2)溶液中各离子的物质的量浓度由大到小顺序为_____________________________________________________
(3)溶液中粒子中浓度为0.1mol/L的是________________,浓度为0.05mol/L的是____________________
(4)物质的量之和为0.lmol的两种粒子是______________与__________
(5)CH3COO-和OH-的物质的量之和比H+多________mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活关系密切。下列关于生活中常见物质的说法,不正确的是( )
A.羊毛、蚕丝、塑料、合成橡胶都属于有机高分子材料
B.天然植物油没有恒定的熔沸点,常温下难溶于水
C.所有的油脂、糖类和蛋白质都能发生水解反应
D.麦芽糖及其水解产物均能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.氧化剂本身被还原,生成氧化产物
B.氧化剂是在反应中得到电子(或电子对偏向)的物质
C.还原剂在反应时所含元素的化合价降低
D.在一个反应中,氧化剂和还原剂不可能是同一物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器的名称、组装及使用方法是中学化学实验的基础,根据下图所示实验装置,回答下列问题。
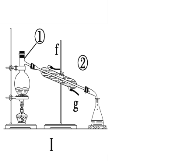
(1)写出上图中仪器的名称:①____________,②_____________。
(2)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器___________;②中进水口是________(填“f”或“g”)。
(3)下列实验需要在哪套装置中进行(填序号):
a.从海水中提取蒸馏水:______; b.分离氯化钠和水:______;
c.分离碳酸钙和水:______; d.分离植物油和水:______。
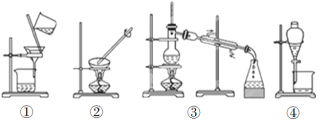
(4)装置②中玻璃棒的作用是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氮化合物在工农业生产中都有重要应用。
(1)氨和肼(N2H4)是两种最常见的氮氢化物。
己知:4NH3(g)+3O2(g) ![]() 2N2(g)+6H2O(g) ΔH1=-541.8kJ/mol,化学平衡常数为K1。N2H4(g)+O2(g)
2N2(g)+6H2O(g) ΔH1=-541.8kJ/mol,化学平衡常数为K1。N2H4(g)+O2(g) ![]() N2(g)+2H2O(g) ΔH2=-534kJ/mol,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为_________,该反应的化学平衡常数K=____(用K1、K2表示)。
N2(g)+2H2O(g) ΔH2=-534kJ/mol,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为_________,该反应的化学平衡常数K=____(用K1、K2表示)。
(2)对于2NO(g)+2CO(g) ![]() N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1molNO和0.3molCO,反应开始进行。
N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1molNO和0.3molCO,反应开始进行。
①下列能说明该反应已经达到平衡状态的是____(填字母代号)。
A.c(CO)=c(CO2) B.容器中混合气体的密度不变
C.v(N2)正=2v(NO)逆 D.容器中混合气体的平均摩尔质量不变
②图1为容器内的压强(P)与起始压强(P0)的比值(P/P0)随时间(t)的变化曲线。0~5min内,该反应的平均反应速率v(N2)= ____,平衡时NO的转化率为____。

(3)使用间接电化学法可处理燃煤烟气中的NO,装置如图2所示。已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式_________。用离子方程式表示吸收池中除去NO的原理__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com