
【题目】研究碳、氮、硫等元素化合物的性质或转化对建设生态文明、美丽中国具有重要意义.
(1)海水中无机碳的存在形式及分布如下图所示:
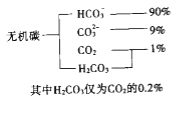
用离子方程式表示海水呈弱碱性的原因______________.已知春季海水pH=8.1,预测夏季海水碱性将会_____________(填写“增强”或“减弱”),理由是_________________________.
(2)工业上以CO和H2为原料合成甲醇的反应:CO(g)+2H2(g)CH3OH(g) △H<0,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇.如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系.下列说法正确的是_______________.
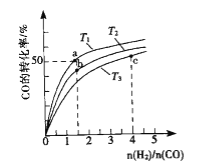
A.a、b、c三点H2转化率:c>a>b
B.上述三种温度之间关系为T1>T2>T3
C.a点状态下再通入0.5 mol co和0.5 mol CH3OH,平衡不移动
D.c点状态下再通入1 mol co和4mol H2,新平衡中H2的体积分数增大
(3)NO加速臭氧层被破坏,其反应过程如图所示:
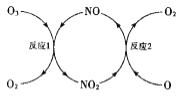
①NO的作用是___________________。
②已知:O3(g)+0(g)=202(g) △H=-143kJ·mol-l
反应1: O3(g)+NO(g)NO2(g)+O2(g) △H1=-200.2kJ·mol-l
反应2:热化学方程式为_____________________。
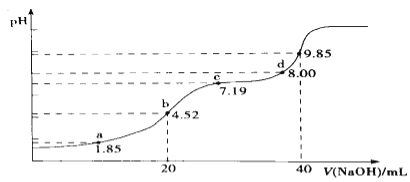
(4)大气污染物SO2可用NaOH吸收.已知pKa=-lgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19。该温度下用0.1mol· L-1 NaOH溶液滴定20mL0.1mol·L-1H2SO3溶液的滴定曲线如图所示.b点所得溶液中各离子浓度由大到小的顺序是________________;c点所得溶液中:c(Na+)___________3c(HSO3-)(填“>”、“<”或“=”).
【答案】HCO3-+H2O![]() H2CO3+OH-或CO32-+H2O
H2CO3+OH-或CO32-+H2O![]() HCO3-+OH- 增强 一方面水解平衡为吸热反应,夏天温度升高,平衡正向移动,c(OH-)增大,一方面夏天光合作用强,使得CO2+H2O
HCO3-+OH- 增强 一方面水解平衡为吸热反应,夏天温度升高,平衡正向移动,c(OH-)增大,一方面夏天光合作用强,使得CO2+H2O![]() H2CO3平衡逆向移动,酸性减弱,一方面夏天温度高,二氧化碳在水中的溶解度减小,酸性减弱 C 催化剂 NO2(g)+O(g)═NO(g)+O2(g)△H2=+57.2kJ/mol c(Na+)> c(HSO3-)> c(SO32-)>c(H+)>c(OH-) >
H2CO3平衡逆向移动,酸性减弱,一方面夏天温度高,二氧化碳在水中的溶解度减小,酸性减弱 C 催化剂 NO2(g)+O(g)═NO(g)+O2(g)△H2=+57.2kJ/mol c(Na+)> c(HSO3-)> c(SO32-)>c(H+)>c(OH-) >
【解析】
(1)本小题考查是盐类水解,强碱弱酸盐水解显碱性,强酸弱碱盐显酸性;水解平衡为吸热反应,夏天温度升高,水解平衡正向移动,溶液碱性增强;
(2)A.图中![]() 值:c>b,该值越大,即增大氢气浓度,正向进行程度越大,CO转化率增大,而氢气转化率减小,图中CO转化率:c>b,则H2转化率:b>c,a、b两点
值:c>b,该值越大,即增大氢气浓度,正向进行程度越大,CO转化率增大,而氢气转化率减小,图中CO转化率:c>b,则H2转化率:b>c,a、b两点![]() 相同,CO转化率越大,氢气转化率也越大,故氢气转化率:a>b;
相同,CO转化率越大,氢气转化率也越大,故氢气转化率:a>b;
B.图中![]() 一定时,CO的转化率:T1>T2>T3,正反应为放热反应,
一定时,CO的转化率:T1>T2>T3,正反应为放热反应,![]() 一定时,升高温度平衡逆向移动,CO的转化率会减小,故温度:T1<T2<T3;
一定时,升高温度平衡逆向移动,CO的转化率会减小,故温度:T1<T2<T3;
C.利用三段式求出T1温度下平衡常数K,在通入0.5 mol co和0.5 mol CH3OH 后求出Qc,比较K和Qc;
(3)①反应过程如图1是臭氧在NO作用下生成二氧化氮和氧气,二氧化氮在氧原子作用下生成NO和氧气;
②Ⅰ.O3(g)+O(g)═2O2(g)△H=-143kJ/mol
Ⅱ.O3(g)+NO(g)═NO2(g)+O2(g)△H1=-200.2kJ/mol
盖斯定律计算Ⅰ-Ⅱ得到反应2的热化学方程式;
(4)b点是用0.1molL-1NaOH溶液20ml滴定20mL0.1molL-1H2SO3溶液,恰好反应生成NaHSO3,溶液显酸性;c点pH=7.19=PKa2,依据平衡常数溶液显碱性,溶液中溶质主要为Na2SO3,SO32-+H2OHSO3-+OH-,Kh=![]() ,c(OH-)=
,c(OH-)=![]() ,带入计算得到:c(HSO32-)=c(SO32-),溶液中2n(Na)=3c(S),2c(Na+)=3[c(SO32-)+c(H2SO3)+c(HSO3-)]=3[c(H2SO3)+2c(HSO3-)],c(Na+)>3c(HSO3-)。
,带入计算得到:c(HSO32-)=c(SO32-),溶液中2n(Na)=3c(S),2c(Na+)=3[c(SO32-)+c(H2SO3)+c(HSO3-)]=3[c(H2SO3)+2c(HSO3-)],c(Na+)>3c(HSO3-)。
(1)海水中无机碳的存在形式主要是HCO3-、CO32-,两种离子为弱酸根离子,水解使海水显碱性,离子方程式为HCO3-+H2O![]() H2CO3+OH-或CO32-+H2O
H2CO3+OH-或CO32-+H2O![]() HCO3-+OH-;一方面水解平衡为吸热反应,夏天温度升高,平衡正向移动,c(OH-)增大,一方面夏天光合作用强,使得CO2+H2O
HCO3-+OH-;一方面水解平衡为吸热反应,夏天温度升高,平衡正向移动,c(OH-)增大,一方面夏天光合作用强,使得CO2+H2O![]() H2CO3平衡逆向移动,酸性减弱,一方面夏天温度高,二氧化碳在水中的溶解度减小,酸性减弱。本小题答案为:HCO3-+H2O
H2CO3平衡逆向移动,酸性减弱,一方面夏天温度高,二氧化碳在水中的溶解度减小,酸性减弱。本小题答案为:HCO3-+H2O![]() H2CO3+OH-或CO32-+H2O
H2CO3+OH-或CO32-+H2O![]() HCO3-+OH-;增强;一方面水解平衡为吸热反应,夏天温度升高,平衡正向移动,c(OH-)增大,一方面夏天光合作用强,使得CO2+H2O
HCO3-+OH-;增强;一方面水解平衡为吸热反应,夏天温度升高,平衡正向移动,c(OH-)增大,一方面夏天光合作用强,使得CO2+H2O![]() H2CO3平衡逆向移动,酸性减弱,一方面夏天温度高,二氧化碳在水中的溶解度减小,酸性减弱。
H2CO3平衡逆向移动,酸性减弱,一方面夏天温度高,二氧化碳在水中的溶解度减小,酸性减弱。
(2)A.图中![]() 值:c>b,该值越大,即增大氢气浓度,正向进行程度越大,CO转化率增大,而氢气转化率减小,图中CO转化率:c>b,则H2转化率:b>c,a、b两点
值:c>b,该值越大,即增大氢气浓度,正向进行程度越大,CO转化率增大,而氢气转化率减小,图中CO转化率:c>b,则H2转化率:b>c,a、b两点![]() 相同,CO转化率越大,氢气转化率也越大,故氢气转化率:a>b,可知H2转化率:a>b>c,故A错误;
相同,CO转化率越大,氢气转化率也越大,故氢气转化率:a>b,可知H2转化率:a>b>c,故A错误;
B.图中![]() 一定时,CO的转化率:T1>T2>T3,正反应为放热反应,
一定时,CO的转化率:T1>T2>T3,正反应为放热反应,![]() 一定时,升高温度平衡逆向移动,CO的转化率会减小,故温度:T1<T2<T3,故B错误;
一定时,升高温度平衡逆向移动,CO的转化率会减小,故温度:T1<T2<T3,故B错误;
C.T1温度下,a点![]() =1.5,起始时CO为1mol,则氢气为1.5mol,平衡时CO转化率为50%,反应的CO为0.5mol,容器体积为1L,则:
=1.5,起始时CO为1mol,则氢气为1.5mol,平衡时CO转化率为50%,反应的CO为0.5mol,容器体积为1L,则:
CO(g) + 2H2(g) CH3OH(g)
起始浓度(mol/L): 1 1.5 0
变化浓度(mol/L): 0.5 1 0.5
平衡浓度(mol/L):
故T1温度下平衡常数K=![]() ,而Qc=
,而Qc=![]() ,所以平衡不移动,故C正确;
,所以平衡不移动,故C正确;
D.c点状态下再通入1 molCO和4 molH2,等效为在原平衡的基础上压强增大一倍,正反应为气体体积减小的反应,故平衡正向移动,新平衡中H2的体积分数减小,故D错误。答案选C。
(3)①反应过程是臭氧在NO作用下生成二氧化氮和氧气,二氧化氮在氧原子作用下生成NO和氧气,反应过程中NO参与反应最后又生成,作用是催化剂。本小题答案为:催化剂。
②Ⅰ.O3(g)+O(g)═2O2(g)△H=143kJ/mol
Ⅱ.O3(g)+NO(g)═NO2(g)+O2(g)△H1=200.2kJ/mol
盖斯定律计算ⅠⅡ得到反应2的热化学方程式:NO2(g)+O(g)═NO(g)+O2(g)△H2=+57.2kJ/mol。本小题答案为:NO2(g)+O(g)═NO(g)+O2(g)△H2=+57.2kJ/mol。
(4)b点是用0.1molL-1NaOH溶液20ml滴定20mL0.1molL-1H2SO3溶液,恰好反应生成NaHSO3,溶液显酸性,则溶液中各离子浓度由大到小的顺序是c(Na+)> c(HSO3-)> c(SO32-)>c(H+)>c(OH-);c点pH=7.19=PKa2,依据平衡常数溶液显碱性,溶液中溶质主要为Na2SO3,SO32-+H2OHSO3-+OH-,Kh=![]() ,c(OH-)=
,c(OH-)=![]() ,带入计算得到:c(HSO32-)=c(SO32-),溶液中2n(Na)=3c(S),2c(Na+)=3[c(SO32-)+c(H2SO3)+c(HSO3-)]=3[c(H2SO3)+2c(HSO3-)],c(Na+)>3c(HSO3-)。本小题答案为:c(Na+)> c(HSO3-)> c(SO32-)>c(H+)>c(OH-);>。
,带入计算得到:c(HSO32-)=c(SO32-),溶液中2n(Na)=3c(S),2c(Na+)=3[c(SO32-)+c(H2SO3)+c(HSO3-)]=3[c(H2SO3)+2c(HSO3-)],c(Na+)>3c(HSO3-)。本小题答案为:c(Na+)> c(HSO3-)> c(SO32-)>c(H+)>c(OH-);>。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】某厂废酸主要含硫酸、Fe3+、Fe2+、TiO2+、Al3+ 。利用该废液制备过二硫酸铵[( NH4) 2S2O8]和TiO2的一种工艺流程如下:

已知:i.TiOSO4在热水中易水解生成H2TiO3,相关离子形成氢氧化物沉淀的pH范围如 下表:
金属离子 | TiO2+ | Fe3+ | Fe2+ | Al3+ |
开始沉淀的pH | 1.2 | 1.9 | 7.0 | 3.2 |
沉淀完全的pH | 2.8 | 3.1 | 9.4 | 4.7 |
ii. pH>7 时,Fe2+部分生成 Fe( Ⅱ)氨络离Fe(NH3)2]2+o
请回答下列问题:
(1)加入适量Fe的作用是________________ .
(2)生成TiO(OH)2的化学方程式为_______________ 。
(3)滤渣I、滤渣II均含有的物质的化学式为_____________ .
(4)加入H2O2的目的是除掉Fe( Ⅱ)氨络离子[Fe(NH3)2]2+,此过程中氧化剂与还原剂的物质的量之比理论上等于________ (填数值)。
(5)常温下,含硫微粒主要存在形式与pH的关系如下图所示。

用Pt电极电解饱和NH4HSO4溶液制备过二硫酸铵时,为满足在阳极放电的离子主要为 HSO4-,应调节阳极区溶液的pH范围在______之间,其电极反应式为____________ 。
(6)科研人员常用硫酸铁铵[NH4Fe(SO4)2]滴定法测定TiO2的纯度,其步骤为: 用足量酸溶解wg 二氧化钛样品,用铝粉做还原剂,过滤、洗涤,将滤液定容为100 mL,取 25.00 mL,以NH4SCN作指示剂,用标准硫酸铁铵溶液滴定至终点,反应原理为: Ti3++Fe3+=Ti4++Fe2+。
①判断滴定终点的方法:________________________ 。
②滴定终点时消耗c mol/L-1 NH4Fe(SO4)2溶液VmL,则TiO2纯度为___________(写岀相关字母表示的代数式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中的实验操作不能达到实验目的或得出相应结论的是
选项 | 实验操作 | 实验目的或结论 |
A | 向同pH、同体积的醋酸和盐酸溶液中加入足量镁粉,完全反应后收集H2的体积 | 比较两种酸的电离程度 |
B | 将混有Ca(OH)2杂质的 Mg(OH)2样品放入水中,搅拌,成浆状后,再加入饱和MgCl2溶液,充分搅拌后过滤,用蒸馏水洗净沉淀。 | 除去Mg(OH)2样品中的Ca(OH)2杂质 |
C | 向盛有1mL0.01mol/LAgNO3溶液的试管中滴加5滴0.01mol/L NaCl溶液,有白色沉淀生成,再滴加0.01mol/L NaI溶液,产生黄色沉淀。 | 常温下,Ksp(AgCl)>Ksp(AgI) |
D | 室温下,用pH试纸测得:0.1mol/LNa2SO3溶液pH约为10,0.1mol/LNaHSO3溶液pH约为5 | HSO3-结合H+的能力比SO32-的弱 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是用于治疗帕金森病的药物,名称为匹莫范色林,一种合成路线如图所示:
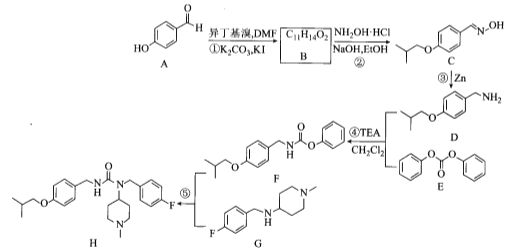
请回答下列问题:
(1)A的化学名称为_____________。
(2)B的结构简式为____________。
(3)D中官能团的名称是__________。
(4)③、⑤的反应类型分别为________、________。
(5)反应④的化学方程式为______________。
(6)芳香化合物X是E的同分异构体,X中含有两个苯环,能与FeCl3溶液发生显色反应也能发生银镜反应,其核磁共振氢谱显示有6种不同化学环境的氢,符合条件的X有:___种,写出其中一种的结构简式:________。
(7)已知: 。参考上述合成路线和信息,设计以化合物A和溴乙烷,乙醇为原料(无机试剂任选).制备
。参考上述合成路线和信息,设计以化合物A和溴乙烷,乙醇为原料(无机试剂任选).制备 的合成路线:______。
的合成路线:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含NH4NO3废水的原理如图所示,在直流电场的作用下,两膜中间的NH4+和NO2—可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.工作一段时间后,在两极区均得到副产品NH4NO3.下列叙述正确的是

A. a极为电源负极,b极为电源正极
B. c膜是阴离子交换膜,d膜是阳离子交换膜
C. 阴极电极反应式为2NO3-+12H++10e-=N2 +6H2O
D. 当电路中通过1mol电子的电量时,会有5.6LO2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,22.4L己烷中含有分子数目为NA
B. 1mol/LNaOH溶液中含有Na+数目为NA
C. 7.8gNa2O2中含有的共价键数目为0.1NA
D. 将0.5molN2O4充入密闭容器中充分反应转化成NO2的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备N2H4·H2O(水合肼)和无水Na2SO3主要实验流程如下:

已知:① 氯气与烧碱溶液的反应是放热反应;
② N2H4·H2O有强还原性,能与NaClO剧烈反应生成N2。
⑴从流程分析,本流程所用的主要有机原料为_______________(写名称)。
⑵步骤Ⅰ制备NaClO溶液时,若温度为41℃,测得产物中除NaClO外还含有NaClO3,且两者物质的量之比为5∶1,该反应的离子方程式为____________________。
⑶实验中,为使步骤Ⅰ中反应温度不高于40 ℃,除减缓Cl2的通入速率外,还可采取的措施是_________________。
⑷步骤Ⅱ合成N2H4·H2O(沸点约118 ℃)的装置如图。NaClO碱性溶液与尿素[CO(NH2)2](沸点196.6℃)水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。

① 使用冷凝管的目的是_________________。
② 滴液漏斗内的试剂是_______;
将滴液漏斗内的液体放入三颈烧瓶内的操作是______________________________;
③ 写出流程中生成水合肼反应的化学方程式________________________________。
⑸ 步骤Ⅳ制备无水Na2SO3(水溶液中H2SO3、HSO3-、SO32-随pH的分布如图所示)。

① 边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定停止通SO2的pH值为____(取近似整数值,下同);
②用制得的NaHSO3溶液再制Na2SO3溶液的pH应控制在________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下将0.2 mol/LHCl溶液与0.2 mol/LMOH溶液等体积混合,测得混合溶液的pH=6,则混合溶液中由水电离出的c(H+)__________0.2 mol/LHCl溶液中由水电离出的c(H+)。(填“>”“<”或“=”),该混合溶液的物料守恒式为 。
(2)常温下若将0.2 mol/LMOH溶液与0.1 mol/LHCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度__________MCl的水解程度。(填“>”“<”或“=”)
(3)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH__________。(填“>7”“<7”或“无法确定”)
(4)纯碱溶液呈碱性的原因(用离子方程式表示)__________________________,纯碱溶液离子浓度由大到小的顺序为 。
(5)某温度时,测得0.01 mol/L的NaOH溶液pH为11,在此温度下,将pH=a的NaOH溶液Va L与pH=b的硫酸Vb L混合。若所得混合溶液为中性,且a=12,b=2,求Va ∶Vb = 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA,下列叙述正确的是
A. 等质量的N2O和CO2中,分子数均为NA
B. 3.1g 31P与3.2g 32S中,中子数均为1.6NA
C. 0.4 mol BaCl2与0.4 mol Na2O2中,阴离子数均为0.8NA
D. 1mol正丁烷与1mol异丁烷中,化学键数均为14NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com