
【题目】已知氯化铝的熔点为190℃(2.202×l05Pa),但它在180℃即开始升华。
(1)氯化铝是____________。(填“离子化合物”或“共价化合物”)
(2)在500K和1.01×105Pa时,它的蒸气密度(换算为标准状况时)为11.92g·L-1,试确定氯化铝在蒸气状态时的化学式为____________。
(3)无水氯化铝在空气中强烈的“发烟”,其原因是__________。
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗
B.用排饱和氯化铵溶液的方法收集氨气
C.金属着火时,可用细沙覆盖灭火;电器设备引起的火灾,不可用泡沫灭火器灭火
D.在4mL0.1mol·L-1的K2Cr2O7溶液中滴加数滴1mol·L-1的NaOH溶液,溶液颜色从橙色变成黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮、硫、硒等元素的单质及其化合物有重要的科学研究价值。回答下 列问题:
(1)氰[化学式(CN)2]、硫氰[化学式(SCN)2]等与卤素单质性质相似,又称类卤素。(CN)2 中π键和σ键的数目之比为__________。沸点:(CN)2__________ (SCN)2(填“大于”、“等于”或“小于”),理由是__________。
(2)无机含氧酸的通式可写成(HO)mROn,如果成酸元素 R 相同,则 n 值越大,R 的正电性越高,在水中越容易电离出 H+。酸性强弱:HNO2____________HNO3(填“大于”、“等于”或“小于”);NO2-中氮原子的杂化方式为___________。
(3)一种硒单质晶体的晶胞为六方晶胞,原子排列为无限螺旋链,分布在六方晶格上,同一条链内原子作用很强,相邻链之间原子作用较弱,其螺旋链状图、晶 体结构图和晶体结构俯视图如下所示。

已知正六棱柱的边长为 a cm,高为 b cm,NA 表示阿伏加德罗常数,则该晶体的密度为__________g·cm-3(用含 NA、a、b 的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
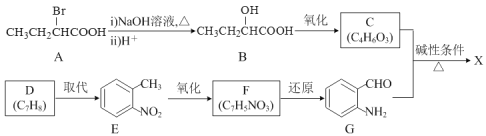
【题目】有机物X( ![]() )是重要的化工试剂,一种合成路线如下:
)是重要的化工试剂,一种合成路线如下:
已知:①RNH2+ ![]()
![]()
![]() +H2O
+H2O
② ![]() +H2O
+H2O
(1)D→E的反应试剂及条件是_____。
(2)F的结构简式为_____。
(3)一定条件下,HCHO与![]() 以等物质的量发生反应。可能生成的所有有机产物的结构简式有___。
以等物质的量发生反应。可能生成的所有有机产物的结构简式有___。
(4)有机物X的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:__。
①除苯环外无其他环状结构;
②能发生银镜反应,能与酸反应生成盐;
③核磁共振氢谱图中有4个峰。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
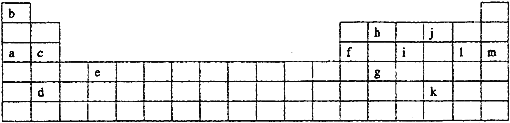
如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
A.原子核对核外电子的吸引力 B.形成稳定结构的倾向
下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1):
锂 | X | Y | |
失去第一个电子 | 519 | 502 | 580 |
失去第二个电子 | 7296 | 4570 | 1820 |
失去第三个电子 | 11799 | 6920 | 2750 |
失去第四个电子 | 9550 | 11600 |
(1)通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量_______________________________;
(2)表中X可能为以上13种元素中的______(填写字母)元素。用元素符号表示X和j形成化合物的化学式________;
(3)Y是周期表中_______族元素;
(4)以上13种元素中,_____(填写字母)元素原子失去核外第一个电子需要的能量最多。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅酸钠被列为“我国优先发展的精细化学品”和“今后我国无机化工产品发展重点”之一。如图是用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的工艺流程简图:
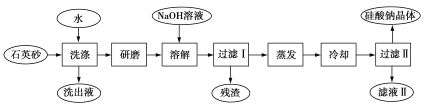
(1)要将洗出液中的溶质析出,采用的方法是蒸发结晶,则蒸发时用到的主要仪器有______。
(2)图中加入NaOH溶液,发生反应的离子方程式为______。
(3)洗涤石英砂的目的是______,过滤Ⅰ所得残渣为______(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅酸及其盐的叙述不正确的是( )
A.硅酸是一种弱酸,可由其酸性氧化物![]() 与水化合而制得
与水化合而制得
B.硅酸盐是构成地壳中岩石的主要成分,黏土的主要成分是硅酸盐
C.陶瓷材料是人类应用最早的硅酸盐材料
D.高温结构陶瓷、生物陶瓷是新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,元素周期表的第7周期已被填满。2017年,第113号、115号、117号和118号元素有了中文名称:鉨(![]() )、镆(
)、镆(![]() )、(
)、(![]() )、(
)、(![]() )。已知第113号元素与
)。已知第113号元素与![]() 元素同主族,根据元素周期律的知识,下列预测或说法合理的是( )
元素同主族,根据元素周期律的知识,下列预测或说法合理的是( )
A.![]() 的最高价氧化物对应的水化物可能具有两性
的最高价氧化物对应的水化物可能具有两性
B.![]() 在元素周期表中的位置是第7周期第VB族
在元素周期表中的位置是第7周期第VB族
C.![]() 的非金属性比I的弱
的非金属性比I的弱
D.![]() 在元素周期表的所有元素中非金属性最强
在元素周期表的所有元素中非金属性最强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com