
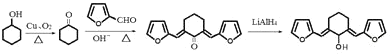
【题目】丁香酚存在于丁香花的花蕊中,以丁香酚为原料制取有机物 F 的路线如下:

已知:![]()
(1)丁香酚的分子式为_______。
( 2) A 中的含氧官能团是_______( 填名称), ② 的反应类型为_______。
(3)写出满足下列条件的 C 的所有同分异构体的结构简式_______。
①含苯环且环上只有两个取代基;
②属于酯类化合物;
③核磁共振氢谱有 3 组峰,且峰面积之比为 3∶1∶1。
(4)1 mol D 最多可以与_______molH2 发生加成反应。
(5)反应⑤中,试剂 X 的结构简式为_______。
(6)设计用呋喃甲醛( ![]() )和环己醇为原料制
)和环己醇为原料制 ![]() 的合成路线_______(无机试剂任选)。
的合成路线_______(无机试剂任选)。
【答案】C10H12O2 羟基、醚键 取代反应 ![]() 、
、![]() 4
4 ![]()
【解析】
(1)根据有机物的键线式书写分子式;(2)根据有机物的结构简式分析官能团的种类,根据有机反应的结构变化判断反应类型;(3)根据有机物的分子式及限制条件书写同分异构体;(4)根据双键与苯环的加成反应分析解答;(5)根据反应物和生成物的结构变化判断另一种反应物;(6)由反应产物和原料、题干进行对比,设计合成路线。
(1)根据丁香酚的键线式,可知其分子式为C10H12O2,故答案为:C10H12O2;
(2)从A的键线式判断该有机物的官能团为碳碳双键、羟基和醚键,含氧官能团只有羟基和醚键;根据A. B两种有机物的结构对比,结合另一反应物为(CH3CO)2O,从羟基变成酯基,得出该反应为取代反应,故答案为:羟基、醚键;取代反应;
(3)C的分子式为C10H10O4,根据信息中含有苯环,则取代基只剩下4个碳原子,且苯环上有两个取代基,其相对位置应该有邻位、间位和对位三种结构。又因其核磁共振氢谱为3组峰,峰面积比为3:1:1,它可能的同分异构体应该是邻位的两个相同的取代基,因为C是酯类化合物,故取代基为COOCH3或者OOCCH3,可以确定符合条件C的同分异构体结构简式为![]() 、
、![]() ,故答案为:
,故答案为:![]() 、
、![]() ;
;
(4)由D的结构简式可知,其分子中含有一个醛基,1分子醛基可以加成1分子H2,另外1分子苯环也可以加成3分子H2,1molD最多可以与4molH2发生加成反应,故答案为:4;
(5)反应⑤的条件与题给已知反应对应,对比D、 E的结构,发现E比2个D多了中间的三个碳原子,可以得出试剂X为![]() ,故答案为:
,故答案为:![]() ;
;
(6)由反应产物和原料、题干进行对比,可以得出该流程利用题给已知信息的反应。所以应先把环己醇转化为环己酮,再与![]() 进行反应,根据题干中反应⑥的转化,为了保护碳碳双键,使用LiAlH4还原得到目标产物而不是用H2进行加成,合成路线流程图为:
进行反应,根据题干中反应⑥的转化,为了保护碳碳双键,使用LiAlH4还原得到目标产物而不是用H2进行加成,合成路线流程图为: ,故答案为:
,故答案为: 。
。


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:
【题目】某![]() 的溶液X,其中可能含有
的溶液X,其中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的一种或几种,取200 mL该溶液进行实验,其现象及转化如图.
中的一种或几种,取200 mL该溶液进行实验,其现象及转化如图.
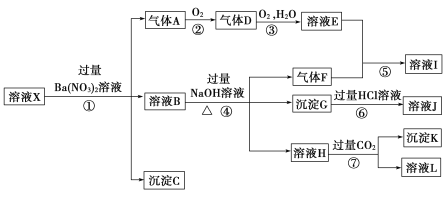
已知:反应过程中有一种气体是红棕色.
请回答下列问题:
(1)仅由强酸性条件便可判断溶液X中一定不存在的离子有________.
(2)溶液X中,关于![]() 的判断一定正确的是________(填字母).
的判断一定正确的是________(填字母).
a.一定有 b.一定没有 c.可能有
(3)①中产生气体A的离子方程式为_____________________________________________________.
(4)⑦中生成沉淀K的离子方程式为_____________________________________________________.
(5)溶液X中不能确定的离子是_____________________用实验证明该离子一定不存在的化学方法为______________________________________________________________________________________.
(6)若实验测定A.F.K均为![]() l,试确定沉淀C及其物质的量范围:_________.
l,试确定沉淀C及其物质的量范围:_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,有关物质的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数K | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)电解质由强至弱顺序为_________________(用化学式表示,下同)。
(2)常温下,0.02 mol·L-1的CH3COOH溶液的电离度约为 ,体积为10mLpH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者 后者(填“>”、“<”或“=”)。
(3)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的顺序为_____________。
(4)NaHSO3溶液显酸性的原因___________________________(离子方程式配适当文字叙述),其溶液中离子浓度由大到小的关系是_______________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向10 mL 0.1 mol/L醋酸溶液中加水稀释后,下列说法正确的是( )
A. 溶液中离子的数目减小
B. 再加入CH3COONa固体能促进醋酸的电离
C. 醋酸的电离程度增大,c(H+)亦增大
D. 溶液中c(CH3COO-)/c(CH3COOH)c(OH-)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d是淡黄色粉末,m为元素Y的单质,通常为无色、无味的气体。上述物质间的转化关系如图所示。下列说法错误的是( )

A.简单阴离子的还原性:Y>W
B.简单离子半径:Z<Y
C.简单气态氢化物的热稳定性:Y>X
D.W、Y、Z形成的化合物含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知HX和HY是两种一元弱酸,常温下用NaOH溶液分别滴定这两种弱酸溶液,若pKa=-lgKa,y=![]() 或lg
或lg![]() ,得到y和溶液pH的变化关系如图所示。下列有关叙述错误的是( )
,得到y和溶液pH的变化关系如图所示。下列有关叙述错误的是( )
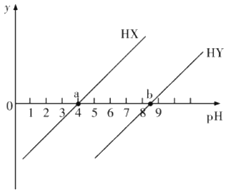
A.常温下,Ka(HX)=10-4,Ka(HY)=10-8.5
B.a点溶液中,c(X-)=c(HX)>c(Na+)>c(H+)>c(OH-)
C.常温下,0.1mol/LNaX溶液pH大于0.1mol/LNaY溶液的pH
D.往HY溶液中滴入NaOH溶液后所得的混合溶液中,![]() =10pH-pKa(HY)
=10pH-pKa(HY)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池为电源电解![]() 溶液,实验装置如图所示.下列关于此装置的说法中,正确的是( )
溶液,实验装置如图所示.下列关于此装置的说法中,正确的是( )

A.燃料电池工作时,负极反应为![]()
B.a极是石墨,b极是铜时,b极的电极反应为:![]()
C.a极是石墨,b极是纯铜时,电解一定时间后两极产生的气体体积都为![]() 标准状况
标准状况![]() ,则原溶液的浓度是
,则原溶液的浓度是![]()
D.a、b两极均是石墨时,若a极产生的气体为![]() 标准状况
标准状况![]() ,则U形管中溶液的PH为
,则U形管中溶液的PH为![]() 体积变化忽略不计
体积变化忽略不计![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于盐类水解反应的应用说法正确的是( )
A.可以把FeCl3固体直接溶于水制FeCl3溶液
B.热的纯碱溶液去油污效果好
C.Al(NO3)3溶液与K2S溶液混合后无明显现象
D.Mg粉投入到饱和NH4Cl溶液中无明显现象
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com