
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。

(1)实验过程中铜网出现红色和黑色交替的现象,请写出实验过程中总的化学方程式______________;在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是_______反应。(填“吸热”或“放热”).
(2)甲是热水浴,乙是冷水浴,但两个水浴作用不相同,①甲的作用是___________;②乙的作用是____________________________________。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是________________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还有___________ 。要除去该物质,可先在混合液中加入__________(填写字母),然后再通过蒸馏即可除去。
A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
【答案】2CH3CH2OH + O2 ![]() 2CH3CHO + 2H2O 放热 提供乙醇蒸气 冷却产生的乙醛等气体 乙醛、乙醇、水 乙酸 C
2CH3CHO + 2H2O 放热 提供乙醇蒸气 冷却产生的乙醛等气体 乙醛、乙醇、水 乙酸 C
【解析】
(1)乙醇的催化氧化反应实质是:金属铜被氧气氧化为氧化铜,氧化铜将乙醇氧化为乙醛,金属铜起催化剂作用;熄灭酒精灯,反应仍能继续进行,说明反应放热;
(2)甲为热水浴,乙为冷水浴,结合实验的原理分析解答;
(3)根据物质的沸点高低不同来确定获得的物质;
(4)能使紫色石蕊试纸变红,说明该物质显酸性,结合乙酸的性质和选项是否反应分析判断。
(1)铜与氧气反应生成黑色的氧化铜,氧化铜与乙醇发生氧化反应生成铜和乙醛、水,反应的方程式:2Cu+O2![]() 2CuO,CH3CH2OH+CuO
2CuO,CH3CH2OH+CuO![]() CH3CHO+Cu+H2O,反应的总反应方程式为2CH3CH2OH + O2
CH3CHO+Cu+H2O,反应的总反应方程式为2CH3CH2OH + O2![]() 2CH3CHO + 2H2O;熄灭酒精灯,反应仍能继续进行,说明该乙醇的氧化反应是放热反应,放出的热量足以维持反应进行,故答案为:2CH3CH2OH + O2
2CH3CHO + 2H2O;熄灭酒精灯,反应仍能继续进行,说明该乙醇的氧化反应是放热反应,放出的热量足以维持反应进行,故答案为:2CH3CH2OH + O2![]() 2CH3CHO + 2H2O;放热;
2CH3CHO + 2H2O;放热;
(2)甲和乙两个水浴作用不相同,甲是热水浴,作用是乙醇平稳气化成乙醇蒸气,乙是冷水浴,目的是将乙醛冷却下来,故答案为:提供乙醇蒸气;冷却产生的乙醛等气体;
(3)乙醇的催化氧化实验中的物质:乙醇、乙醛和水的沸点高低不同,在试管a中能收集这些不同的物质,故答案为:乙醛、乙醇、水;
(4)若试管a中收集到的液体用蓝色石蕊试纸检验,试纸显红色,说明溶液呈酸性,则溶液中含有乙酸;乙酸具有酸的通性,四个选择答案中,只有碳酸氢钠可以和乙酸反应,生成乙酸钠、水和二氧化碳,然后再通过蒸馏即可分离除去乙酸,故答案为:乙酸;C。


科目:高中化学 来源: 题型:
【题目】下列离子方程式表达不正确的是 ( )
A. 向FeCl3溶液滴加HI溶液:2Fe3++2I-== 2Fe2++I2
B. CuSO4溶液吸收H2S 气体:Cu2++H2S == CuS↓+2H+
C. 用氢氧化钠溶液吸收工业废气中的NO2:2NO2+2OH- == NO![]() +NO
+NO![]() +H2O
+H2O
D. 向NH4Al(SO4)2溶液中滴加少量Ba(OH)2溶液:2NH4++Ba2++SO42-+2OH—= BaSO4↓+2NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前世界上海水淡化的主要方法有蒸馏法、电渗析法、反渗透法等。电渗析法是在直流电源作用下通过离子交换膜对海水进行处理(原理如图所示);反渗透法是利用压强差使海水一侧的水分子通过渗透膜进入淡水一侧,从而得到淡水和浓缩的盐溶液(原理如图所示)。下列说法正确的是
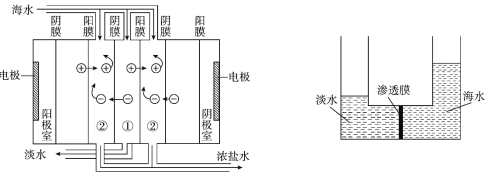
A. 蒸馏法、电渗析法、反渗透法均不发生化学反应
B. 反渗透法所用渗透膜的微孔直径范围是1~100nm
C. 蒸馏法具有设备简单、成本低等优点
D. 浓缩的盐溶液可用于提取或制备食盐、镁、溴等物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有CaCl2、MgCl2、Na2SO4以及泥沙等杂质,以下是制备精盐的实验方案,步骤如下图:
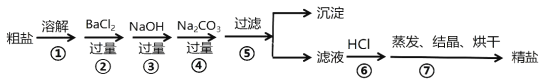
(1)第②步操作的目的是除去粗盐中的______________;( 填化学式,下同)
(2)图中“沉淀”的成分是:____________、_____________、____________、_____________;
(3)第④步操作的目的是除去________________、_________________;写出相应的离子反应方程式:_______________________;_________________________;
(4)第⑥步操作的目的是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锆(Zr)是40号元素,位于第五周期ⅣB族,锆可溶于氢氟酸和王水,锆及其化合物在陶瓷、耐火材料等多个领域有着重要用途。请回答下列相关问题。
(1)基态锆原子的价电子排布图(轨道表示式)是___。
(2)ZrSiO4和ZrSiO3是锆的两种硅酸盐,二者含有的阳离子Zr4+和Zr2+中比较稳定的是____,原因是___。SiO32-的空间构型是____,SiO42-中的Si原子的杂化类型是____。
(3)[Zr(C2H5O)2]2+是Zr4+形成的一种配离子,其中的配位原子是___(填元素符号),该离子中含有的化学键种类不包括___(填选项序号)。
A.极性键 B.非极性键 C.σ键 D.π键
(4)立方氧化锆是一种人工合成的氧化物,由于硬度极高且外观接近钻石常被用作钻石的替代品,其晶胞结构如图所示,立方氧化锆的化学式是___,锆原子的配位数是____。若晶胞中距离最近的两个氧原子间的距离为anm,则立方氧化锆的密度为__g/cm3。
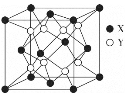
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,下列叙述正确的是
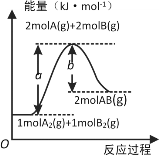
A. 形成2molA-B键,吸收b kJ能量
B. 每生成2分子AB吸收bkJ热量
C. 反应物的总能量低于生成物的总能量
D. 该反应热ΔH=(b-a)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是 ( )
A. 氯化钙溶液中通入CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+
B. 以石墨作电极电解氯化铝溶液:2Cl-+ 2H2O![]() 2OH-+ H2↑+ Cl2↑
2OH-+ H2↑+ Cl2↑
C. Ca(C1O)2溶液中通人过量的SO2气体:ClO-+SO2+H2O=HSO3-+HClO
D. 向明矾溶液中加入氢氧化钡溶液至沉淀的质量最大:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HCl的相对分子质量为_________,HCl的摩尔质量为__________。49 g H2SO4的物质的量为 ____________;它与 _______gH2O含相同氧原子;与________L(标准状况)的CO2 相同分子数;与_____________个CO含相同氧原子数。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z都是元素周期表中前四周期的元素,他们的原子序数依次增大,并且不在同一个周期。元素X的原子核外有8个运动状态不同的电子。元素Y基态原子的最外电子层没有空轨道,而且成对电子数是未成对电子数的2倍。元素Z基态原子的内层轨道全部排满电子,且最外层电子数为2。
(1)基态X原子的核外电子排布图(轨道表达式)为_________,X的氢化物在乙醇中的溶解度大于Y的氢化物,其原因是________________________。
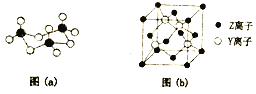
(2)X与Y形成的固体YX3中存在(a)所示的三聚分子,该分子中Y原子的杂化轨道类型为_______。基态Y原子中,核外能级最高的原子轨道上,具有的电子数为______。
(3)X与Y还可以形成YX42-离子,YX42-的空间构型为_________,写出一种与YX42-互为等电子体的分子的化学式________。
(4)Z与Y的离子形成化合物晶体的晶胞如图(b)所示。在晶胞中,Z离子的配位数为_________,该化合物的化学式为______。
(5)Z的氯化物与氨水反应可形成配合物[Z(NH3)4]Cl2,1mol该配合物中含有![]() 键的数目为_______。
键的数目为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com