
【题目】有机玻璃(聚甲基丙烯酸甲酯、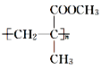 )广泛应用于商业、轻工业、建筑、化工甚至人工角膜等方面,下面是工业上由丙酮为起始反应物合成有机玻璃的一种路线图,请回答下列问题:
)广泛应用于商业、轻工业、建筑、化工甚至人工角膜等方面,下面是工业上由丙酮为起始反应物合成有机玻璃的一种路线图,请回答下列问题:
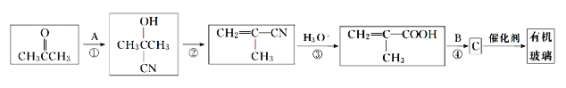
(1)A的化学式为__________;B的名称是_______。
(2)反应①、②的反应类型分别是____________、___________。
(3)下列有关![]() 的说法错误的是________(填字母)。
的说法错误的是________(填字母)。
a.分子中所有碳原子均在同一平面上 b.能使溴水、酸性KMnO4溶液褪色
c.与丙酸互为同系物 d.能与新制的Cu(OH)2悬浊液反应
(4)写出反应④的化学方程式:_____________。
(5)C有多种同分异构体,其中满足下列条件的有______种(不包含C),在这些同分异构体中,核磁共振氢谱有3组峰的物质的结构简式为_______________。
①能发生水解反应但不能发生银镜反应; ②能使溴的CCl4溶液褪色。
【答案】HCN 甲醇 加成 消去反应 c CH2=C(CH3)COOH+CH3OH![]() CH2=C(CH3)COOCH3+H2O 7 CH3COOC(CH3)=CH2
CH2=C(CH3)COOCH3+H2O 7 CH3COOC(CH3)=CH2
【解析】
丙酮和A为加成反应,从产物中的结构简式来看,丙酮的羰基的双键打开,与HCN加成,随后消去一分子的水,生成双键,氰基再水解,生成羧酸,与甲醇生成酯,得到有机玻璃的单体,再加聚得到高分子化合物。
(1)丙酮与A发生加成反应,利用化学式减去丙酮的分子式,即可得到A的化学式,A为HCN;根据有机玻璃高分子化合物的链节,知道B为甲醇。答案为HCN 甲醇;
(2)反应①为丙酮与HCN发生加成反应,反应②发生的是醇类的消去反应。答案为加成反应 消去反应;
(3)a.分子中有双键,且C原子与碳碳双键的C相连,根据乙烯分子的六原子共面结构可知,分子中所有碳原子均在同一平面上,a不符合题意; b.分子中有碳碳双键,能使溴水、酸性KMnO4溶液褪色,b不符合题意;c.同系物之间的官能团的种类和数目都相同,丙酸中没有碳碳双键,两者不能互称同系物,c符合题意; d.分子中有羧基,能与碱反应,所以能与新制的Cu(OH)2悬浊液反应,d项不符合题意,答案为c;
(4)反应④为2-甲基丙烯酸与甲醇的酯化反应,答案为CH2=C(CH3)COOH+CH3OH![]() CH2=C(CH3)COOCH3+H2O;
CH2=C(CH3)COOCH3+H2O;
(5)C为甲基丙烯酸甲酯[CH2=C(CH3) COOCH3],其同分异构体要满足以下条件:能发生水解,但是不能发生银镜反应,说明有酯基,但不是甲酸酯。能使溴的CCl4溶液褪色,说明有碳碳双键。分子中共5个碳原子,第一种情况:酸中有2个碳原子、醇中有3个碳原子,碳碳双键只能在醇中,这样的酯一共有3种,分别为CH2=CHCH2OOCCH3、CH3CH=CHOOCCH3、CH2=C(CH3)OOCCH3;第二种情况:酸中有3个碳原子、醇中有2个碳原子,碳碳双键可以在酸中、也可以在醇中,这样的酯有2种,CH2=CHCOOCH2CH3、CH3CH2COOCH=CH2;第三种情况,酸中有4个碳原子、醇中有1个碳原子,碳碳双键在酸中,CH3CH=CHCOOCH3、CH=CHCH2COOCH3,共2种。综上所述,满足条件的C的同分异构体共有7种。其中核磁共振氢谱有3组峰的为CH2=C(CH3)OOCCH3;答案为7 CH2=C(CH3)OOCCH3。


 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
【题目】如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条;F中为红色的铜网,其右端出气管口放有脱脂棉。
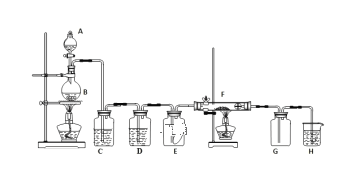
(1)装置C中盛装的溶液是___,D中试剂的作用是___。
(2)写出F中反应的化学反应方程式:__ ,其反应现象为___。
(3)H中的试剂为____,用来吸收多余氯气。该反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氧化性: Cl2>Br2>Fe3+>I2,则下列离子方程式正确的是:
A. 少量氯气与FeBr2溶液反应Cl2+2Br-=2C1-+Br2
B. 过量氯气与FeBr2溶液反应Cl2+Fe2++2Br-=2Cl-+Br2+Fe3+
C. 氯气与FeBr2溶液以物质的量1:1反应2Cl2+2Fe2++2Br-=4Cl-+Br2+2Fe3+
D. 少量氯气与FeI2溶液反应Cl2+2Fe2+=2Cl-+2Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合图回答问题:如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
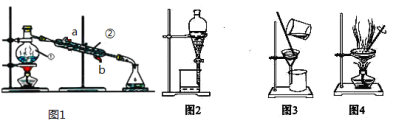
(1)写出上述装置中仪器的名称:①________。
(2)若利用上述装置分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的仪器有________,图1中仪器 ②是从______口进水(填a或b)。
(3)图2在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是______
(4)从氯化钾溶液中得到氯化钾固体,选择装置______(填代表装置图的序号,下同);除去自来水中的Cl等杂质,选择装置______。
(5)实验室常用上述装置分离碘水中的碘,进行该操作时,需在碘水中加一试剂,在选择试剂时,下列性质你认为哪些性质是必需的:________(填序号)。
①常温下为液态 ②I2在其中溶解程度大 ③与水互不相容 ④密度要比水大。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)键线式![]() 的名称是_______。
的名称是_______。
(2)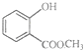 中含有的官能团的名称为_________、________。
中含有的官能团的名称为_________、________。
(3)C5H12的某种同分异构体只有一种一氯代物,写出它的结构简式______。
(4)某炔烃和氢气充分加成产物为2,5-二甲基己烷,该炔烃的结构简式是____________。
(5)某芳香烃结构为![]() 。它的分子式为________,一氯代物有______种。
。它的分子式为________,一氯代物有______种。
(6)分子式为C6H12的某烃的所有碳原子都在同一平面上,则该烃的结构简式为_________。若分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为__________。
(7)分子式为C8H10的芳香烃,苯环上的一氯代物只有一种,该芳香烃的结构简式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用如图装置进行铁与水蒸气反应的实验,并检验产物的性质,请回答下列问题:
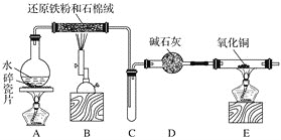
(1)A装置的作用是____________,烧瓶底部放碎瓷片的作用是_____________。
(2)装置B中发生反应的化学方程式是____________________________________,该反应中氧化剂是__________,氧化产物是_____________。
(3)D的作用是____________________________。
(4)E中的实验现象是_____________________。
(5)该同学对反应后硬质试管中固体物质的组成提出了如下假设:
假设1:只有Fe;
假设2:只有________;
假设3:既有Fe也有Fe3O4。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)某工厂排放出有毒物质NOCl,它遇水就会生成NO3-。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_____。水源中的NO3-对人类健康会产生危害。为了降低水源中NO3-的浓度,有研究人员建议在碱性条件下用铝粉将NO3-还原为N2,该反应的离子方程式为____
(二)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,发生反应的化学方程式为:2FeCl3+Cu==2FeCl2+CuCl2。实验小组的同学对生产印刷电路板的废液成分进行了如下探究:
①取少量废液,滴加KSCN溶液显红色。
②取100mL废液,加入足量的AgNO3溶液,析出沉淀43.05g。
③另取100mL废液,加入一定质量的铜片,充分反应后,测得铜片的质量减少了2.56g,再向反应后的溶液中滴加KSCN溶液不变色。
根据探究实验得出结论:
(1)废液中含有的金属离子是______。
(2)100mL废液中Cl-的物质的量是______。
(3)原100mL废液中铜离子的物质的量浓度是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A. 标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA
B. 标准状况下,2.24L NO和2.24L O2混合后气体分子数为0.15 NA
C. 加热条件下,1mol Fe投入足量的浓硫酸中,生成NA个SO2分子
D. 0.1mol Na2O2与足量的潮湿的二氧化碳反应转移的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室里,用足量的浓盐酸与一定量的MnO2反应,来制取氯气。
⑴用“双线桥法”标出电子转移情况
MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
⑵若生成2.24L标准状况时的氯气,请计算(写出必要的计算过程):
①理论上需要多少克MnO2参加反应?
②被氧化的HCl的物质的量为多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com