
【题目】对恒温恒容密闭容器中的可逆反应:A(s)+3B(g)![]() 2C(g) ΔH<0,下列叙述正确的是( )
2C(g) ΔH<0,下列叙述正确的是( )
A.升高温度,v(逆)增大,v(正)减小
B.增大压强,v(正)增大,v(逆)减小
C.增大A的物质的量,v(正)增大,v(逆)减小
D.采用催化剂,降低反应活化能,v(正)、v(逆)同时增大,且增大的倍数相同
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的△H前者小于后者的有( )
①C(s)+O2(g)═CO2(g) △H1 C(s)+![]() O2(g)═CO(g) △H2
O2(g)═CO(g) △H2
②S(s)+O2(g)═SO2(g) △H3 S(g)+O2(g)═SO2(g) △H4
③2H2(g)+O2(g)═2H2O(l) △H5 2H2(g)+O2(g)═2H2O(g) △H6
④CaCO3(s)═CaO(s)+CO2(g) △H7 CaO(s)+H2O(l)═Ca(OH)2(s) △H8
⑤![]() H2SO4(浓)+NaOH(aq)=
H2SO4(浓)+NaOH(aq)=![]() Na2SO4(aq)+H2O(l) ΔH9CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH10
Na2SO4(aq)+H2O(l) ΔH9CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH10
⑥N2O4(g)![]() 2NO2(g) △H11 2NO2(g)
2NO2(g) △H11 2NO2(g)![]() N2O4(g) △H12
N2O4(g) △H12
A.2项B.3项C.4项D.5项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)比较氧化性相对强弱:Cl2_______I2(填“)”>“<”或“=”);用一个离子方程式说明Cl2和I2氧化性的相对强弱_______。
(2)NH5是离子化合物,各原子最外层满足稳定结构。写出NH5的电子式__________。
(3)请用系统命名法对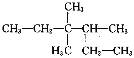 命名__________。
命名__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含+6价铬的废水毒性强,对环境污染严重,工业上常利用化学原理把+6价铬转化为不溶性Cr(OH)3除去。
Ⅰ、SO2还原法:化工厂常用SO2处理含铬废水,其工艺流程如下图所示:
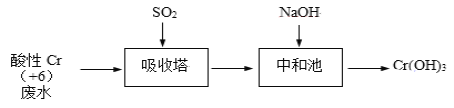
已知:Cr2O72- + H2O ![]() 2CrO42- + 2H+,吸收塔中 Cr2O72-与SO2反应如下:Cr2O72﹣(aq)+3SO2(g)+2H+(aq)═2Cr3+(aq)+3SO42﹣(aq)+H2O(l) ΔH = -1145 kJ/mol。
2CrO42- + 2H+,吸收塔中 Cr2O72-与SO2反应如下:Cr2O72﹣(aq)+3SO2(g)+2H+(aq)═2Cr3+(aq)+3SO42﹣(aq)+H2O(l) ΔH = -1145 kJ/mol。
(1)其他条件不变,研究吸收塔中pH对反应的影响。
pH | 2 | 4 | 6 |
Cr(+6)最大去除率 | 99.99%达排放标准 | 99.95%达排放标准 | 99.5%未达排放标准 |
时间 | 30 min | 35 min | 45 min |
①由上述数据获得的结论有_________。
②实际工业生产控制pH = ____左右。
③下列说法不合理的是_____。
a.该酸性含铬废水中一定含有CrO42-,pH越大其含量越高
b.其他条件不变,增大压强,吸收塔中反应的K增大,有利于除去Cr(+6)
c.理论上看,SO32-、Fe2+等也可以用于除去Cr(+6)
(2)其他条件不变,研究温度对Cr(+6)去除率的影响(如图所示)。
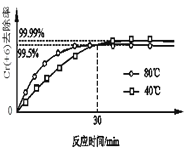
已知:30min前相同时间内,80℃的Cr(+6)去除率比40℃高,是因为30min前反应正向进行,温度高反应速率快反应物的转化率增大;试解释30min后80℃的Cr(+6)去除率低的原因:________。
Ⅱ、电解法处理:
工业上处理含Cr2O72-离子的酸性废水,采用往工业废水中加入适量的食盐,再用Fe为电极进行电解,将Cr2O72—离子还原为可溶性三价铬离子,再调pH使三价铬离子变为不溶性氢氧化物除去。
(1)加入食盐的目的是 _______;
(2)电解时阳极反应式为 _________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列生产、生活等实际应用,不能用勒沙特列原理解释的是( )
A.冰镇的啤酒打开后泛起泡沫
B.实验室中常用排饱和食盐水的方法收集Cl2
C.工业合成氨时选择高温能极大加快反应速率
D.工业生产硫酸的过程中使用过量的空气以提高SO2的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.乙酸和乙醇在浓硫酸作用下可以发生加成反应
B.分子式为C4H9Cl的同分异构体有4种
C.甲醇、乙二醇、丙三醇互为同系物
D.聚乙烯塑料可用于食品的包装,该塑料的老化是由于发生了加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列各项叙述的判断及理由正确的是
选项 | 叙述 | 判断及理由 |
A | 糖类和油脂完全燃烧的产物是CO2和水 | 正确.糖类和油脂的组成元素是C、H、O |
B | 一定条件下乙醇、甲烷均能发生取代反应 | 错误.乙醇不能发生取代反应 |
C | 淀粉和纤维素是同分异构体 | 正确.淀粉和纤维素的化学式均为(C6H10O5)n |
D | 若乙烯中混有SO2气体,可通过酸性高锰酸钾溶液除去 | 正确.酸性条件下SO2可被高锰酸钾氧化 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是![]()
A.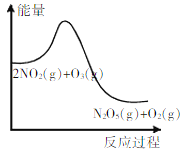 图所示的反应,若升高温度,该反应的平衡常数变小
图所示的反应,若升高温度,该反应的平衡常数变小
B.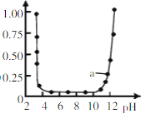 图所示的是
图所示的是![]() 与
与![]() 反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在
反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在![]()
C.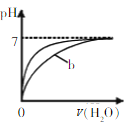 表示等pH的盐酸与醋酸中分别加水稀释的pH变化,其中曲线b对应的是盐酸
表示等pH的盐酸与醋酸中分别加水稀释的pH变化,其中曲线b对应的是盐酸
D.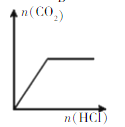 表示向
表示向![]() 溶液中逐滴加稀盐酸,生成
溶液中逐滴加稀盐酸,生成![]() 与所甲盐酸物质的量的关系
与所甲盐酸物质的量的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某烃的结构简式是![]() ,分子中饱和碳原子数为 _________,可能在同一平面上的碳原子数最多为 _________
,分子中饱和碳原子数为 _________,可能在同一平面上的碳原子数最多为 _________
(2)从某些植物树叶提取的挥发油中含有下列主要成分:
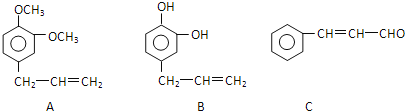
①C的含氧官能团名称为______。
②在这三种物质中,_______显酸性,________能发生银镜反应(填A、B或C)
③这三种物质都不能发生的反应有 __________。
A. 氧化反应 B.取代反应 C.消去反应 D.还原反应
④1 mol A与足量的浓溴水充分反应,消耗溴单质的物质的量为______ 。
⑤C发生加聚反应的产物的结构简式为_______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com