
【题目】下列变化中,需要加入还原剂才能发生的是( )
A. Cl→Cl2 B. FeCl3→FeCl2 C. C→CO2 D. KMnO4→MnO2
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】中科院宁波材料所研发金属空气电池获得重大突破.该电池的工作原理如图所示:下列有关说法正确的是( )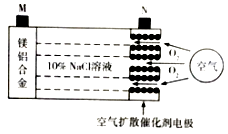
A.电池工作时,负极附近溶液的pH升高
B.电池工作时,电流由M极经外电路流向N极
C.电路中转移2mol电子,理论上约消耗标准状况下空气56L
D.电池总反应为4Al+3O2=2Al2O3、2Mg+O2=2MgO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素A、B、C都是短周期元素,A元素原子的2p轨道上只有两个未成对电子,B的3p轨道上有空轨道,A、B同主族,B、C同周期,C是本周期中电负性最大的.请回答:
(1)A原子的核外电子排布图 , B原子的核外电子排布式 , C原子的价电子排布式 .
(2)A,B,C的气态氢化物的化学式分别是 , 其中最不稳定的是 .
(3)它们的最高价氧化物的水化物中,酸性最强的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.从海水中可提取多种化工原料,下面是工业上对海水的几项综合利用的示意图。

(1)海水中所得粗盐中含Ca2+、Mg2+、SO42-等杂质,为了得到精盐,下列试剂加入的先后顺序正确的是_______
A. BaCl2→Na2CO3→NaOH→HCl B. NaOH→BaCl2→Na2CO3→HCl
C. Na2CO3→NaOH→BaCl2→HCl D. BaCl2→NaOH→Na2CO3→HCl
(2)为了检验精盐中是否含有SO42-,正确的方法是____________________________。
(3)写出电解饱和NaCl溶液的化学方程式____________________________________。
Ⅱ.海藻中提取碘的流程如图:

(4)指出提取碘的过程中有关实验操作名称:①__________,③___________;
(5)步骤②反应的离子方程式为_______________________________。
(6)下列关于海藻提取碘的说法,正确的是_____________
A.海藻的灼烧可以在蒸发皿中进行
B.含碘的有机溶液呈现出紫红色
C.操作③中先放出下层液体,然后再从下口放出上层液体
D.蒸馏操作时,温度计的水银球应伸入液面以下但不能触碰到蒸馏烧瓶的底部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,将xmL pH=a的稀NaOH溶液与ymL pH=b的稀盐酸充分反应.下列关于反应后溶液pH的判断,正确的是( )
A.若x=y,且a+b=14,则pH>7
B.若10x=y,且a+b=13,则pH=7
C.若ax=by,且a+b=13,则pH=7
D.若x=10y,且a+b=14,则pH>7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜器久置,表面会生成一层绿色固体,为了解铜在空气中的腐蚀情况,某化学兴趣小组收集家中铜器表面的绿色固体进行探究.查阅相关资料后,猜想该绿色物质可能是铜的碳酸盐. 该小组同学利用如图装置进行实验.
①对试管内的绿色固体进行加热,至完全分解,观察到A装置中绿色固体逐渐变成黑色,B装置中无水硫酸铜变成蓝色,C装置中澄清石灰水变浑浊.
②取少量加热后生成的黑色固体于试管中,加入稀硫酸.观察到黑色固体逐渐溶解,溶液变成蓝色.
③取少量上述蓝色溶液加入试管中,浸入一根洁净的铁丝.观察到铁丝表面有红色物质析出.
请回答下列问题:
(1)绿色固体中含有的元素是 .
(2)加热后试管中剩余的黑色物质是 .
(3)假设该绿色物质是一种纯净物,则其化学式可能是 , 加热分解的化学方程式为 .
(4)上述实验步骤③中的反应的离子方程式为 .
(5)实验装置最后的干燥管的作用是 .
(6)如果将B、C两装置对调,能否达到实验目的? , 为什么? .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氢化钾(KH)属于离子化合物,KH跟水反应可以放出氢气.下列说法中正确的是( )
A.KH的水溶液呈碱性
B.KH中氢离子可以被还原为氢气
C.KH是一种强氧化剂
D.KH中的氢离子是裸露的质子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某Na2O2 固体中因吸收CO2 而含有少量Na2CO3,经实验测定样品中Na2O2的质量分数为88.0%。现称取该样品8.86g,加入水充分反应后放出气体,所得溶液体积为500mL。试计算:(要求:写出解题过程,计算结果保留两位小数)
(1)上述反应所得气体在标准状况下的体积;_________
(2)反应后溶液中Na+的物质的量浓度。_______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com