
【题目】用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量10.0g含有少量中性易溶杂质的样品,配成500mL待测溶液。 用0.100mol![]() L-1硫酸滴定,写出该中和反应的热化学方程式______________________(中和热ΔH=-57.3 kJ/mol)。
L-1硫酸滴定,写出该中和反应的热化学方程式______________________(中和热ΔH=-57.3 kJ/mol)。
(2)将该烧碱样品配成500mL待测溶液需要的玻璃仪器有________________________。
(3)滴定过程中,眼睛应注视_________________________,若用酚酞作指示剂达到滴定终点颜色变化是______________________________________________________。
(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是________molL-1,烧碱样品的纯度是___________。
滴定次数 | 待测溶液 体积(mL) | 标准酸体积 | |
滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 4.10 | 24.00 |
(5)下列实验操作会对滴定结果产生什么后果?(填“偏高”“偏低”或“无影响”)
① 观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果____________。
② 若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果____________。
【答案】 2NaOH(aq)+H2SO4(aq)=2H2O(l) +Na2SO4 (aq) △H= -114.6kJ·mol—1或者 H+ (aq) + OH- (aq) = H2O(l) △H= -57.3kJ·mol—1 量筒、烧杯、玻璃棒、500 mL容量瓶、胶头滴管 锥形瓶内溶液颜色变化 溶液由浅红色变成无色,且半分钟内不恢复原色 0.400 80.0% 偏高 偏高
【解析】(1)可以用化学方程式表示,也可以用离子方程式表示;
(2)配制一定物质的量浓度的溶液步骤有:计算、称量、溶解、冷却转移、洗涤转移、定容、摇匀,据此分析解答;
(3)根据中和滴定的操作和滴定终点判断方法解答;
(4)根据c(待测)×V(待测)═c(标准)×V(标准)计算,V(标准)用两次的平均值;再根据m=cVM计算500mL溶液中氢氧化钠的质量,计算质量分数;
(5)根据c(待测)=![]() 分析误差。
分析误差。
(1)氢氧化钠与硫酸反应的热化学方程式为2NaOH(aq)+H2SO4(aq)==2H2O(l) +Na2SO4 (aq) △H= -114.6kJ·mol—1或者 H+ (aq) + OH- (aq) == H2O(l) △H= -57.3kJ·mol—1,故答案为:2NaOH(aq)+H2SO4(aq)==2H2O(l) +Na2SO4 (aq) △H= -114.6kJ·mol—1或者 H+ (aq) + OH- (aq) == H2O(l) △H= -57.3kJ·mol—1;
(2)配制一定物质的量浓度的溶液步骤有:计算、称量、溶解、冷却转移、洗涤转移、定容、摇匀。将该烧碱样品配成500mL待测溶液需要的玻璃仪器有:量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管,故答案为:量筒、烧杯、玻璃棒、500 mL容量瓶、胶头滴管;
(3)滴定过程中,眼睛应注视锥形瓶内溶液颜色变化,若用酚酞作指示剂,判断滴定终点的方法:滴入最后一滴NaOH溶液时,溶液刚好由无色变为粉红(或由黄色变为橙色),且半分钟内不变色,故答案为:锥形瓶内溶液颜色变化;溶液由浅红色变成无色,且半分钟内不变色;
(4)V(标准)=[(20.50-0.40)+(24.00-4.10)]mL÷2=20.00mL,硫酸的浓度为0.100mol![]() L-1,则氢离子浓度为0.200mol
L-1,则氢离子浓度为0.200mol![]() L-1,
L-1,
c(待测)═![]() =
=![]() ═0.4000molL-1,m(烧碱)═cVM═0.4000molL-1×0.5L×40g/mol═8.0g,ω═
═0.4000molL-1,m(烧碱)═cVM═0.4000molL-1×0.5L×40g/mol═8.0g,ω═![]() ×100%═80.0%,故答案为:0.4000;80.0%;
×100%═80.0%,故答案为:0.4000;80.0%;
(5)①开始俯视,滴定终点平视,导致计算出的标准液体积偏大,浓度偏高,故答案为:偏高;
②若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,导致待测液的物质的量增加,消耗的标准液体积增大,结果偏高,故答案为:偏高。


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】25℃时,水的电离达到平衡:H2OH++OH-△H>0,下列叙述正确的是( )
A. 向平衡体系中加入水,平衡正向移动,c (H+)增大
B. 将水加热,Kw增大,pH不变
C. 向水中加入少量硫酸氢钠固体, 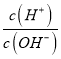 增大
增大
D. 向水中加入少量NaOH固体,平衡正向移动,c(H+)降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.5 mol Na和0.5 mol Mg分别投入到过量的m1 g水和m2 g盐酸中,分别得到溶液a和b,若m1 = m2,则a和b的质量关系是 ( )
A.a>bB.a<bC.a=bD.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室中可通过以下反应制得:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是( )
A.CO2是氧化产物
B.H2C2O4在反应中被氧化
C.H2C2O4的氧化性强于ClO2的氧化性
D.ClO2作水处理剂时,利用了其强氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于反应2Na+2H2O=2NaOH+H2↑的说法错误的是( )
A.属于氧化还原反应
B.金属钠发生还原反应
C.水发生还原反应
D.H2是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其化合物在科学研究和工业生产中具有重要的用途。
(1)三氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:
①此配合物中,铁离子价电子排布图为_____;
②此配离子中碳原子的杂化轨道类型为_____;
③此配离子中含有的化学键为_____。
A.离子键 B.金属键 C.极性键 D.非极性键 E.配位键 F.氢键 G.σ键 H.π键
(2)NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验K+的存在。NO2-离子的VSEPR模型名称为_____,K3[Co(NO2)6]是黄色沉淀,该物质中四种元素的电负性由大到小的顺序是_____。
(3)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2,其中适合作录音带磁粉原料的是_____。

(4)锰的一种配合物的化学式为Mn(BH4)2(THF)3,写出两种与BH4-互为等电子体的微粒_____(请写一个分子和一个离子)。
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶体的结构如图所示,a的配位数为_____,已知晶胞密度为ρ g/cm3,则相邻2个b微粒之间的距离为_____nm(列计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com