
【题目】某化学兴趣小组用下图装置制取并探究氯气的性质。[A装置中发生反应的化学方程式:2KMnO4+16HCl(浓)=2KCl+2MnCl2 + 5Cl2↑+ 8H2O ]

(实验探究)
(1)A装置中a仪器的名称是_____________。
(2)制取氯气反应中KMnO4所起的作用是_____(填“氧化剂”或“还原剂”)。
(3)实验进行一段时间后,可观察到______(填“B”或“C”)装置中有色布条褪色,其褪色原因是______________________________________。
(4)当氯气进入D装置后,可观察到溶液颜色变为____(填“红色”或“蓝色”),写出该反应的离子方程式为为_____________________________________。
(5)E装置中反应的化学方程式为_____________________________________。
(6)用31.6 g KMnO4固体与足量的浓盐酸反应,最多可生成标准状况下_____L氯气。(KMnO4的摩尔质量为158 g·mol—1)
(7)近年来,某些含氯的化合物(如ClO2、NaClO等)在生产、生活中应用广泛。
①高效净水剂ClO2中氯元素的化合价为_____________。
②NaClO是一种强氧化剂。某种家用洗涤剂含有NaClO,请写出NaCIO在洗涤过程中的一种作用___________________________________________。
【答案】分液漏斗 氧化剂 C 氯气与水反应生成漂白性物质(HCIO) (其它合理答案也给分) 蓝色 Cl2 + 2I-=2Cl-+ I2 Cl2 + 2NaOH = NaCl + NaClO + H2O 17.92 +4 杀菌(或消毒或漂白)等作用(其它合理答案也给分)
【解析】
(1)、根据中学化学常见的实验仪器名称,滴加浓盐酸时用分液漏斗;
(2)、据化学反应前后Mn元素价态,并根据“升失氧化还,降得还原氧"来分析;
(3)、据Cl2本身不具有漂白性,但是Cl2与H2O反应生成的HClO具有漂白性来分析;
(4)、氯气具有强氧化性,能够氧化碘离子生成单质碘,碘遇到淀粉变蓝;
(5)、氯气有毒不能直接排放到空气中;
(6)、据方程式2KMnO4+16HCl (浓) =2 KCl+2MnCl2+8Cl2↑+8H2O计算;
(7)①、据物质化合价代数和为0分析;
②、据NaClO是一种强氧化剂来分析。
(1)、滴加浓盐酸时用分液漏斗,
故答案为:分液漏斗;
(2)、由方程式2KMnO4+16HCl (浓) =2 KCl+2MnCl2+8Cl2↑+8H2O得反应前后Mn元素价态降低,并根据“升失氧化还,降得还原氧"分析得KMnO4是氧化剂,
故答案为:氧化剂;
(3)、因为干燥的Cl2本身不具有漂白性,不能将有色物质褪色,故B干燥布条不变色,C中布条有水,因此Cl2+ H2O= HCl+ HClO,生成的HClO具有漂白性能将有色物质褪色,故C褪色,
故答案为: C;氯气与水反应生成的次氯酸具有漂白性;
(4)、氯气具有强氧化性,能够氧化碘离子生成单质碘,化学方程式:Cl2 + 2I-=2Cl-+ I2,碘遇到淀粉变蓝,所以会看到溶液变蓝;
故答案为:蓝色;Cl2 + 2I-=2Cl-+ I2 ;
(5)、氯气是酸性有毒气体,不能直接排放到空气中,因此用碱液吸收;
故答案为:Cl2 + 2NaOH = NaCl + NaClO + H2O;
(6)、n(KMnO4)=![]() = 0.2mol,2KMnO4 + 16HCl(浓) = 2KCl+ 2MnCl2 +8Cl2↑+8H2O,
= 0.2mol,2KMnO4 + 16HCl(浓) = 2KCl+ 2MnCl2 +8Cl2↑+8H2O,
2mol 8×22.4L
0.2mol 0.8×22.4L
故答案为:17.92;
(7)①、O元素化合价为-2价,化合物中化合价代数和为0,Cl元素的化合价为+4价,
故答案为:+4 ;
②、NaClO是一种强氧化剂因此可用于杀菌消毒,NaClO本身又具有漂白性,
故答案为:杀菌,消毒,漂白。


 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:
【题目】SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
(1)SCR(选择性催化还原)工作原理:
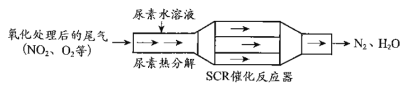
①尿素[CO(NH2)2]水溶液热分解为NH3和CO2,该反应的化学方程式:__________________
②反应器中NH3还原NO2的化学方程式:________________________;
③当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒。用化学方程式表示(NH4)2SO4的形成:_____________________________;
④尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60 g·mol 1)含量的方法如下:取a g尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的v1 mL c1 mol·L1 H2SO4溶液吸收完全,剩余H2SO4用v2 mL c2 mol·L1 NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是_________________;
(2)NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图a所示。
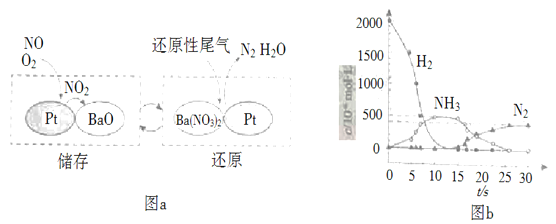
①通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。还原NOx的物质是_________________;
②用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第二步反应消耗的NH3与Ba(NO3)2的物质的量之比是__________________;
③还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有氧条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。将该反应的化学方程式补充完整:__________________![]() ____15NNO+___H2O
____15NNO+___H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年1月3日上午,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背面的软着陆。所搭载的“玉兔二号”月球车,通过砷化镓(GaAs)太阳能电池提供能量进行工作。回答下列问题:
(1)基态As原子的价电子排布图为____________,基态Ga原子核外有________个未成对电子。
(2)镓失去电子的逐级电离能(单位:kJmol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为____和+3,砷的电负性比镓____(填“大”或“小”)。
(3)1918年美国人通过反应:HC≡CH+AsCl3![]() CHCl=CHAsCl2制造出路易斯毒气。在HC≡CH分子中σ键与π键数目之比为________;AsCl3分子的空间构型为___________。
CHCl=CHAsCl2制造出路易斯毒气。在HC≡CH分子中σ键与π键数目之比为________;AsCl3分子的空间构型为___________。
(4)砷化镓可由(CH3)3Ga和AsH3在700℃制得,(CH3)3Ga中碳原子的杂化方式为_______
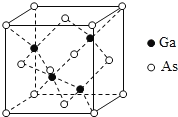
(5)GaAs为原子晶体,密度为ρgcm-3,其晶胞结构如图所示, Ga与As以_______键键合。Ga和As的原子半径分别为a pm和b pm,设阿伏伽德罗常数的值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为_______________(列出计算式,可不化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25 g·L-1。某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。


(1)仪器A的名称是_________,水通入A的进口为_________。
(2)B中加入300.00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为______________________________________________________。
(3)除去C中过量的H2O2,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的_________;若滴定终点时溶液的pH=8.8,则选择的指示剂为_________;若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积(填序号)_________(①=10 mL,②=40 mL,③<10 mL,④>40 mL)。
(4)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为_________g·L-1。
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B卷题.某兴趣小组为了提高电池的效率,设计了下图所示的原电池。
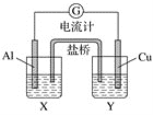
请回答下列问题:
(1)若X是AlCl3溶液,Y是稀硫酸,请你写出电极反应式和总反应式:
Al片上的电极反应式__________________________________,
Cu片上的电极反应式__________________________________,
总反应的方程式:________________________________________________。
(2)若X是浓硝酸,Y是NaCl溶液,请你写出电极名称及电极反应:
Al片上的电极反应式__________________________________,
Cu片上的电极反应式__________________________________,
总反应的方程式:________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 95℃时纯水的pH<7,说明加热可导致水呈酸性
B. pH=3的醋酸溶液,稀释至10倍时溶液的pH<4
C. 等浓度的醋酸溶液与氢氧化钠溶液等体积混合后pH=7
D. 等体积pH均为3的醋酸和盐酸分别与足量Zn反应,盐酸产生的H2多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己烯雌酚是一种激素类药物,结构如 ![]() 下列叙述中正确的是
下列叙述中正确的是
A. 分子中有7个碳碳双键,可以与氢气1:7加成
B. 该分子中有2个H,2个O,6个C共直线
C. 该分子对称性好,所以没有顺反异构
D. 该有机物分子中,最多可能有18个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1 mol·L-1某一元酸(HA)溶液中![]() =1×10-8,下列叙述正确的是
=1×10-8,下列叙述正确的是
A.溶液中水电离出的c(H+)=10-10 mol·L-1
B.溶液中c(H+)+c(A-)=0.1 mol·L-1
C.与0.05 mol·L-1 NaOH溶液等体积混合后所得溶液中离子浓度大小关系为:c(A-)>c(Na+)>c(OH-)>c(H+)
D.上述溶液中加入一定量CH3COONa晶体或加水稀释,溶液c(OH-)均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒压、NO和O2的起始浓度一定的条件下发生反应,在相同时间内,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法不正确的是( )
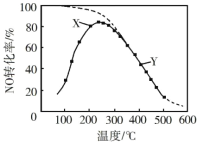
A.反应2NO(g) + O2(g) = 2NO2(g)的H<0
B.图中X点所示条件下,由于测定时间较短,反应未达到平衡
C.从 X→Y 过程中,平衡逆向移动,O2反应量减少
D.380℃下,c 平衡(O2)=5.0×104 mol·L1,NO 平衡转化率为 50%,则平衡常数 K=2000
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com