
【题目】能正确表示下列反应的离子方程式是( )
A. 大理石溶于醋酸中:CaCO3+2H+═Ca2++CO2↑+H2O
B. 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+
C. MnO2与浓盐酸反应制Cl2:MnO2+4H++4Cl﹣![]() Mn2++2Cl2↑+2H2O
Mn2++2Cl2↑+2H2O
D. 浓硝酸中加入过量铁粉并加热:Fe+3NO3﹣+6H+![]() Fe3++3NO2↑+3H2O
Fe3++3NO2↑+3H2O
科目:高中化学 来源: 题型:
【题目】将钠放入盛有空气的密闭容器中,生成Na2O还是Na2O2是由下列哪项因素所决定的( )
A.反应温度B.空气的量C.钠粒的大小D.钠的状态(s、l)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C都是常见有机物,其转化关系如下(部分反应物、产物和反应条件已略去):
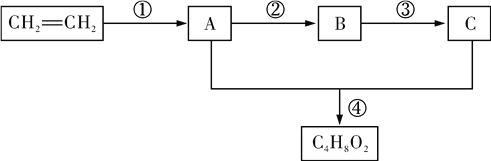
请回答下列问题:
(1)写出①的反应类型______________;
(2)写出C中官能团的名称____________;
(3)写出反应②的化学方程式________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G(分子式为C13H18O2)是一种香料,如图是该香料的一种合成路线。

已知:
①E能发生银镜反应,在一定条件下,1 mol E能与2 mol H2反应生成F;
②R—CH===CH2![]() R—CH2CH2OH;
R—CH2CH2OH;
③有机物D的摩尔质量为88 g·mol-1,其核磁共振氢谱有3组峰;
④有机物F是苯甲醇的同系物,苯环上只有一个无支链的侧链。
回答下列问题:
(1)用系统命名法命名有机物B________________;
(2)E的结构简式为__________________________;
(3)C与新制Cu(OH)2反应的化学方程式为____________________________;
(4)已知有机物甲符合下列条件:①为芳香族化合物;②与F互为同分异构体;③能被催化氧化成醛。符合上述条件的有机物甲有________种,写出一种满足苯环上有3个侧链,且核磁共振氢谱有5组峰,峰面积比为6∶2∶2∶1∶1的有机物的结构简式____________________;
(5)以丙烯等为原料合成D的路线如下:

X的结构简式为_______,步骤Ⅱ的反应条件为___________,步骤Ⅳ的反应类型为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)纯碱(![]() )、小苏打(
)、小苏打(![]() )广泛应用在食品加工。苏打饼干原料中含有小苏打,在烘焙受热过程,小苏打发生分解反应,该反应的化学方程式是______;苏打饼干可以适当缓解人体胃酸(主要成分盐酸)过多症状,该反应的化学方程式是_______。
)广泛应用在食品加工。苏打饼干原料中含有小苏打,在烘焙受热过程,小苏打发生分解反应,该反应的化学方程式是______;苏打饼干可以适当缓解人体胃酸(主要成分盐酸)过多症状,该反应的化学方程式是_______。

(2)某同学利用如图装置(夹持仪器已略去)研究纯碱和小苏打的性质。
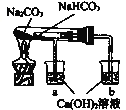
①该实验的目的是_______。
②观察到有白色沉淀生成的烧杯是_________(填字母序号)。
③实验结论是__________。
④为进一步定量研究碳酸氢钠的性质,甲同学用天平准确称量![]() 碳酸氢钠,放入质量为
碳酸氢钠,放入质量为![]() 的坩埚中加热,冷却称量,理论上坩埚及剩余固体的总质量为______
的坩埚中加热,冷却称量,理论上坩埚及剩余固体的总质量为______![]() ,但实际称得的质量比该数值要大,可能的原因是________,改进的操作方法是_______________。
,但实际称得的质量比该数值要大,可能的原因是________,改进的操作方法是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙均为单质,它们的转化关系如图所示(某些条件和部分产物已略去)。下列说法不正确的是:
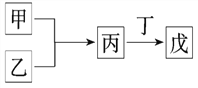
A. 若甲既能与盐酸反应又能与NaOH溶液反应,则丙可能属于两性氧化物
B. 若丙、丁混合产生白烟,且丙为18电子分子,丁为10电子分子,则乙的水溶液可能具有漂白作用
C. 若甲为短周期中原子半径最大的主族元素的单质,且戊为碱,则丙只能为Na2O2
D. 若甲、丙、戊含有同一种元素,则三种物质中,该元素的化合价由低到高的顺序可能为甲<丙<戊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究小组用下图装置制取Cl2,证明产生的气体中含有HCl。
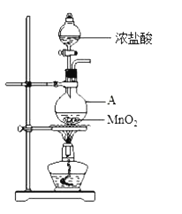
(1)仪器A的名称为________;A中反应的离子方程式为________。
(2)甲同学将A中产生的气体通入下列溶液:
实验序号 | 试剂 | 现象 |
a | 紫色石蕊溶液 | |
b | AgNO3溶液 | 出现白色沉淀 |
①实验a中的现象为________。
②不能证明产生的气体中含有HCl的实验是________(填字母序号)。
(3)已知将HCl气体通入饱和食盐水中有白色固体析出。乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因:______________________________________。
(4)已知:2S2O32-+I2=== S4O62-+2I-。丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl。
I.测定X中溶解的Cl2。取25.00 mL溶液X,加入过量KI溶液,然后用0.04 molL-1 Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3溶液V mL。
II.测定X中Cl元素总量。另取25.00 mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl-,再用0.10 molL-1 AgNO3溶液滴定所得溶液中的Cl-。
①X中的HClO不会影响I的测定结果,原因是________。
②由I、II 中实验数据可证明A中产生的气体中含有HCl,则II中消耗0.10 molL-1 AgNO3溶液的体积应大于________mL(用含V的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com