
����Ŀ��Һ��������ֽ��������������Ϊȼ�Ϲ�������ȼ�ϵ�ء�
��֪��2NH3(g) ![]() N2 (g)+3H2(g) ��H= 92.4 kJ��mol-1
N2 (g)+3H2(g) ��H= 92.4 kJ��mol-1
2H2 (g)+O2 (g)=2H2O(g) ��H= - 483.6 kJ��mol-1
NH3(l) ![]() NH3 (g) ��H= 23.4 kJ��mol-1
NH3 (g) ��H= 23.4 kJ��mol-1
(1) 4NH3(l)+3O2 (g)![]() 2N2(g)+6H2O(g) �ġ�H=______���÷�Ӧ��ƽ�ⳣ������ʽΪ______��
2N2(g)+6H2O(g) �ġ�H=______���÷�Ӧ��ƽ�ⳣ������ʽΪ______��
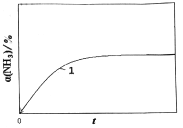
(2) 2NH3(g) ![]() N2(g)ʮ3H2(g)���Է���������_________������¡����¡��������£�T1������ʱ�����ֽ��ʼŨ��Ϊc0�İ������ð�����ת���ʦ�(NH3)��ʱ��t�仯�Ĺ�ϵ��ͼ����1��������������������䣬����Ӧ�¶���ߵ�T2������ͼ��������һ�����ֽ��ʼŨ��ҲΪc0�İ��������Ц�(NH3)��t������������_________����ע2����
N2(g)ʮ3H2(g)���Է���������_________������¡����¡��������£�T1������ʱ�����ֽ��ʼŨ��Ϊc0�İ������ð�����ת���ʦ�(NH3)��ʱ��t�仯�Ĺ�ϵ��ͼ����1��������������������䣬����Ӧ�¶���ߵ�T2������ͼ��������һ�����ֽ��ʼŨ��ҲΪc0�İ��������Ц�(NH3)��t������������_________����ע2����
(3)���о����������¶ȴ���70�桢������������Һ�У���ͨ����ⷨ��ԭ�����õ�������д�������ĵ缫��Ӧʽ______________________��
(4) 25��ʱ����amol/L�İ�ˮ��b mol/L����������ϣ�����仯���Բ��ƣ�����Ӧ����Һǡ�������ԣ���a��b��ʾNH3��H2O�ĵ���ƽ�ⳣ��Ϊ_______________��
���𰸡� -1172.4kJ/mol 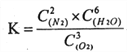 ����
����  N2+3H2O+6e-=2NH3+6OH-
N2+3H2O+6e-=2NH3+6OH- ![]()
�����������⿼���˹���ɵ�Ӧ�ã���Ӧ�Է����е��жϣ����ԭ����Ӧ�ü�����ƽ�ⳣ����֪ʶ�����ݾ���֪ʶ��ɡ�
��1����2NH3(g) ![]() N2 (g)+3H2(g) ��H= 92.4 kJ��mol-1����2H2 (g)+O2 (g)=2H2O(g) ��H= - 483.6 kJ��mol-1����NH3(1)
N2 (g)+3H2(g) ��H= 92.4 kJ��mol-1����2H2 (g)+O2 (g)=2H2O(g) ��H= - 483.6 kJ��mol-1����NH3(1) ![]() NH3 (g) ��H= 23.4 kJ��mol-1���ɸ�˹���ɣ�2����+3����+4���۵õ���Ӧ4NH3(l)+3O2 (g)
NH3 (g) ��H= 23.4 kJ��mol-1���ɸ�˹���ɣ�2����+3����+4���۵õ���Ӧ4NH3(l)+3O2 (g)![]() 2N2(g)+6H2O(g) �ġ�H=92.4��2+��-483.6����3+23.4��4=-1172.4kJ/mol�����ݻ�ѧƽ�ⳣ���ĺ��壬�÷�Ӧ��ƽ�ⳣ������ʽΪ
2N2(g)+6H2O(g) �ġ�H=92.4��2+��-483.6����3+23.4��4=-1172.4kJ/mol�����ݻ�ѧƽ�ⳣ���ĺ��壬�÷�Ӧ��ƽ�ⳣ������ʽΪ![]() ��
��
��2����֪2NH3(g) ![]() N2 (g)+3H2(g) ��H= 92.4 kJ��mol-1����Ӧ����������ʵ����������S��0�����ҡ�H��0����Ҫʹ��H-T����S��0�������ڽϸ��¶��£�����2NH3(g)
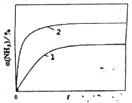
N2 (g)+3H2(g) ��H= 92.4 kJ��mol-1����Ӧ����������ʵ����������S��0�����ҡ�H��0����Ҫʹ��H-T����S��0�������ڽϸ��¶��£�����2NH3(g) ![]() N2(g)ʮ3H2(g)���Է����е������Ǹ���������Ӧ�¶���ߵ�T2����Ӧ���ʼӿ죬����ƽ������ʱ�����̣������ķֽⷴӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���������ת����������T2�¶�ʱ�����ֽ��ʼŨ��Ϊc0�Ĺ����Ц���NH3����t������������Ϊ
N2(g)ʮ3H2(g)���Է����е������Ǹ���������Ӧ�¶���ߵ�T2����Ӧ���ʼӿ죬����ƽ������ʱ�����̣������ķֽⷴӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���������ת����������T2�¶�ʱ�����ֽ��ʼŨ��Ϊc0�Ĺ����Ц���NH3����t������������Ϊ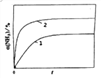 ��
��
��3���������⣬��ⷨ��ԭ�����õ������������ǵ����õ��ӷ�����ԭ��Ӧ���ɰ�����1mol������6mol���ӣ�����OH��ƽ���ɣ�Ȼ����ԭ���غ���ƽ�����缫��ӦʽΪN2+3H2O+6e-=2NH3+6OH- ��
��4����amol/L�İ�ˮ��bmol/L������������ϣ���Ӧ����Һ�����ԣ�����Һ��c(H��)=c��OH-��=1��10-7mol/L�����ݵ���غ�c(Cl-)+c(OH-)=c(NH4+)+c(H+)����Һ��c��NH4+��=c��Cl-��=![]() mol/L����Ϻ�Ӧǰc��NH3H2O��=
mol/L����Ϻ�Ӧǰc��NH3H2O��=![]() mol/L����Ӧ��c��NH3H2O��=��
mol/L����Ӧ��c��NH3H2O��=��![]() -
-![]() ��mol/L��mol/L��Kb=[c(NH4�� )��c(OH��)]��c(NH3��H2O)=
��mol/L��mol/L��Kb=[c(NH4�� )��c(OH��)]��c(NH3��H2O)=![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̫���ܵ�ذ����̫��ʱ��һ���ֵ���ֱ�ӹ������칬һ������һ���ֵ������ڵ���������̫��ʱʹ�á����칬һ����ʹ�õ��������أ��������Һ�Լ��ԡ��䷴Ӧ����ʽΪ�� LaNi5+Ni(OH)2![]() LaNi5H+NiOOH�������й�˵������ȷ����
LaNi5H+NiOOH�������й�˵������ȷ����
A. �ŵ�ʱ������ԭ B. �ŵ�ʱ����LaNi5H+OH����e����LaNi5+H2O
C. ���ʱOH���������ƶ� D. ���ʱÿ����lmol Ni(OH)2ת��lmol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��50 mL 0.50mol��L��1������50 mL 0.55mol��L��1 NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ���ش��������⣺
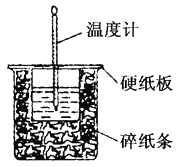
��1��С�ձ��з�����Ӧ�����ӷ���ʽΪ�� ________________________________��
��2����ʵ���з�Ӧ����������,�¶ȼ���ʾ�¶�����,˵���÷�Ӧ��__________��Ӧ(����ȡ������ȡ�)
��3���������ĽǶȿ�,�Ͽ���ѧ��Ҫ________________���γɻ�ѧ��Ҫ_________________________��
��4����ʵ���е�ҩƷ��Ϊ��Ƭ��ϡ���ᣬ�¶ȼ���ʾ�¶�������������Ӧ�Ļ�ѧ����ʽΪ______________________,��Ӧ���������__________�������������(����ڡ���С�ڡ�)
��5��Ŀǰ��ȫ������Ҫ���ڻ�ʯ��Դʱ�ڣ������й���Դ˵����ȷ����__________��
A��ú��ʯ�͡���Ȼ�����ڿ�ʯ��Դ����ȡ֮������֮���ߵģ����Դ���ʹ��
B����������Ҫ�ɷ��Ǽ״�����һ�������Դ
C��̫���ܡ����ܡ����ܵ��Ժ�Ϊ�ṩ��Դ����Ҫ��ʽ
D�������÷��ܷ����������ˮ���ڵĵ��ܲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����SO2ͨ��BaCl2��Һ�����ͣ�δ���������ɣ�����ͨ����һ�����壬���������tͨ������������
A. CO2 B. NH3 C. NO2 D. Cl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
���ཬ����ɳ��������ˮ���ܼ�
��ҽ�þƾ��У�ˮ���ܼ����ƾ�������
��������ɢ����ͨ����Ĥ�ķ�ɢϵ�����ڽ���
��ͨ�������������Լ���������Һ
A���٢ڢۢ� B���ڢ� C���ڢ� D���٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A. ������![]() ��������2-�һ�����
��������2-�һ�����
B. 2-�������2��2-�������黥Ϊͬϵ��
C. �����£���ϩ�ͱ����ܱ�����KMnO4������ʹKMnO4��Һ��ɫ
D. �����ʵ�������ϩ���Ҵ���ȫȼ�գ��������������ʵ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ��X��Ԫ��Yλ�ڵڶ����ڣ�����X��ԭ��������о�������δ�ɶԵ��ӣ�Y��ԭ��ֻ��������״�ĵ����ƣ���������״�ĵ����Ƶĵ�������ȣ�����x��y��ɵ����У������ܴ��ڵ���
A. X2Y5 B. XY42- C. XY2- D. XY3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D��E��F��Ԫ�����ڱ���ǰ36��Ԫ�أ����ǵ�ԭ��������������A�������������Ӳ�������������������ȣ�BԪ�ػ�̬ԭ���е���ռ������������ͬ��ԭ�ӹ����ÿ�ֹ���еĵ���������ͬ��D�Ļ�̬ԭ�Ӻ���ɶԵ������dzɵ���������3����E4+���ԭ�ӵĺ�������Ų���ͬ��F�ǵ�������d��ԭ����������Ԫ�ء���ش��������⣺
��1��д��E�ļ۲�����Ų�ʽ ��
��2��A��B��C��D�縺���ɴ�С��˳��Ϊ________________����Ԫ�ط��ţ���
��3��F(BD)4Ϊ��ɫ�ӷ��Ծ綾Һ�壬�۵�-25�� ���е�43����������ˮ���������Ҵ������ѡ������л��ܼ����������幹�ͣ��þ��������Ϊ ��F��BD֮���������Ϊ ��
��4���������ʹ���������������õ���Ҫ�о�����
����A��B��E����Ԫ�ع��ɵ�ij�����ʹ�����ϵ����۽ṹģ����ͼ1��ʾ��ͼ�����߿���Bԭ�ӵ��ӻ���������� �֣�
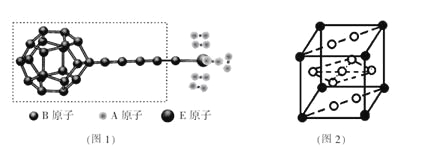
������X����ͨ������γ�����״�ṹ������ΪDZ�ڵĴ�����ϡ�Xһ������ �����ţ���
A.H20 B. CH4C.HF D.CO(NH2)2
��FԪ������( La)Ԫ�صĺϽ����������ϣ��þ���ľ�����ͼ2��ʾ������������һ��Fԭ�ӣ�����Fԭ�Ӷ��ھ������ϣ���þ���Ļ�ѧʽΪ ����֪��Ħ������ΪMg��mol-1����������Ϊapm����NA��ʾ����٤����������þ������ܶ�Ϊ g��cm-3��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com