
【题目】25℃时,向0.1molL-1NaA溶液中逐滴滴加盐酸,测得混合溶液的pH与p![]() 变化关系如图所示[p
变化关系如图所示[p![]() =-lg
=-lg![]() ]。下列说法正确的是( )
]。下列说法正确的是( )
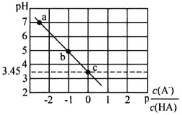
A.a点溶液中c(Na+)=c(A-)
B.电离常数K(HA)的数量级为10-4
C.滴加过程中![]() 不断减小
不断减小
D.b点溶液中c(HA)>c(Na+)>c(A-)>c(OH-)
【答案】B
【解析】
A.从图中信息可以看出a点溶液为中性即氢离子浓度等于氢氧根离子浓度,由电荷守恒可知:![]() 所以
所以![]() ,故A 错误;
,故A 错误;
B.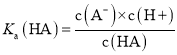 ,横坐标为0时,
,横坐标为0时,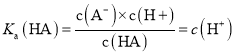 ,这时pH为
,这时pH为![]() , p
, p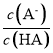 =lg
=lg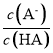 =0,
=0,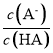 =1,Ka(HA)=
=1,Ka(HA)=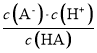 =c(H+)=103.45,则Ka(HA)的数量级为104,故B正确;
=c(H+)=103.45,则Ka(HA)的数量级为104,故B正确;
C. p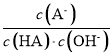 =lg
=lg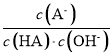 =lg
=lg  =lg
=lg![]() ,温度不变,Ka(HA)、Kw不变,则滴加过程中p
,温度不变,Ka(HA)、Kw不变,则滴加过程中p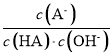 保持不变,故C错误;
保持不变,故C错误;
D.b点溶液中,pH=5,p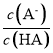 =lg
=lg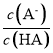 =1,
=1,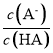 =10,则c(HA)<c(A),根据物料守恒c(Na+)=c(HA)+c(A)可知,c(Na+)>c(A),正确的离子浓度大小为:c(Na+)>c(A)>c(HA) >c(OH),故D错误;
=10,则c(HA)<c(A),根据物料守恒c(Na+)=c(HA)+c(A)可知,c(Na+)>c(A),正确的离子浓度大小为:c(Na+)>c(A)>c(HA) >c(OH),故D错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】R、X、Y、Z是周期表前四周期元素,原子序数依次增大。R是宇宙中含量最多的元素,X、Y、Z三种元素的基态原子内层所有能级均已填满电子。X元素的基态原子的核外电子分布在三个能级上,且每个能级上排布了相同的电子数。Y与X同周期,且Y与X的基态原子中未成对电子数相同。Z的周期数比X的周期数多2,Z的基态原子最外层只有1个电子。回答下列问题:
(1)Z元素的价电子排布式为____________。
(2)R2Y可与Z的正二价离子形成一种复杂离子[Z(R2Y)4]2+,[Z(R2Y)4]2+的几何构型是______;将[Z(R2Y)4]2+与硫酸根形成的盐溶液装入试管中,逐滴加入氨水直至过量,出现的实验现象是______________。
(3)X与R可形成一种化学式为X3R4的不稳定化合物,是一种话性中间体,X3R4分子中3个X原子成直线排列,中间的X原子的杂化轨道类型为_____杂化。当X3R4分子中的4个R原子被其他4个不同种类元素的原子取代时,形成的新分子___(填“具有“或”不具有”)手性。
(4)下列排列方式中,通常条件下Z的晶体的堆积方式是______(填序号)。Z的晶体中,Z原子的配位数为________。
A.ABCABCABC B.ABABABABAB C.ABBAABBA D.ABCCBCABCCBA
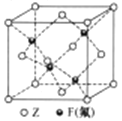
(5)Z与F(氟)形成的一种化合物的晶胞结构如右图所示,若晶体密度为ag.cm-3,则Z与F(氟)最近距离为______pm(阿伏加德罗常数用NA表示,列出计算表达式,不用化简,1pm=1.0×10-12m)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】清华大学王晓琳教授首创三室电解法制备LiOH,其工作原理如图所示,下列说法不正确的是( )

A.X电极连接电源正极
B.M为阴离子交换膜
C.Y电极反应式为![]()
D.制备2.4gLiOH产生的H2在标准状况下为1.12L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验离不开水。请根据水的不同作用和功能,分析以下四个装置图,回答问题:
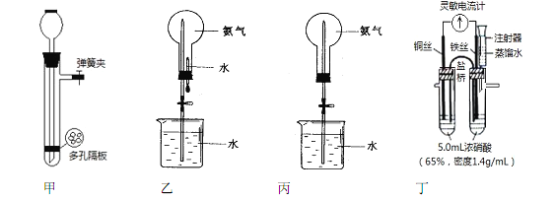
实验一:制取氢气
(1)图甲所示装置可用于实验室制取氢气,这种制气装置在加入反应物前,如何检查气密性______。
(2)用锌与稀硫酸制取氢气时,加入少量硫酸铜溶液会加快产生氢气的速率,请解释加快反应速率的原因:________________________________。
实验二:喷泉实验
(3)图乙所示装置中烧瓶已装满干燥氨气, 进行喷泉实验时应该先___________(填“挤捏胶头滴管”或“打开止水夹”)。
(4)如果只提供如图丙所示装置,若想迅速引发喷泉,下列方法可行的是____________。
a.用热毛巾捂住烧瓶
b.用冰块捂住烧瓶
c.将烧杯中的水换成饱和食盐水
d.向烧杯中加入少量硫酸
实验三:探究一定温度下能使铁钝化的硝酸的最低浓度,实验装置如图丁所示。
①开始实验时,观察到灵敏电流计指针指向铜丝,但又迅速反转指向铁丝;
②再用盛蒸馏水的注射器缓慢向具支试管内加水并振荡,在指针恰好开始反转指向铜丝时停止实验;
③重复三次实验得平均加水量为2.5 mL(水的密度按1.0g/mL计算)。
(5)该实验装置的不足之处是__________________________________。
(6)当指针第一次指向铜丝时,正极的电极反应式为_______________________________。
(7)根据此实验计算,使铁钝化的硝酸最低质量分数为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是合成新农药的重要中间体。以化合物A为原料合成化合物G的工艺流程如下:

(1)化合物G中含氧官能团的名称为________。
(2)反应D→E的反应类型为________。
(3)化合物B的分子式为C7H6Cl2,B的结构简式为______。
(4)写出同时满足下列条件的G的一种同分异构体的结构简式:______。
①能发生银镜反应;
②核磁共振氢谱显示氢原子的峰值比为3∶2∶2∶1。
(5)请以化合物F和CH2(COOC2H5)2为原料制备 ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在20 mL 0.1 mol·L-1一元弱酸HA溶液中滴加0. 1 mol· L-1 NaOH溶液,溶液中1g[c(A-)/c(HA)]与pH关系如图所示。下列说法正确的是

A. A点对应溶液中:c(Na+)>c(A-)>c(H+)>c(OH-)
B. 25℃时,HA酸的电离常数为1. 0× 10-5.3
C. B点对应的NaOH溶液体积为10 mL
D. 对C点溶液加热(不考虑挥发),则c(A-)/[c(HA)c(OH-)]一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用如图所示的电化学装置电解硫酸铜溶液,有一个电极为Al,其它三个电极均为Cu,则下列说法正确的是( )

A.电子方向:电极Ⅳ→→电极ⅠB.电极Ⅰ发生还原反应
C.电极Ⅱ逐渐溶解D.电极Ⅲ的电极反应:Cu-2e-═Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。请填写下列空白:
Ⅰ.测定过氧化氢的含量
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250 mL_______(填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式为________。
(3)判断滴定到达终点的现象是_________________________。
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为____________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏高”或“偏低”或“不变”)。
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
请将他们的实验方法和实验现象填入下表:
实验内容 | 实验方法 | 实验现象 |
验证氧化性 | ____________ | ____________ |
验证不稳定性 | ____________ | ____________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示的装置,可以验证![]() 和 HCl的有关性质。实验前a、b、c活塞均关闭。
和 HCl的有关性质。实验前a、b、c活塞均关闭。

(1)若要在烧瓶Ⅱ中产生“喷泉”现象,烧瓶Ⅰ中不产生“喷泉”现象,其操作方法是 ______
(2)若先打开a、c 活塞,再挤压胶头滴管![]() 假设
假设![]() 不被完全吸收
不被完全吸收![]() ,在烧瓶Ⅱ中可观察到的现象 ______
,在烧瓶Ⅱ中可观察到的现象 ______ ![]()
(3)通过挤压胶头滴管和控制活塞的开关,在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是 ______ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com